HOME > 広報活動 > 刊行物 > July 2017 No.026

Jul. 2017 No.026
特集
研究紹介
受賞報告
開催報告
編集後記
研究紹介
パーキンソン病やレビー小体型認知症の病態解明、診断、治療に役立つことが期待されるマーモセットモデルの開発に成功
神経病理学速報紙「Acta Neuropathologica Communications (アクタ ニューロパソロジカ コミュニケーションズ)」に研修生の下沢明希(首都大学東京、博士課程)らの研究成果が発表されました。
認知症・高次脳機能研究分野 分野長長谷川 成人
1.研究の背景
αシヌクレイン*1(αS)はパーキンソン病やレビー小体型認知症の原因蛋白質であり、その異常病変の広がりと症状の相関が示されています。マウスの実験で、線維化した異常型αSを脳内へ接種すると、内在性αSが異常型に変化して蓄積し、細胞間を超えて拡がるプリオン*2様伝播の現象が実験的に観察されています。今回、よりヒトに近い動物モデルとして注目されている小型霊長類のマーモセットに、線維化した異常型αSを接種する実験を行いました。
2.研究成果の概要
マーモセットの線条体に線維化αSを接種し、3ヶ月後の脳を観察すると、線条体の他、黒質、大脳皮質、扁桃体などに異常リン酸化αS病変の出現と脳内伝播を確認しました。特に線条体から黒質に逆行性に広がり、黒質のチロシン水酸化酵素*3陽性のドパミン神経細胞内に多数の異常αS病理が形成され、それに伴い神経細胞の減少が観察されました。また、これら異常αS構造物は、チオフラビンなどのβシート構造を認識する蛍光試薬で検出されることも確認されました。マーモセットにおいても、3ヶ月という短期間で患者脳に蓄積するような異常αS病理が形成され、逆行性に伝播することが観察できました。
3.発見の意義
このマーモセットモデルは、αSの伝播メカニズムの解明をはじめ、異常αSを特異的に検出するPETプローブの評価や、進行を抑える根本治療薬の評価に役立つことが期待されます。
図.
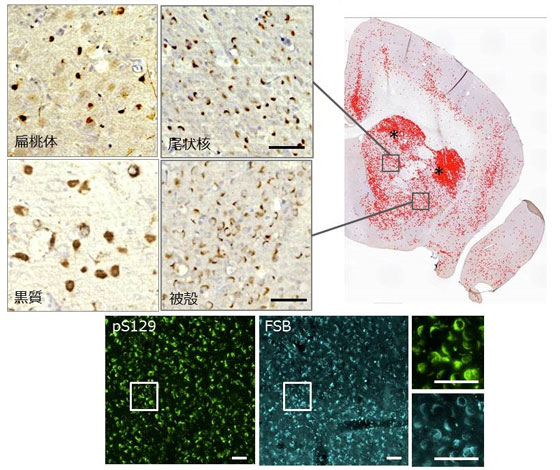
αシヌクレイン線維を接種した3ヶ月後のマーモセット右脳における異常リン酸化αシヌクレイン抗体(pS129)による免疫染色像(右図: 接種部位付近の冠状断の半球切片における病変を赤色で示す、左図: 異常リン酸化αS病変が出現した部位の拡大図 )。下図はβシートリガンドであるFSBによるαシヌクレイン病変の染色像を示す。
図.
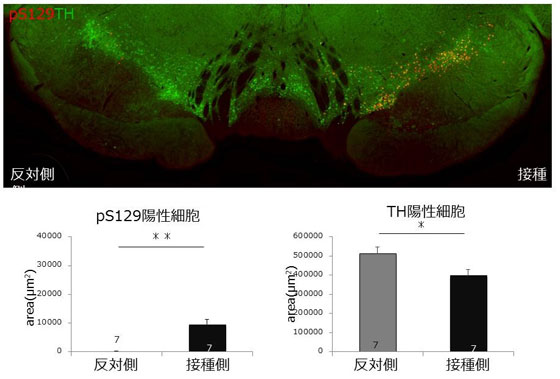
αシヌクレイン線維を接種したマーモセット右脳黒質のチロシン水酸化酵素とリン酸化αシヌクレインの免疫染色
上段: リン酸化αシヌクレイン(pS129, 赤)とTH(緑)の免疫組織染色。右側に多くのpS129陽性のαシヌクレイン凝集体が認められる。
下段: αシヌクレイン線維を接種したマーモセット脳の右側と左側のαシヌクレイン凝集体数とTH陽性神経細胞数の定量を示す。
用語解説
- *1 αシヌクレイン :
- 140アミノ酸からなるタンパク質。脳に豊富に存在し、正常ではシナプスの機能維持に働くが、パーキンソン病やレビー小体型認知症では、細胞内に線維状構造をとって凝集、蓄積し、細胞毒性を有し神経変性を引き起こすと考えられている。
- *2 プリオン :
- タンパク質のみで自己増殖し、病気(感染症)の原因となる病原体としてPrusiner博士が提唱した概念。ヒトのクロイツフェルト・ヤコブ病やウシの海綿状脳症は、正常プリオン蛋白が変化した異常型プリオン蛋白が原因であることが判明している。
- *3 チロシン水酸化酵素(TH) :
- ドパミンの合成に必要な酵素で、黒質のドパミン神経細胞のマーカーとして用いられる。
参考文献
Shimozawa A, Ono M, Takahara D, Tarutani A, Imura S, Masuda-Suzukake M, Higuchi M, Yanai K, Hisanaga SI, Hasegawa M.
Propagation of pathological α-synuclein in marmoset brain.
Acta Neuropathol Commun. 2017 Feb 2;5(1):12 doi: 10.1186/s40478-017-0413-0.

