花粉症プロジェクト研究の紹介
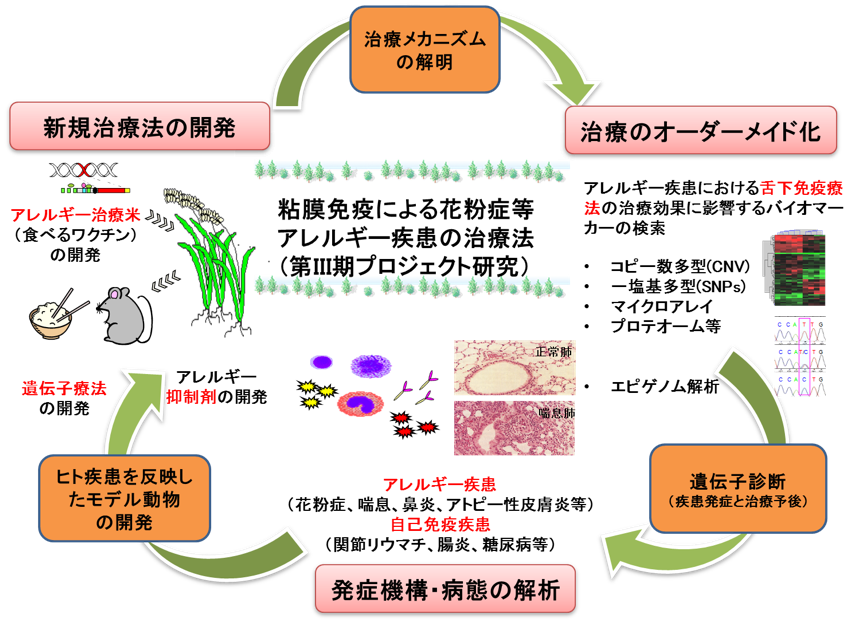
花粉症プロジェクト研究の全体像
治療のオーダーメイド化
1. スギ花粉症における舌下免疫療法の臨床研究
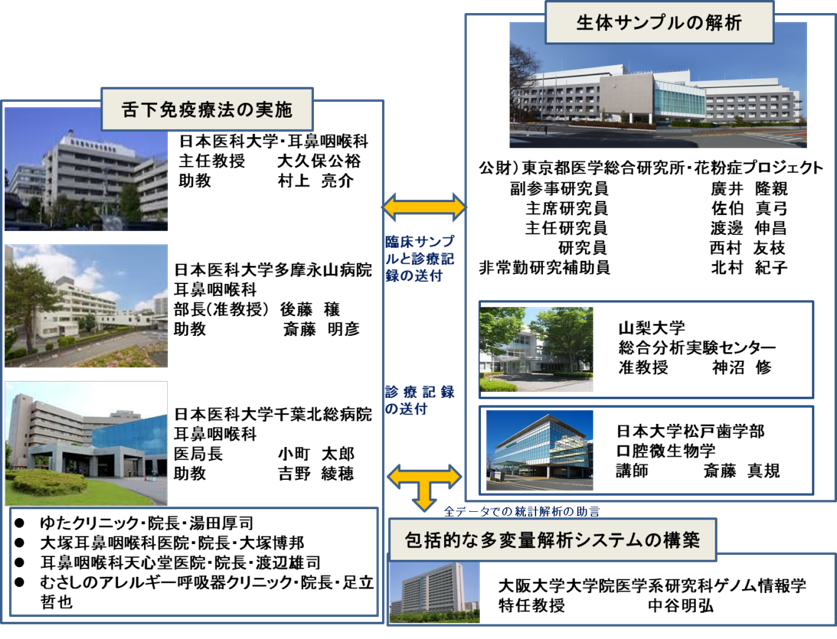
舌下免疫療法の研究組織
(A)舌下免疫療法の作用機序の解明
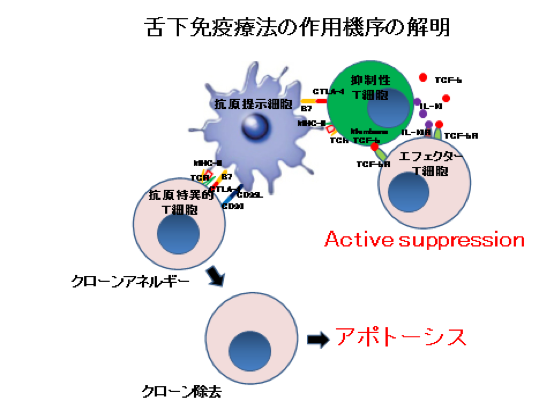
現在、アレルギー抗原(スギ花粉症)を用いた舌下免疫療法が健康保険制度下で施行されているが、この免疫療法に関しての作用機序に関して不明な点が多い。そこで本研究の目的は、粘膜免疫学のコンセプトを用いて「舌下免疫療法」の免疫寛容誘導機構を解明し、その特徴を踏まえた抗原デリバリーシステムを開発することである。これにより、将来の舌下免疫療法において科学的な根拠に基づいた医学的な効果と安全性、さらに社会学的また経済的に優れたアレルギー予防・治療薬を社会に提供することである。
(B)治療効果に関わるバイオマーカーの検索
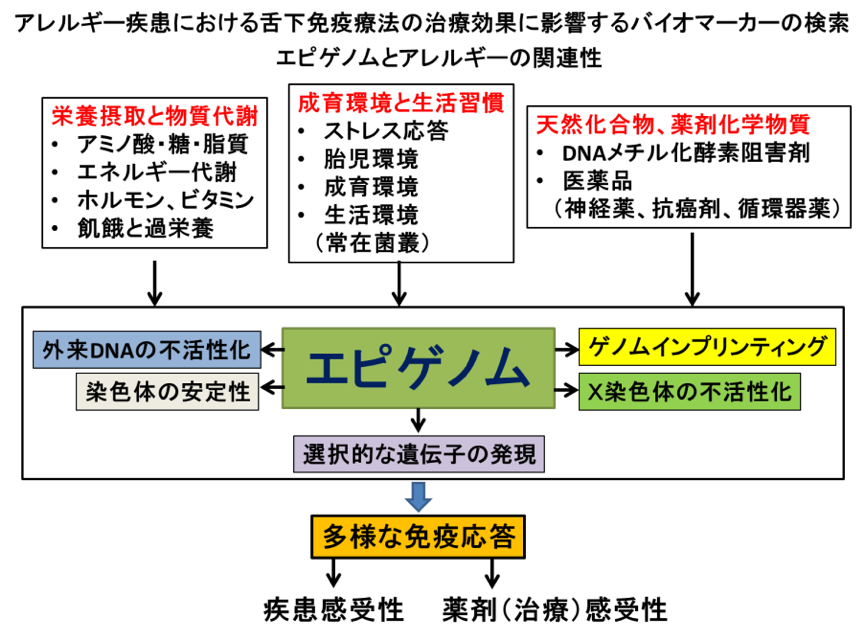
これまでアレルギーに関して、DNAの1次構造に潜む遺伝子多型(一塩基多型:SNP、コピー数多型:CNVなど)が疾患感受性や治療効果に影響するという考え方より、疾患感受性や治療標的となる関連因子の検索が行われてきた。しかし、その結果は必ずしも疾患の発生・病態や治療効果を説明するものではなく、統計学的手法により導き出された結論であり生物学的には合理性が乏しかった。一方でアレルギーは、年齢や生活環境にいたる様々な後天的要因が関連していることが知られている。本研究は、後天的要因である環境因子(食事・ストレス・栄養状態・口腔常在菌など)が、舌下免疫療法の作用機序に影響がある可能性に注目し環境因子や生活習慣とアレルギー免疫療法の関連性を明らかにし、そのバイオマーカーを見出すことによって免疫学的個性化を定義し、診断ならびに治療に寄与することである。
Allergol Int. (2018) pii: S1323-8930(18)30008-X. doi: 10.1016/j.alit.2018.02.003.
Journal of nippon medical school. (2018) In press.
Allergy, Asthma and Immunology Research. (2018) In press.
Int Immunol. 29(6):291-300 (2017)
発症機構・病態の解析
1. 免疫抑制分子CTLA-4によるTh17型腸炎増悪メカニズム
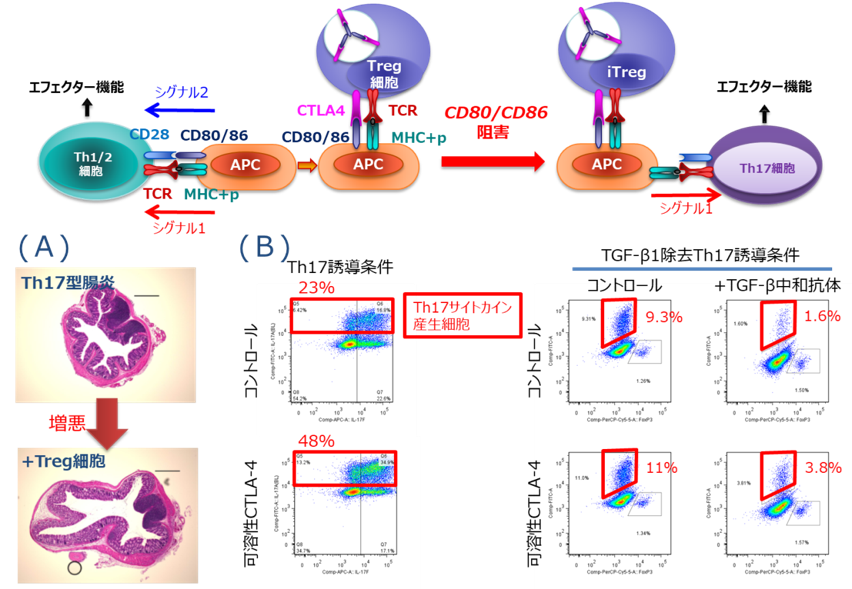
潰瘍性大腸炎やクローン病に代表される炎症性腸疾患(inflammatory bowel disease:IBD)は、不適切な免疫反応が亢進/慢性化し、組織傷害に至る自己免疫疾患と考えられるが、その詳細な発症機序に関してはよく分かってない。私たちは、単一抗原ペプチドに特異的なTh1細胞、Th2細胞およびTh17細胞を野性型マウスに移入した後、抗原を投与することにより臓器特異的アレルギー・炎症モデルの構築に成功した。その腸炎モデルを用いることにより、免疫抑制性と考えられていたTreg細胞がTh17型腸炎に対しては増悪作用を示すことを明らかにした(図A)。その作用機序は、やはり免疫抑制分子として知られているCTLA-4を介したものであることを見出した。さらに、CTLA-4のTh17増強作用は、Th17細胞分化因子であるTGF-βとは独立したものであることを明らかにした(図B)。これらの結果は、Th17型慢性炎症においては、CTLA-4分子を起点とする治療戦略に対して再検討の必要があることを示している。
PLoS ONE 11(3): e0150244. (2016)
(渡邊伸昌)
2. 気管支喘息の病態解析と新規治療法の開発
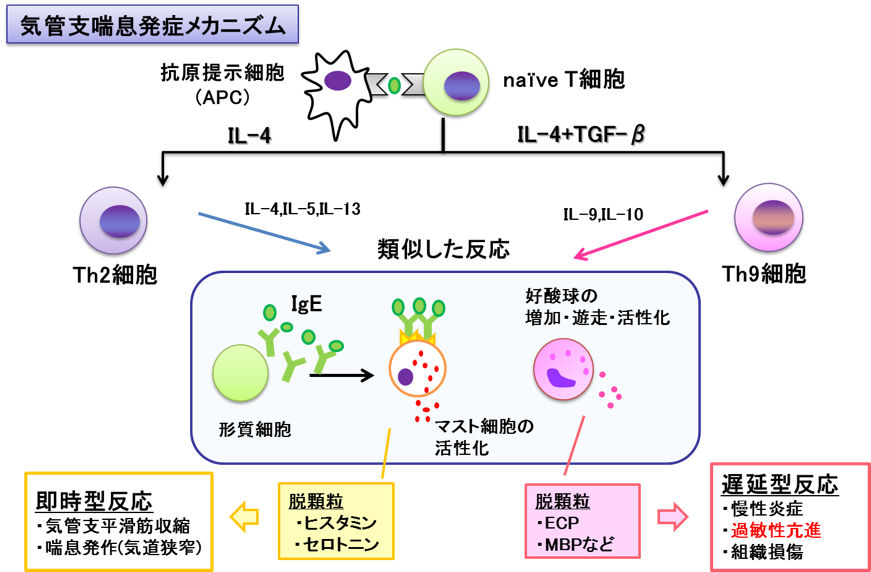
気管支喘息は、気道の慢性炎症、狭窄、過敏性の亢進を伴う慢性炎症性疾患であり、その病態像は複雑な様相を呈している。喘息患者は国内に5%程度存在し、吸入ステロイドの普及により以前と比べて治療は安易になってきたが、その中でも約5~10%の患者はステロイド効果がなく重症化している。
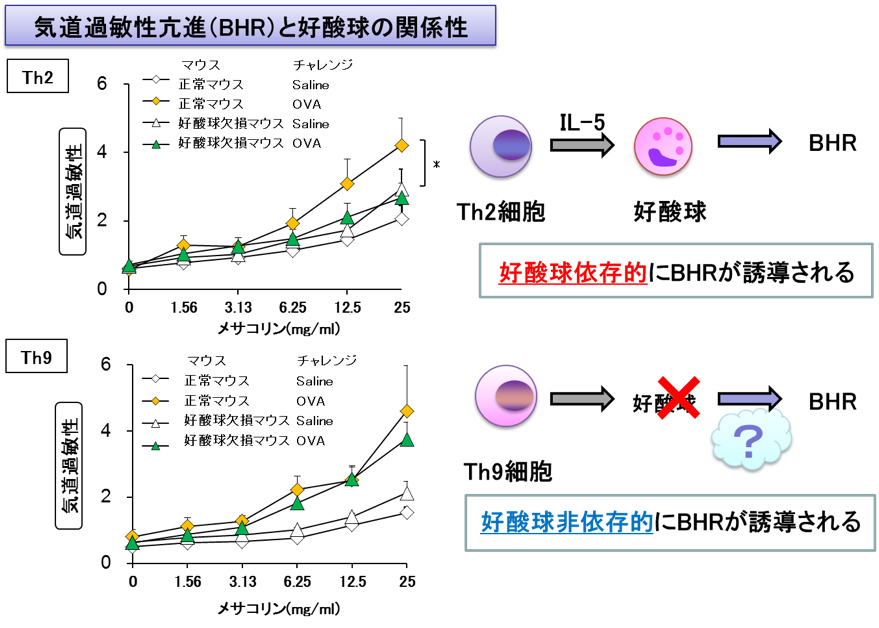
本研究では、Th2細胞とTh9細胞において、どちらも好酸球浸潤、気道過敏性亢進を誘導するものの、Th2細胞による気道過敏性亢進とは異なり、Th9細胞による気道過敏性亢進は好酸球非依存的であること、Th9細胞による気道過敏性亢進はステロイド抵抗性を示すことを見出した。これらの活性化機構の分子メカニズムの違いを明らかとすることで、新しい気管支喘息の治療法が開発できる可能性があることから、現在、気管支喘息過敏性亢進にかかわる特異的な分子の探索と機能解析に取り組んでいる。
Allergol Int. 66S:35-40 (2017)
Allergol Int. 65S:24-29 (2016)
(佐伯真弓)
3. ヘルパーT細胞のヒスタミン受容体を介したアレルギー性鼻炎の重症化機序の解明
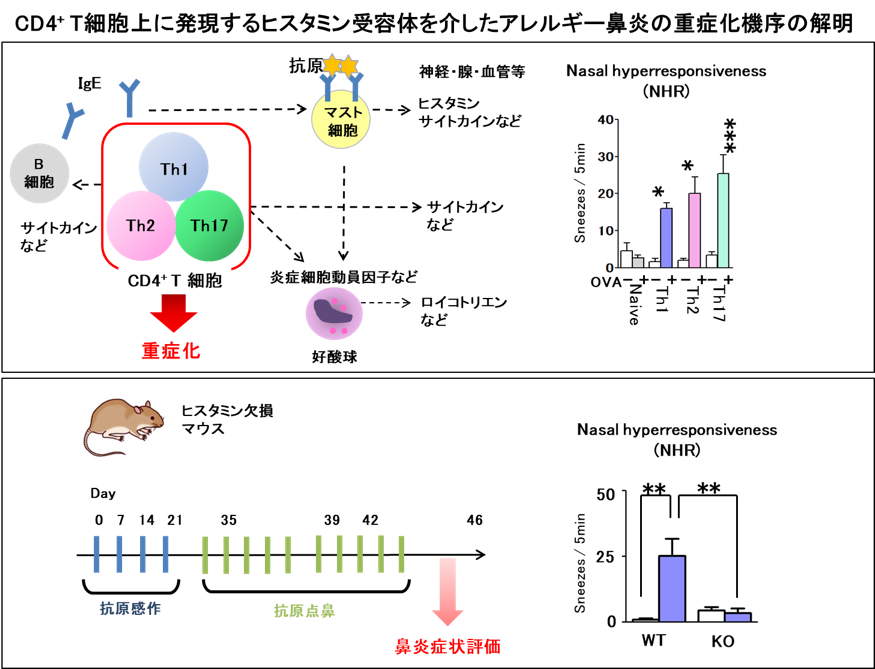
アレルギー鼻炎はスギ花粉などの特異的抗原の刺激などにより、くしゃみ・鼻水・鼻づまりなどの症状が誘発されるが、重症化したアレルギー性鼻炎患者では塵や気温差などの抗原以外の刺激にも強く反応する傾向がある。本研究では、鼻粘膜過敏症亢進(NHR)モデルマウスを用い、この重症化には抗原特異的T細胞が強く関与することを見出した(図上段)。また、その調節機序として、炎症部位に高濃度で存在するヒスタミンを介するものであることが明らかとなった(図下段)。今後、ヒスタミン受容体の発現メカニズム等を明らかとすることでCD4陽性T細胞の機能調節の一端を明らかとし、アレルギー医療に貢献することが期待される。
Allergol Int. (2018) In press.
PLoS One. 1(1):e0146686. (2016)
(西村友枝)
新規治療法の開発
1.T細胞におけるNFAT3欠損の生理学的意味と分子機構の解明
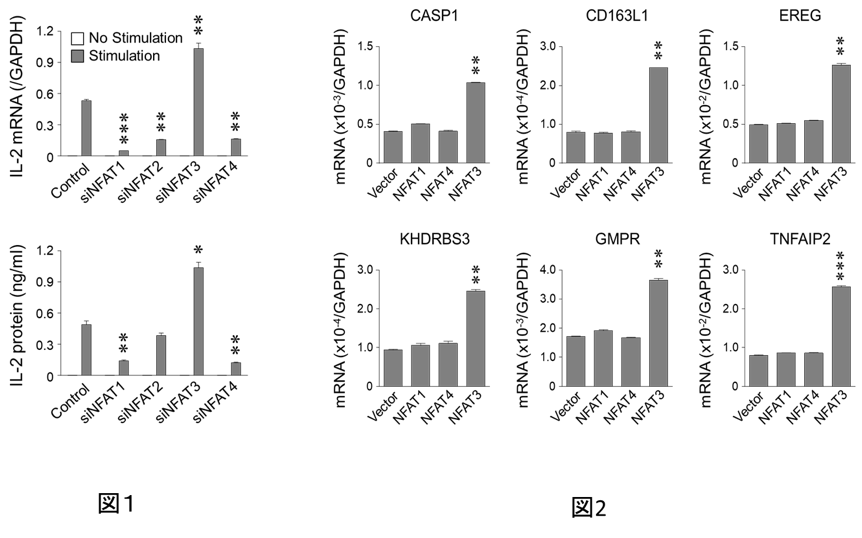
転写因子Nuclear factor of activated T cells (NFAT) の4つのisoform (NFAT1-4)はさまざまな遺伝子発現において一様に転写活性誘導に関与すると考えられてきた。しかしながら免疫細胞ではNFAT3が発現しておらず、その生理学的な意味を調べるなかで、我々はヒトT細胞のサイトカイン産生に対してNFAT3が他のNFAT isoformと相反した抑制的機能を有していることを見出した (図1)。さらにNFAT3欠損によってT細胞が高いサイトカイン産生能を発揮できる分子機構を明らかにした。また、NFAT3を高発現するヒト大動脈平滑筋細胞におけるNFAT3制御遺伝子群を同定し、他のNFATでの制御を調べた結果、NFAT3の相反的な役割はT細胞特異的に認められることが分かった(図2)。
J Immunol, 200(1):92-100 (2018)
(神沼修・北村紀子)
