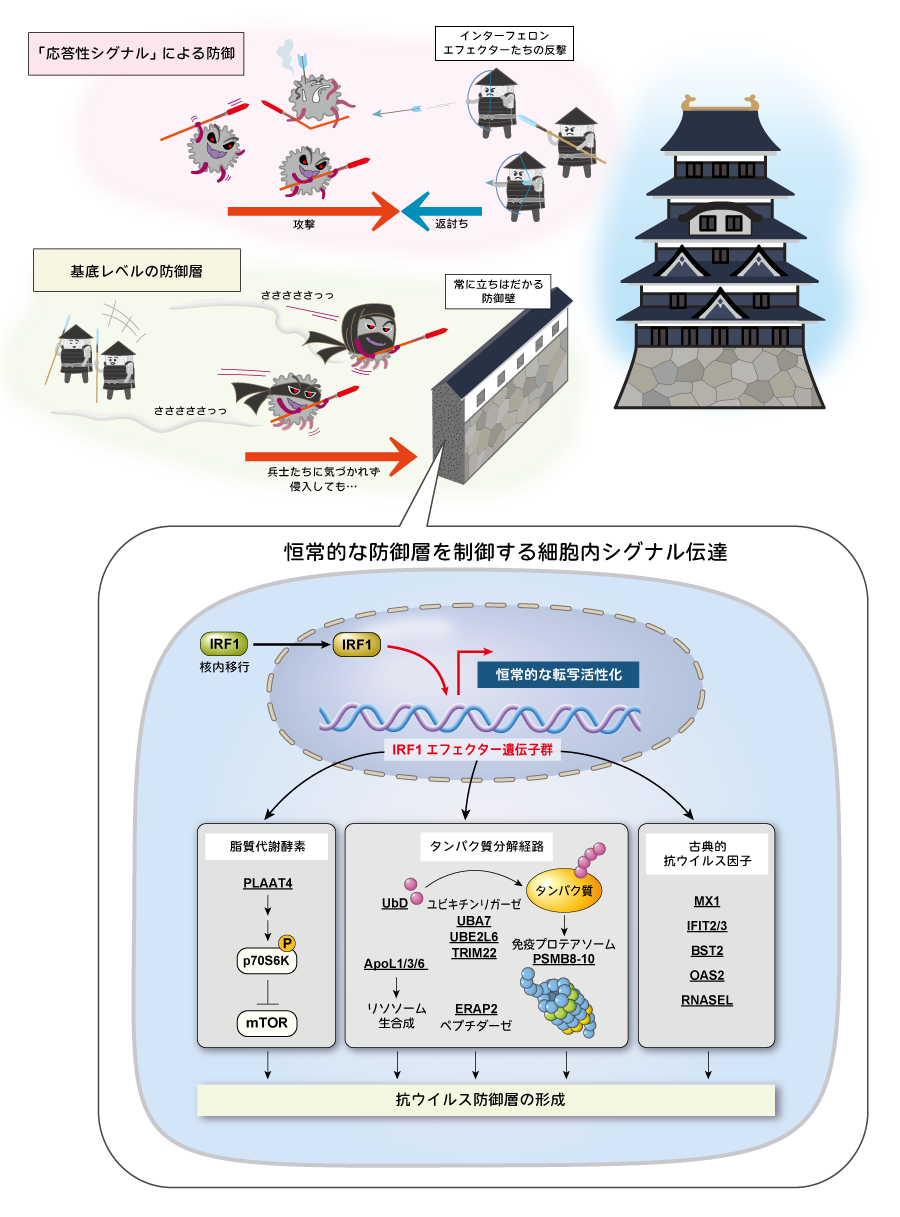
培養困難なウイルスの複製機構を規定する要素として、私たちの細胞に本来備わっているインターフェロンを中心とした自然免疫機構が存在します。
当研究室ではこれまでにウイルス感染が引き金となる「応答性シグナル」に加えて、恒常的に機能する「基底レベルの防御層」の存在を明らかにしてきました。
特定の病原体に対してはこの恒常的に機能する防御層が効果的にウイルス感染を抑制することがわかっています。私たちは、これまでほとんどその重要性が知られていなかった「基底レベルの防御層」を制御するしくみと、ウイルスを直接叩く「エフェクター」となる細胞因子の作用機序に着目した研究を展開しています。
これらの防御層が応答性シグナルと相互作用する仕組み、またそれが感染症の病態形成に与える影響を明らかにすることを目標としています。
これらののメカニズムの研究を通じて、
を目指します。



2019年4月15日
感染制御プロジェクトの山根大典 主席研究員らは「ウイルス感染を抑制する新たな肝細胞の自然免疫シグナルの仕組み」について英国科学雑誌「Nature Microbiology」に発表しました。
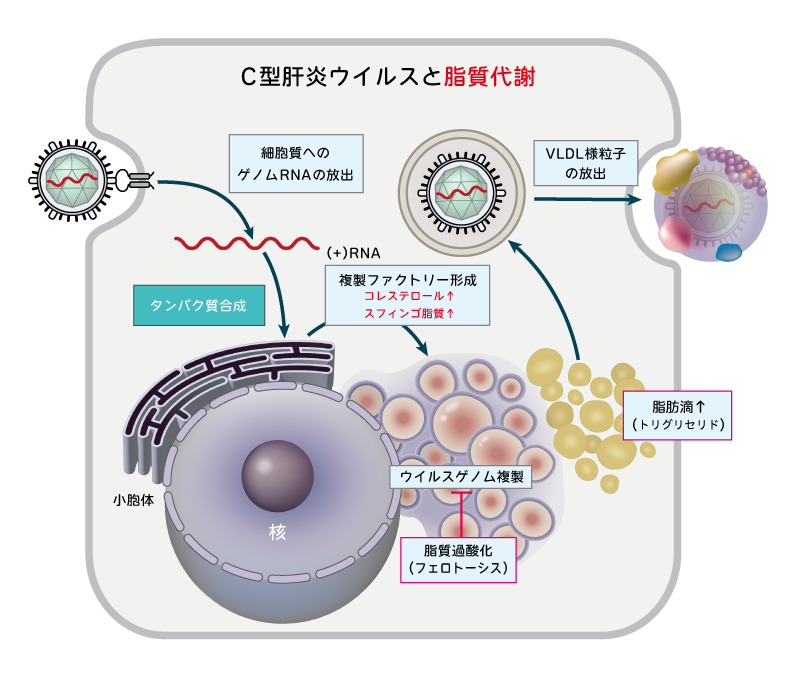
ウイルスは、侵入した細胞内で脂質合成を刺激し、脂質に富んだ環境を自ら構築することで効率よく増殖する戦略をとります。このようにウイルスによる細胞内代謝のハイジャックが宿主の脂質代謝異常の原因となると考えられていますが、その詳細な病原性発現機構については不明な点が多く残されています。
ウイルス感染に伴って起こる代謝変化は、現代社会において問題となっているメタボリックシンドロームが起こる仕組みと重なる可能性があります。そこで、私たちはウイルス感染病態の解明を切り口とした、独自の研究アプローチによって、細胞機能の異常に起因する疾患メカニズムの解明を目指します。
特に、ウイルス感染や脂肪酸代謝異常が脂肪肝を誘導する仕組みや、「フェロトーシス」と呼ばれる脂質過酸化を介したウイルス複製制御機構に着目し、これらの分子機構の理解に基づく創薬へつなげることを目指しています。
2021年9月13日
感染制御プロジェクトの山根大典主席研究員、小原道法特別客員研究員らの研究チームは「C型肝炎ウイルスを抑制する新たな脂質代謝の仕組みを発見」について米国科学誌「Cell Chemical Biology」に発表 
https://www.amed.go.jp/news/release_20210914.html
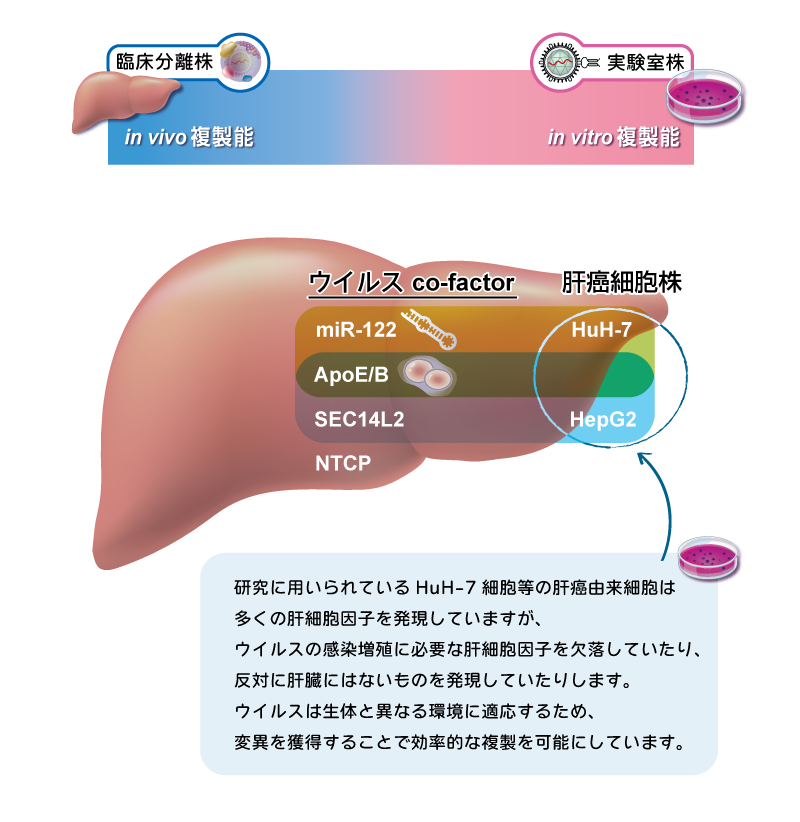
A型からE型に分類される肝炎ウイルスは、古くからその存在が知られており、肝障害や肝がんの原因となることが問題視されています。しかし、感染患者の血清から得られるウイルスを培養細胞に感染・増殖させることは技術的に困難であり、それが基礎研究や創薬の大きな障壁となってきました。 当研究グループは、C型肝炎ウイルスの多くの臨床分離株において、ビタミンEなどの脂溶性抗酸化物質が脂質過酸化を抑制することでウイルス複製を促進する仕組みを明らかにしました(Nature Medicine, 2014)。
また、肝臓と、実験に用いられている肝がん由来細胞とでは、細胞因子の発現プロファイルが大きく異なります。この違いに起因する代謝シグナル経路に着目することで、多くの肝細胞指向性ウイルスの感染・増殖が可能になると考えています。
現在私たちは、この違いを解明し肝臓環境を再現することで、
① 培養が困難な肝炎ウイルスの増殖を可能にする細胞培養システムの構築
② その分子機構を標的とした新たな創薬の展開
を目指して研究を進めています。