TOPICSへ
未来を話そう!
センターの研究紹介
感染症医学研究センター
感染制御ユニット
インフルエンザウイルス、B型肝炎ウイルス、そして、C型肝炎ウイルスによる感染症を研究し、予防法と治療法の開発を目指しています

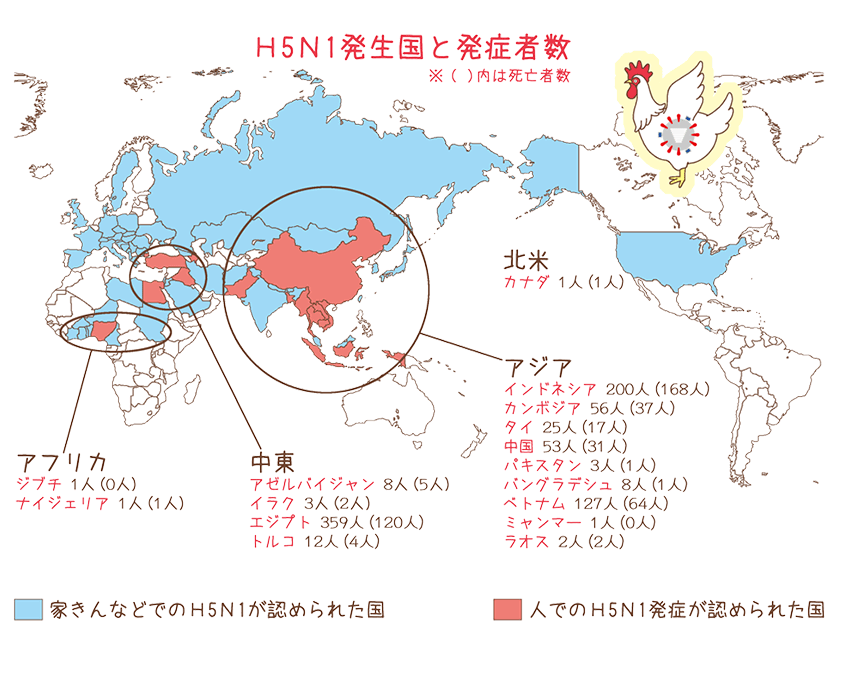
高病原性鳥インフルエンザは死亡率も高く、世界的な流行が心配されています。また、季節性インフルエンザでも毎年多くの人が亡くなっています。
一方、B型肝炎ウイルスには110~140万人、C型肝炎ウイルスには190~230万人の日本人が感染していると推定され、日本人の肝がん発症の7~8割の原因となっています。
私たちのプロジェクトでは急性感染症であるインフルエンザ、そして慢性感染症のウイルス性肝炎を研究し、予防法と治療法の開発を目指しています。
感染制御ユニット
安井 文彦 ユニットリーダーが解説します。
Fumihiko YASUI
Project Leader

感染制御ユニット
安井 文彦 ユニットリーダーが解説します。
Fumihiko YASUI
Project Leader
どんなことに役立つの?
万が一の流行に備えて、強い免疫誘導効果が期待されるH5N1型インフルエンザ向け予防ワクチンの実用化を目指しています。
また、感染後、時間が経過し、重症化した感染者にも効くインフルエンザ治療薬も実用化が期待されています。
C型肝炎ウイルスの治療ワクチンの開発研究も進んでいます。今後は、根治が難しいとされる慢性B型肝炎の治療ワクチンの開発も期待されています。肝硬変、肝がんの治療法についても研究を進めています。

ワクチン開発
より強い免疫力がつくワクチンの開発を目指して
—— インフルエンザウイルスの研究についてお聞かせください。
安井インフルエンザウイルスについては、高病原性鳥インフルエンザの一つ、H5N1型の予防ワクチンの研究を2009年から進めています。H5N1は感染すると重症化することが多く、死亡率も高いものです。通常の季節性インフルエンザと同じ方法で作ったワクチンでは、効果が弱かったため、より免疫誘導効果が高い全粒子不活化ワクチンが備蓄されています。それでもなお、十分な免疫力をつけるためには、複数回接種する必要があるといった問題があります。
2009年の豚由来のインフルエンザの大流行を見てもわかるように、人から人へ伝播が起こると、瞬く間に世界中に広がってしまいます。そこで、私たちは1回の接種で速やかに強い免疫を誘導できるワクチン開発を目指してきました。
また、治療薬の研究も進めています。現在の治療薬は感染後48時間以内に服用しないと効果がでませんが、現在の治療薬とは作用メカニズムの異なる、時間がたって重症化した患者さんでも治せるような新しい治療薬の開発を目標にしています。
—— C型肝炎ウイルスについてはどうでしょうか?
安井前プロジェクトリーダーの小原道法博士の下でC型肝炎研究が長年進められてきました。小原博士は、当時、診断法がなかったC型肝炎の診断薬の開発に携わってきました。
C型肝炎ウイルスの中で、遺伝子型Ib型ウイルスは治療が困難でしたが、近年、効果的な治療薬が開発され、患者さんの90%以上は治るようになりました。しかし、非常に高価で、手厚い健康保険制度がある日本のような国は別として、世界的には、本治療薬を利用できる人はそれほど多くありません。また、原因が定かではないため治療できない患者さんの問題もあります。そこで、私たちはC型肝炎ワクチンの開発に取り組んできました。以前から、B型・C型肝炎の患者さんが突然治癒する事例の臨床報告を受けており、C型肝炎ウイルスへの免疫を活性化するワクチンによってウイルスを排除できないかと考えたのです。予防ではなく、“治療のためのワクチン”です。また、ワクチンは安価に提供でき、多くの患者さんが利用できるという大きな利点もあります。
研究の進捗
強い免疫を誘導することで感染症を治す
—— インフルエンザワクチン開発の進捗はいかがですか?
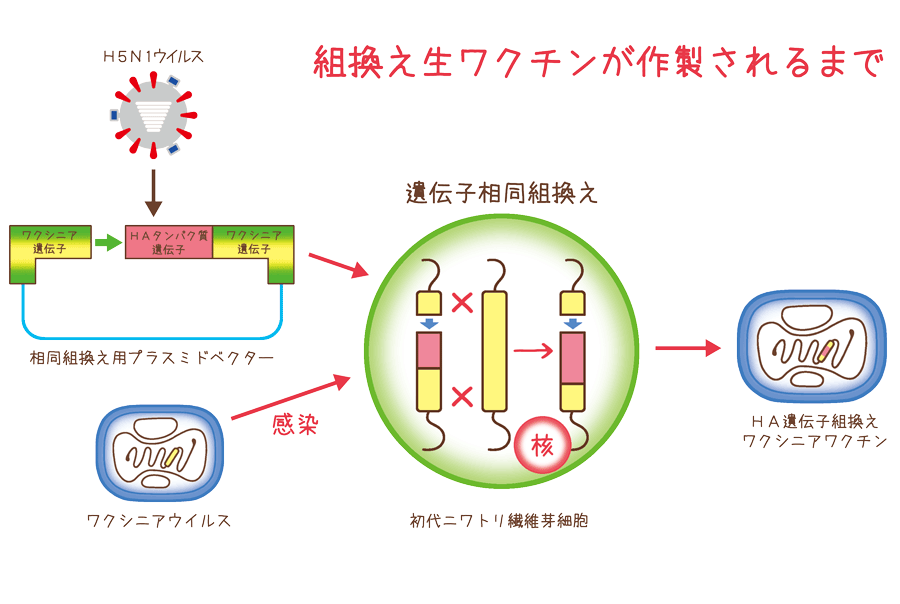
安井インフルエンザウイルスが、人や動物の細胞に感染する時にウイルス表面にあるHAタンパク質(ヘマグルチニン)が必要となることに注目し、HAタンパク質をターゲットとするワクチンの研究を進めてきました。高い安全性を持つ「ワクシニアウイルス」というワクチン株にH5N1インフルエンザウイルスのHAタンパク質の遺伝子を組み込んだ「組換え生ワクチン」を作ることにすでに成功しています。
H5N1亜型ウイルスは、非常に多くのウイルス株が存在し、複数のクレード* に分類されています。備蓄されているプレパンデミックワクチンは、クレードごとに作る必要があるのですが、検証の結果、「クレード2.2」のワクチンでH5N1ウイルスの多くのクレードに対応できることが明らかになりました。一種のワクチンで、H5N1のインフルエンザすべてを防御できることが期待されます。
*クレード
インフルエンザウイルスは、遺伝的に安定ではなく、血清亜型が変わることはないが、遺伝子が変化して、病原性や抗原性などが変化する。現在までに、H5N1亜型ウイルスは、数千の株が分離されており、僅かな抗原性の違いによっていくつかの種類(クレード)に分けられている。
—— 肝炎の治療ワクチンの研究はどの段階にあるのでしょうか?
安井C型肝炎ウイルスの治療ワクチンは、30年近く世界各国の学者が研究してきたのですが、なかなか成功しませんでした。
しかし、私たちは最近、C型肝炎ウイルスのウイルス粒子を作るタンパク質(構造タンパク質)とウイルス増殖のためのタンパク質(非構造タンパク質)をターゲットとした異なる種類のワクチンの接種方法や接種する順番を変えることによって、非常に強い免疫を誘導できることを発見しました。現在、C型肝炎ウイルス遺伝子をマウスのゲノムの中に組み込んだトランスジェニックマウス*を用いて、効果の検証を進めており、C型肝炎ウイルスのタンパク質を減少できることと症状を改善できることがわかってきました。
*トランスジェニックマウス
受精卵に人為的に外来遺伝子を導入し、マウスのゲノム内に外来遺伝子を組み込んだマウス。トランスジェニックマウスでは、組み込まれた遺伝子からできるタンパク質などの性質や機能を解析できる。私たちの研究では、通常、マウスが感染しないC型肝炎ウイルスの遺伝子をマウスのゲノム内に組み込むことで、C型肝炎を発症させ、ワクチンの効果を解析している。
—— 研究で苦労された点は?
安井アイディアを証明する段階で動物モデルが必要な点ですね。治療が難しい疾患は、得てして、研究を進めるうえで重要かつ最適な動物モデルが存在しないことが多いです。B型肝炎ウイルス、C型肝炎ウイルスは、宿主域が狭く、人とチンパンジーにしか効率良く感染しません。そこで、C型肝炎の研究では、先ほどお話ししたトランスジェニックマウスで治療効果を検証しています。人での使用を考えるうえでは、さらに、人に近い動物モデルの開発と治療効果、安全性を確認したいと思います。
未来への展望
重症化インフルエンザも、B型・C型肝炎も治る時代に
—— 今後の研究についてどのような展望をお持ちですか?
安井H5N1ワクチンは、製薬会社と一緒に人に使えるものを作りつつあるところです。次の段階は治験。数年で実用化の目途が立つようにし、万が一の事態に備えたいですね。
いずれは、中国で感染が広がりつつあるH7N9ウイルスへのワクチンや毎年流行する季節性インフルエンザについても、免疫誘導効果の高い新規ワクチンを開発していきたいです。
肝炎ウイルスの治療ワクチンも、実用化に向けて製薬会社と相談をしていこうというところです。B型肝炎ウイルスの治療ワクチンの開発も進めていきたいですね。また、肝硬変の治療薬の開発も良好な結果を得ることができてきましたので、さらに研究を発展させたいと思います。

感染後、時間がたっても効果を発揮する
インフルエンザ治療薬ができる?

現在、臨床で用いられている抗インフルエンザ治療薬は感染から48時間以内に服用しないと効果がなく、重症化した患者さんを治すことができません。
しかし、重症化したインフルエンザ患者に回復患者の血漿を投与したところ、劇的に回復したという報告もあります。詳細な作用メカニズムはわかりませんが、インフルエンザウイルスに対する抗体によって治癒するのではないかということです。
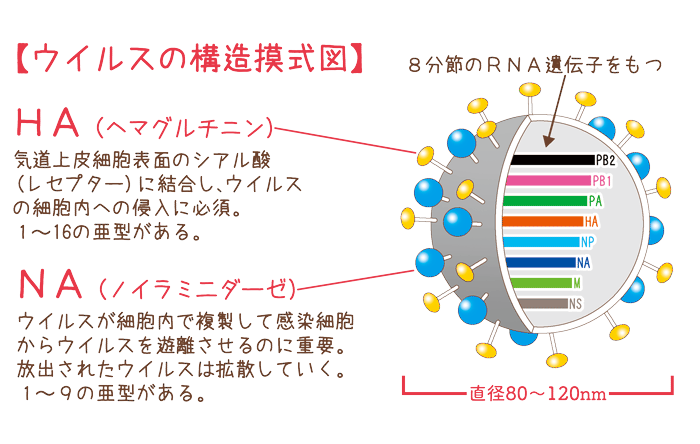
既存のインフルエンザ治療薬はインフルエンザウイルス内のノイラミニダーゼNAタンパクを標的にしていますが、私たちのプロジェクトでは細胞とくっつく働きがあり、細胞内でのウイルス増殖に大きな役割を果たすHAタンパク質をターゲットとした抗体医薬の開発を進めてきました。HAタンパク質による細胞への吸着阻害に加え、ウイルス侵入後における細胞膜への融合も阻害することが明らかになっています。すでに動物モデルでの治療効果も確認できています。
2021年5月11日
感染制御プロジェクトの小原道法特別客員研究員らは、インフルエンザウイルスHAを標的とした特殊環状ペプチドを開発し、その発症を阻害する仕組みに関して動物モデルを使って解明し、中分子ペプチドの新たな抗ウイルス薬としての可能性について発表しました。
インフルエンザウイルスHAを標的とした特殊環状ペプチドの発症阻害機序を解明
研究の背景
インフルエンザウイルス*1)*1)インフルエンザウイルス
インフルエンザは、インフルエンザウイルスを病原体とするとする感染症で、「一般のかぜ症候群」とは異なる。世界各地で毎年インフルエンザの流行がみられ、季節性インフルエンザの病原体のA/H1N1ウイルス、A/H3N2ウイルス、B型ウイルスは、冬季に感染・流行を繰り返す。推定患者数は、毎年1,500万人以上であり、公衆衛生上重大な問題となっている。は過去に4度世界的に大流行し、また、高病原性鳥インフルエンザウイルスH5N1や、世界的流行を起こしたPandemic 2009 H1N1(パンデミックインフルエンザA(H1N1) 2009)、さらに、毎年流行する季節性インフルエンザウイルスによる感染症は、健康及び世界経済に深刻な影響を与え続けています。現在、インフルエンザの治療で主に用いられているのは、リレンザやタミフルといったノイラミニダーゼ阻害薬(NA阻害薬)*2)*2)ノイラミニダーゼ阻害薬(NA阻害薬)
インフルエンザウイルスの表面には、ヘマグルチニン(HA)とノイラミニダーゼ(NA)の二種類のスパイクタンパクがあり、ウイルス感染に重要な役割を果たしている。HAは細胞に結合して感染に関与し、NAは、感染した細胞からウイルスを放出させる役割を持っている。現在、多く使われている抗インフルエンザ薬はNA阻害薬である。今回の研究ではウイルスの細胞への侵入に寄与しているHAの阻害薬の開発を進めた。ですが、既に耐性を獲得したウイルス株の出現が報告されています。そのため、既存の抗ウイルス薬とは作用の仕組みが異なる新たな治療薬の開発が求められています。
抗ウイルス薬に代わるものとして、インフルエンザに対する抗体医薬*3)*3) 抗体医薬
生体の防御のために働くタンパク質である抗体を利用した医薬品で、がん細胞等の疾患に関連する細胞の表面にある目印となる抗原を狙い撃ちにするため、高い治療効果と副作用の軽減が期待できる。の開発が世界中で進められていますが、抗体は分子量が非常に大きいため、抗体が認識できる部位はアクセス可能な領域、例えば、細胞表面や細胞外のものに制限されます。その一方で、ペプチド*4)*4) ペプチド
2個以上のアミノ酸がペプチド結合したもので、神経伝達作用や抗菌作用等を示す物もある。は、抗体よりもはるかに分子量が小さいため、抗体では入り込むことのできないウイルス蛋白上の狭い領域にも入り込むことができます。しかしながら、特異性に乏しく、つまり、標的となる分子に結合する力が弱く、安定性にも問題がありました。こうしたことから、我々は次世代の抗体医薬として、抗体が結合することのできない抗原領域を認識することが可能な特殊環状ペプチド*5)*5) 特殊環状ペプチド
現在、使用されている薬剤は、主に低分子医薬品と抗体医薬品で、古典的ペプチド医薬品は、欠点が多く、インスリン等の限られた薬剤しかない。しかし、特殊環状ペプチドは、抗体並みの活性や基質特異性を獲得することが可能で、古典的ペプチドの弱点の血中安定性が大幅に改善する。に着目しました。東京大学の菅教授及びペプチドリーム社との共同研究により、約12-15個のアミノ酸から構成され、メチル化及び環状化により、高病原性H5N1 HA蛋白に特異的に結合する特殊環状ペプチドをスクリーニングし、生体内における安定性が、従来よりも向上した特殊環状ペプチドを見つけ出しました。
研究の概要
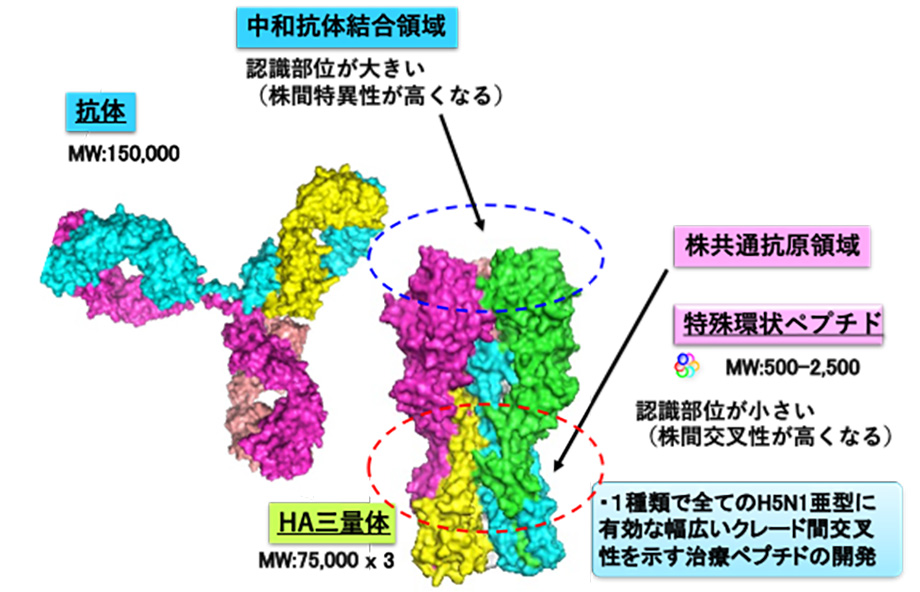
毎年大きな流行を繰り返すインフルエンザは世界的に重大な感染症の一つです。次世代の抗ウイルス薬には、宿主には影響せず、ウイルスに特化した効果が求められます。このうち、第3世代の抗体医薬として特殊環状ペプチドが注目されています。抗体は分子量が大きく、多くはHA蛋白質のグロブラーヘッド領域へ結合し、インフルエンザウイルス株間の特異性が強くなります。特殊環状ペプチドは、分子量が500-2,500と小さく、HA蛋白質のストーク領域へ結合し、交差反応性が高くなることが期待できます。現行のインフルエンザ治療薬のNA阻害薬は、ウイルス因子を標的とした薬剤であり、感染細胞からインフルエンザウイルスが出芽するのを阻害するという作用の特性上、ウイルスが増殖した感染中期以降における阻害効果が著しく弱まることや、遺伝子変異した薬剤耐性ウイルスが出現することが問題点として挙げられます。
H5N1高病原性鳥インフルエンザウイルス感染症の重症患者に対して、回復患者に由来する血漿の投与が、感染中期以降においても治療効果を示したとの報告を基に、我々はインフルエンザウイルスのヘマグルチニン蛋白質を標的とした特殊環状ペプチドの探索を行い、リレンザと同等以上の阻害活性を有する特殊環状ペプチドiHA-100を見い出しました。このiHA-100は、インフルエンザウイルスのH5N1/H1N1/H2N2の3つの亜型に対して防御効果を発揮し、さらに、リレンザに耐性のあるH1N1パンデミック2009に対しても強力な阻害活性を示すことを見い出しました。
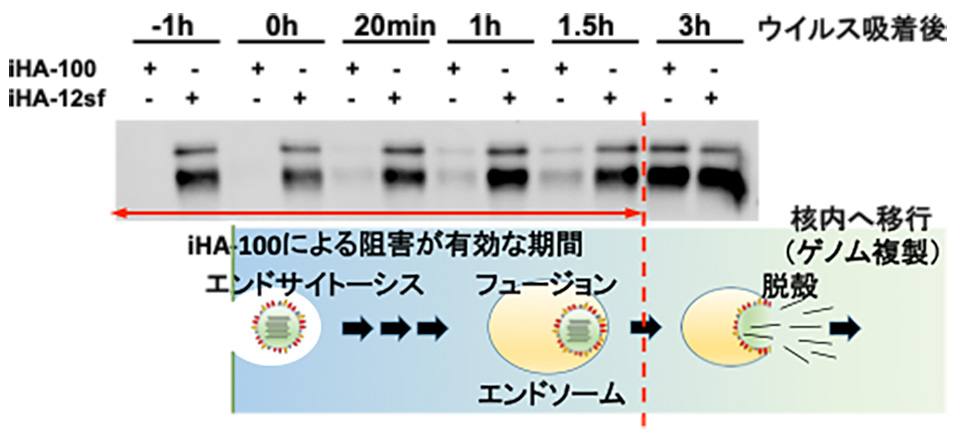
このiHA-100がインフルエンザウイルスの増殖を抑制するメカニズムを明らかにするため、ウイルス感染のどの段階を阻害しているのかについて解析しました。異なるタイミングでiHA-100を培養上清に添加する実験を行ったところ、ウイルス吸着前及び直後の添加により、完全にウイルス感染を阻止することが判明しました。さらに、細胞内に侵入後、エンドソーム膜と融合を開始する感染吸着後90分の段階で添加した場合においても強い抑制効果がみられました。iHA-100の作用の仕組みとして、細胞外に存在するウイルス粒子の感染性を中和するだけでなく、細胞内においてもHAと相互作用し、侵入過程の複数の段階を阻害するといった新たな阻害の仕組みが明らかとなりました。
また、マウスを用いた実験で、感染初期にしか効果の無いリレンザとは異なり、感染後期においても劇症肺炎を抑制する治療効果があることも示されました。この治療効果は、霊長類モデルであるカニクイザルでも同様でした。
研究の意義と今後の展望
今回、H5N1 高病原性鳥インフルエンザウイルスのHA蛋白質に結合する特殊環状ペプチドのうち、リレンザと同等以上の阻害活性を示すiHA-100を見出しました。iHA-100はウイルス粒子の感染性を中和するだけでなく、細胞内においてもHAと相互作用し、侵入過程の複数の段階を阻害するといった新たな阻害の仕組みが明らかとなりました。また、感染4日後及び6日後からの投与においても治療効果を示すことも明らかとなっており、リレンザにはない治療効果を示していることから、新たな抗インフルエンザ薬となる可能性があると考えられます。
用語説明
- *1) インフルエンザウイルス
- インフルエンザは、インフルエンザウイルスを病原体とするとする感染症で、「一般のかぜ症候群」とは異なる。世界各地で毎年インフルエンザの流行がみられ、季節性インフルエンザの病原体のA/H1N1ウイルス、A/H3N2ウイルス、B型ウイルスは、冬季に感染・流行を繰り返す。推定患者数は、毎年1,500万人以上であり、公衆衛生上重大な問題となっている。
- *2) NA阻害薬とHA阻害剤
- インフルエンザウイルスの表面には、ヘマグルチニン(HA)とノイラミニダーゼ(NA)の二種類のスパイクタンパクがあり、ウイルス感染に重要な役割を果たしている。HAは細胞に結合して感染に関与し、NAは、感染した細胞からウイルスを放出させる役割を持っている。現在、多く使われている抗インフルエンザ薬はNA阻害薬である。今回の研究ではウイルスの細胞への侵入に寄与しているHAの阻害薬の開発を進めた。
- *3) 抗体医薬
- 生体の防御のために働くタンパク質である抗体を利用した医薬品で、がん細胞等の疾患に関連する細胞の表面にある目印となる抗原を狙い撃ちにするため、高い治療効果と副作用の軽減が期待できる。
- *4) ペプチド
- 2個以上のアミノ酸がペプチド結合したもので、神経伝達作用や抗菌作用等を示す物もある。
- *5) 特殊環状ペプチド
- 現在、使用されている薬剤は、主に低分子医薬品と抗体医薬品で、古典的ペプチド医薬品は、欠点が多く、インスリン等の限られた薬剤しかない。しかし、特殊環状ペプチドは、抗体並みの活性や基質特異性を獲得することが可能で、古典的ペプチドの弱点の血中安定性が大幅に改善する。