未来を話そう!プロジェクト研究の紹介
がん免疫プロジェクト

免疫細胞のT細胞と、その表面に存在するTCR(T細胞受容体)の働きを解明して、がん治療を効果的に行うための研究をしています
免疫細胞のT細胞と、その表面に存在するTCR(T細胞受容体)の働きを解明して、がん治療を効果的に行うための研究をしています
丹野 秀崇 プロジェクトリーダーが解説します。
Hidetaka TANNO
Project Leader

がん免疫プロジェクト
丹野 秀崇 プロジェクトリーダーが解説します。
Hidetaka TANNO
Project Leader
どんなことに役立つの?
T細胞表面で働くTCRの“病気の原因となる細胞を見つけ出す”役割を活用して、1人1人の患者さんに応じた効果的な遺伝子治療法を確立します。まずは、がんを認識するTCRの構造を解析することからスタート。がんを認識できるTCRを利用することにより、手術が難しかったり、転移があったりする難治性がんへの新たな治療法を開発します。将来的には睡眠障害や感染症などの原因解明や治療にも研究を展開し、創薬の開発も視野に入れています。

メカニズム
T細胞とTCRが新しいがん治療法を作る
—— 病気から体を守ったり、回復させたりする免疫細胞とはどういったものですか?
人間にはがん細胞を退治したり、体に侵入した細菌やウイルスを撃退したりして病気から体を守る免疫細胞が備わっています。T細胞は免疫細胞の1つで、T細胞表面に存在するTCRを介して体の中に病気を引き起こすがん細胞やウイルス感染細胞といった異物があることを見つけ出します。
厳密に言えば、TCRが感知するのはがん細胞自体ではなく、HLA*と呼ばれるものに結合したタンパク質*の細かい断片です。HLAは細胞内に存在するタンパク質断片を細胞表面に提示する機能を持っています。正常な細胞ではHLAの上に正常なタンパク質断片が乗っているのですが、がん細胞では遺伝子が変異して生じた異常タンパク質断片(がん抗原*)が乗っています。T細胞はTCRを介してタンパク質断片-HLAの複合体を常に監視しており、タンパク質断片が異常なものと判断すると、それを提示しているがん細胞の排除に動き出します。
- *HLA:
- 人間の体のほぼ全ての細胞に存在し、細胞の状態をT細胞に知らせる役割を持つ。
- *タンパク質:
- 人間にはおよそ2万種類のタンパク質が存在している。あるタンパク質は光を感じたり、別のタンパク質は食物を分解したりするなどそれぞれが固有の機能を持つ。多種多様なタンパク質が協調的に働くことで生命活動は支えられている。
- *抗原:
- 免疫反応を引き起こす、本来体内に存在しない異物。がん細胞由来の変異タンパク質やウイルスを構成するタンパク質が挙げられる。
—— TCRは、T細胞に抗原の存在を知らせるいわば監視カメラの働きを担っているのですね。
加齢や生活環境の影響を受け遺伝子*が傷つくと、それによって生じた異常タンパク質が細胞を過度に増殖させ、がんとなります。
TCRはまさに監視カメラとして、こういった異常事態を見つけ出しT細胞に制御するように伝えるのです。
- *遺伝子:
- タンパク質を形作るための設計図。その本体となる物質がDNAで、A(アデニン)、T(チミン)、G(グアニン)、C(シトシン)の4つの塩基の配列からなる。
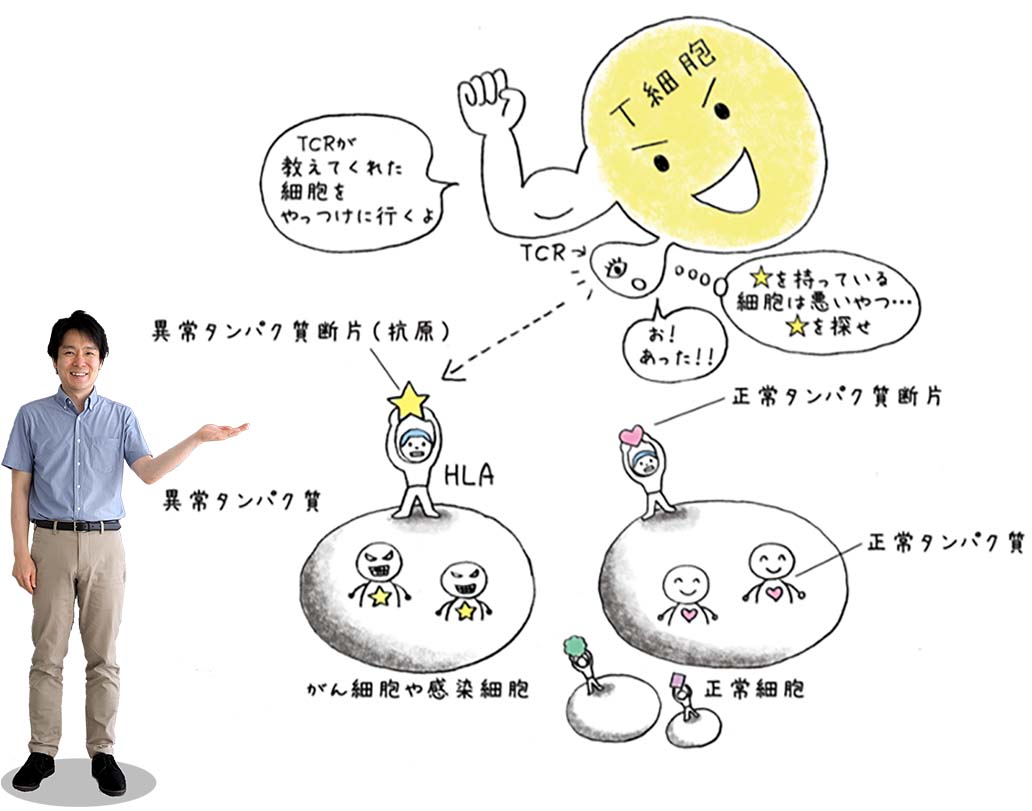
T細胞は正常なタンパク質断片がHLAに乗っている場合は何もしないが、異常タンパク質断片がHLAに乗っている場合はそれを提示している病原細胞の退治に乗り出す。
病気との関係
高速TCR解析技術適用で、一挙に数100倍の解析を可能に
—— TCRのがん細胞を見つけ出す機能を活用して、新たな治療法をどのように開発するのですか?
私たちは、患者さんの血液中からがん細胞を殺傷するTCRを探し出し、それを患者さんのT細胞で増幅させ、患者さんの体内に戻す遺伝子治療法を確立していきます。
欧米では、すでにメラノーマ(悪性黒色腫)と多発性骨髄腫ではこの方法で高い治療効果が実証されています。
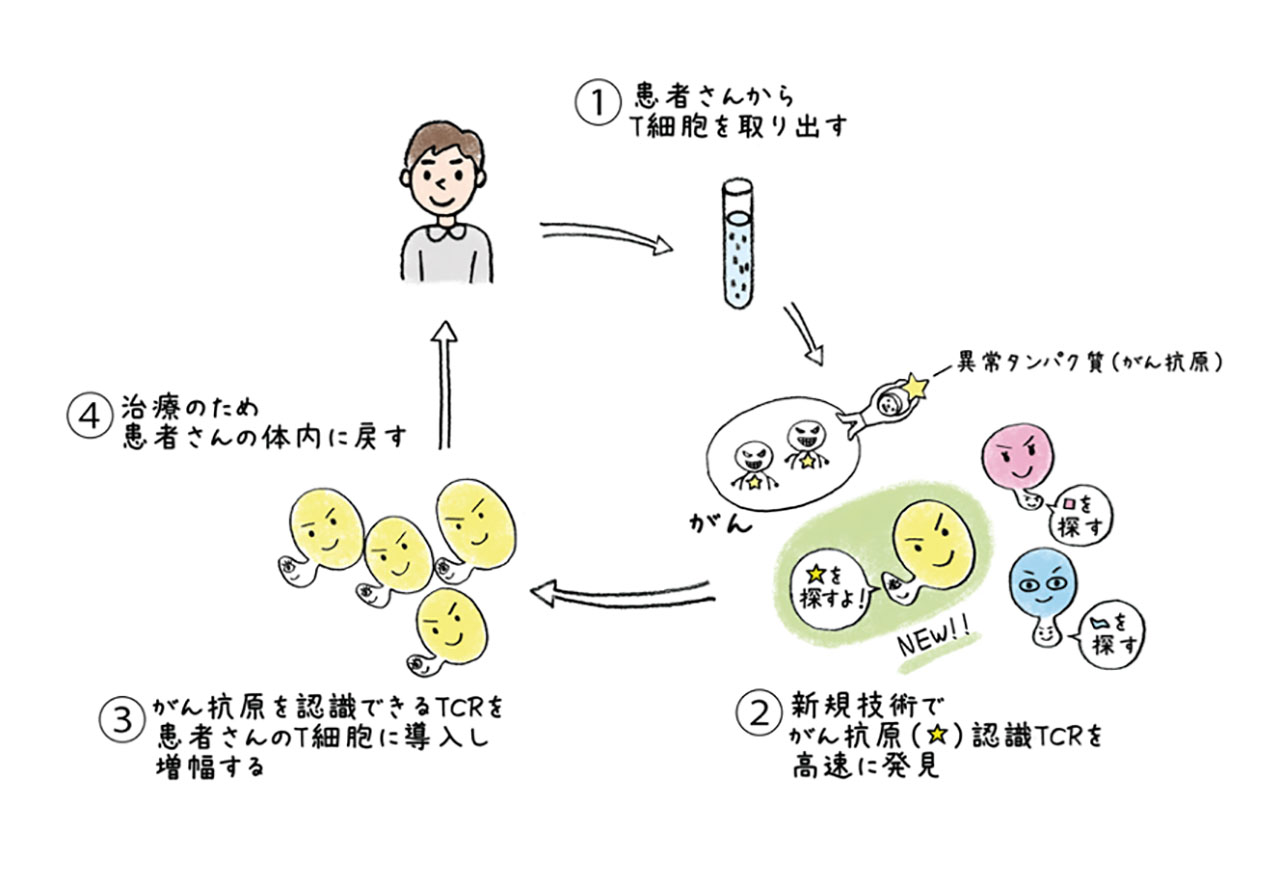
体の中からがん細胞を殺傷するTCRを見つけて増幅し、患者さんの体内に戻す
T細胞は1つ1つが異なるTCRを持っており、それぞれその認識抗原が異なる。多種多様なTCRの中からがん抗原を認識できるTCRを発見することはこれまで困難であった。そこで、新規技術を活用し、がん抗原を認識できるTCRを高速に発見することを試みる。発見されたがん認識TCRを患者さんのT細胞に導入、増幅後、体内に戻すことで、高いがん治療効果が期待される。—— 新たな治療法開発「がん免疫プロジェクト」の道筋をつけた新技術とはどんなものですか?
TCRをがん治療に活用するには、まずがんを認識するTCRを体内から見つけ出す必要があります。しかし、がん認識TCRを発見することは未だに困難です。我々の体内にはTCRが1億種類以上存在し、それぞれ認識する抗原が異なります。これまでの技術だと1回の実験で解析できるTCRの数は、せいぜい100種類止まりでした。この程度の数だと、膨大な種類のTCRの中からがん細胞を認識できるTCRを見つけ出すのはかなり難しいのです。
そこで私たちは、油で区切られた水の中に細胞を閉じ込めるエマルジョンという手法を用いることで、TCR配列を高速に解析する技術開発を成し遂げました。これにより、1回の実験でこれまでの数10~100倍にあたる数1000~数万種類のTCRを一度に解析することが可能になったのです。
未来への展望
TCR解析によりさまざまな病気の治療法を見つける
—— 高速でTCRの配列を解析する技術を今後どのように治療に結び付けるのですか?
TCRの配列を決定するだけでなく、それらのTCRが一体何の抗原を認識するかを一斉に把握できる方法を築き上げます。患者さんの血中からがん殺傷効果の高いTCRを迅速に見つけ出せるようになれば、がん治療が飛躍的に進歩するはずです。
そのためにがんの専門病院と共同で、患者数が非常に少なく革新的な治療法開発が難しい滑膜肉腫、脂肪肉腫の患者さんの血液を用いて、がん細胞を認識するTCRの構造と殺傷効果を調べていきます。この研究で治療法が確立されたら、その後は大腸がんや胃がんなどの治療の研究へと広げていきたいと考えています。
—— TCRを研究することによる画期的な治療法の開発は、がん以外でも可能なのでしょうか。
ここまでTCRの有用性についてお話ししてきましたが、昼間に突然強い眠気に襲われるナルコレプシー*では、TCRが悪さをしているのではないかと疑われています。
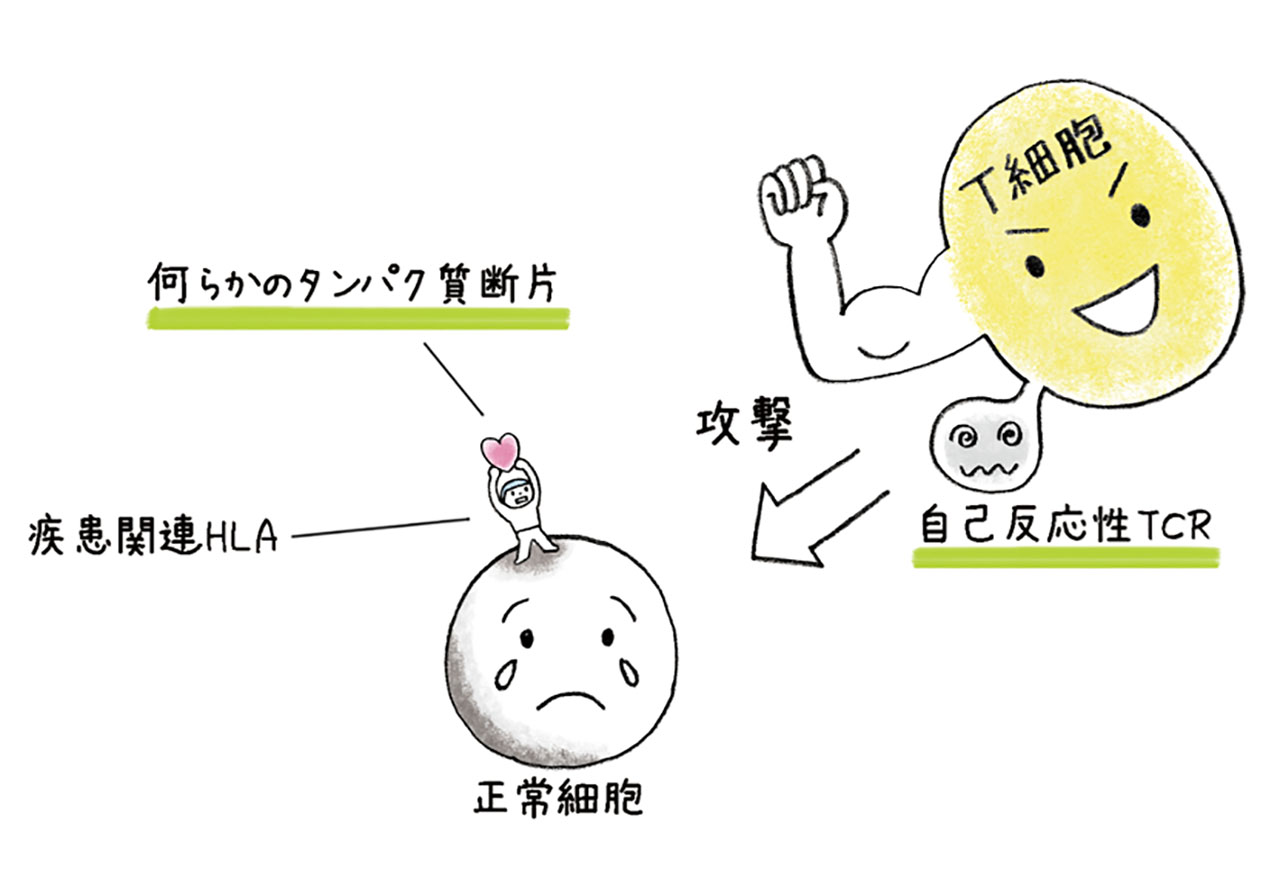
免疫細胞は本来、体にとって有害な物質を攻撃するのですが、この病気は正常な細胞をT細胞が攻撃してしまう自己免疫疾患*の可能性があります。ナルコレプシーの患者さんは特定のHLA遺伝子型を持つことが知られており、何らかのタンパク質断片-HLA複合体を正常な細胞が提示しています。これをTCRが誤って認識しているのではないかと考えられていますが、このTCRとタンパク質断片-HLA複合体の関係は完全には明らかとなっていません。当研究所の睡眠プロジェクトの本多真先生との共同研究でナルコレプシーを引き起こすTCRやその標的タンパク質断片を見つけ、その特性を調べていきます。研究をもとに、ナルコレプシーに対する分子標的薬*ができれば、患者さんにとって福音になるはずです。
TCRの構造や働きはまだまだ謎が多いのですが、解明が進めばがん以外のさまざまな病気の新たな治療法開発に結び付くはずです。

- *ナルコレプシー:
- 過眠症とも呼ばれ、場所や状況に関係なく、昼間、強い眠気に襲われ突然眠り込んでしまう病気。
- *自己免疫疾患:
- 人間の体に備わるウイルスや細菌などを排除する免疫細胞が異常をきたし、正常な細胞を攻撃することによって発症する病気。多くの場合、T細胞の異常が関係しているが、詳しい原因は明らかになっていない。
- *分子標的薬:
- 病気の原因となっている分子だけに働きかけるよう設計された治療薬。従来の治療薬より副作用が少ない。

遺伝子治療が注目されている理由の1つとして、患者さん1人1人に適した治療法をデザインしやすいという点が挙げられます。最新のがん治療は、同じ病気の患者さんに同一の治療を行うのではなく、患者さんの体質や病気に関連する遺伝子を調べて1人1人に合った治療をする方向へと向かっています。というのも、がん細胞の遺伝子やタンパク質などの研究が進み、同じ病名をもつ病気でも遺伝子レベルで細かく見ていくといくつかのタイプに分かれ、症状や治療法に個人差が出ることがはっきりしてきたのです。そこで、患者さん個々の遺伝子を調べて、その人の遺伝子に働きかけるオーダーメードの遺伝子治療への注目が高まっています。ただ、患者さんの遺伝子を調べるのは非常に手間がかかり、データをもとに治療を施すとなると高価になるという懸念も生じています。
高速TCR解析技術を活用することで、患者さんのがん細胞を見つけ出すTCRを今より安価に、素早く解析できれば、個々の患者さんに適したTCRを活用できるようになり、オーダーメード遺伝子治療に大きな弾みがつくでしょう。