
Tomita Y, Toriumi K, Miyashita M, Suzuki K, Kawaji H, Itokawa M, Arai M. Distinct microRNA profiles in neuron-derived extracellular vesicles between recent-onset and chronic-phase schizophrenia. Schizophrenia (2025) in press.
doi: 10.1038/s41537-025-00706-x
統合失調症は思春期から成人初期にかけて発症することが多く、この時期は脳の成熟が著しく進む神経発達上の重要な時期です。そのため、発症期に脳内でどのような分子変化が起きているのかを理解することは、病態解明にとって非常に重要です。しかし、死後脳を用いた従来の研究では、この発症初期の分子動態を直接調べることが難しいという課題があります。
microRNA(miRNA)は神経発生やシナプス形成に重要な役割を果たし、統合失調症との関連も指摘されていますが、発症早期の miRNA の変化については十分に研究が進んでいません。近年、血液から取得できる 神経細胞由来細胞外小胞(NEVs) が、非侵襲的に脳由来の分子情報を得る手段として注目されています。NEVs には miRNA が含まれており、そのプロファイルは脳の状態を反映すると考えられています。
そこで、本研究では、発症早期(5年以内)と慢性期の統合失調症患者から NEVs を抽出し、miRNA プロファイルを比較することで、発症期特異的な分子変化や病態進行のメカニズムを明らかにすることを目的としました。
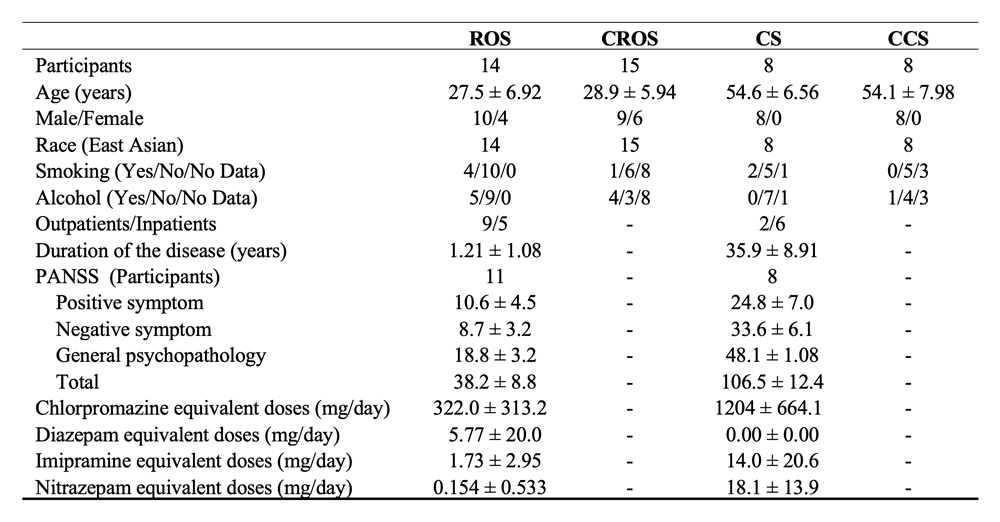
本研究では、発症後5年以内の統合失調症患者14名(ROS群)、年齢・性別を一致させた対照群15名(CROS群)、発症後15年以上経過した統合失調症患者8名(CS群)、および年齢・性別を一致させた対照群8名(CCS群)の末梢血からNEVを濃縮し、全参加者にmiRNAシーケンスを実施しました。。一方、性別、HbA1c、eGFR、家族歴、教育歴、発症年齢、抗精神病薬の服薬量(Chlorpromazine換算, CP換算)については有意差はみられませんでした。
ROS群とCROS群間で、FDR閾値<5%かつ倍比変化>2または<0.5を満たす17個のmiRNAが発現量差を示しました(図1)。このうち10個のmiRNA(hsa-miR-122-5p、hsa-miR-511-5p、hsa-miR-483-5p、hsa-miR-192-5p、hsa-miR-99a-5p、hsa-miR-342-5p、 hsa-miR-193a-5p、hsa-miR-200a-3p、hsa-miR-342-3p、hsa-miR-375-3p)は発現が上昇し、7つ(hsa-miR-100-5p、hsa-miR-423-3p、 hsa-miR-361-5p、hsa-miR-143-3p、miR-3184-5p、hsa-miR-584-5p、およびhsa-miR-184)は発現が低下していました。
一方、CS群とCCS群の比較では、2つのmiRNA(hsa-miR-184およびhsa-let-7c-5p)のみが有意に発現低下を示しました。特にhsa-miR-184は、ROS群およびCS群の双方において、それぞれの対照群と比較して一貫して発現が低下していました。
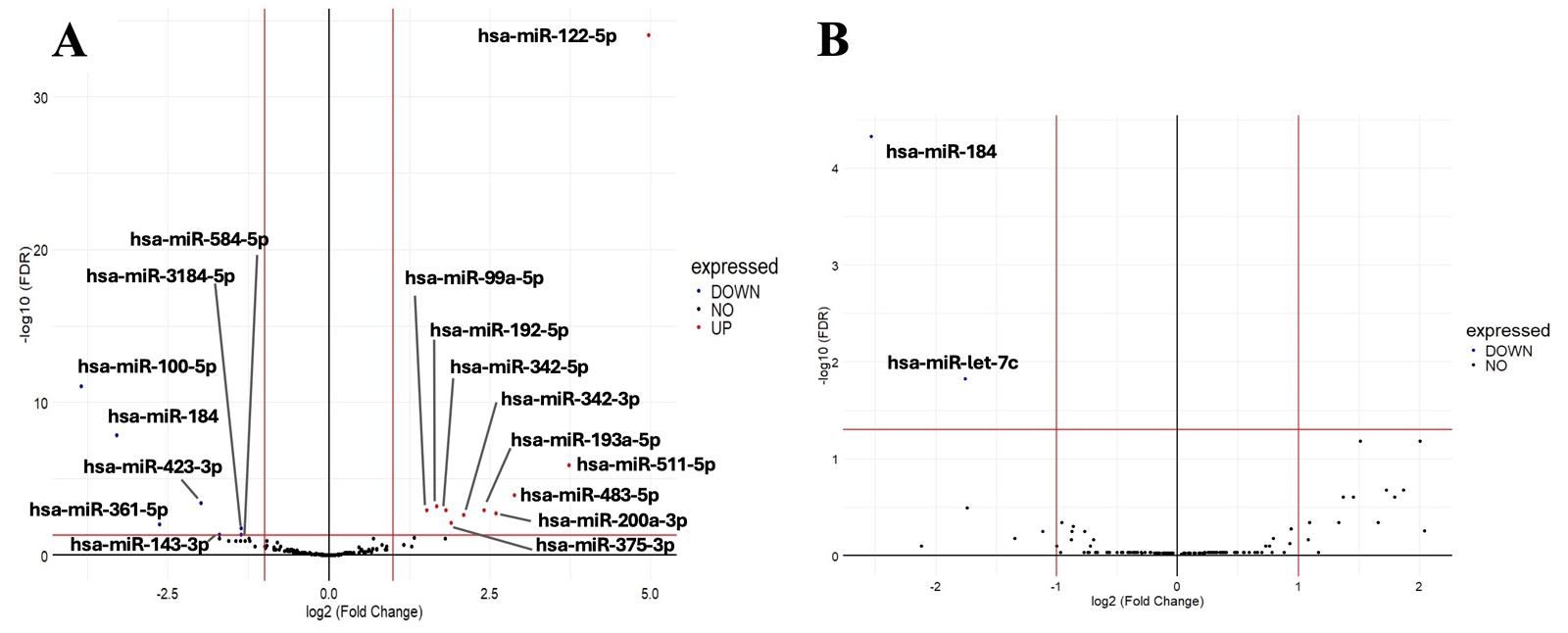
(A) ROS(n = 14)のNEVsでは、年齢および性別を一致させたCROS(n = 15)と比較して有意な発現差が認められました。(B) CS(n = 8)のNEVにおいて、年齢・性別を一致させたCCS(n = 8)と比較して有意な発現差が認められました。各miRNAの倍増率は補正P値に対してプロットされています。青丸はFDR<0.05かつlog2FC<−1.0を満たすmiRNAを示します。赤線は有意差の閾値(FDR<0.05かつ|log2FC|>1.0)を示します。
次に、ROSのバイオマーカーとしてのmiRNAの可能性を評価しました。差異発現miRNA 17種のうち、薬剤投与量との関連性から2種を除外した15種のmiRNAについて、単変量ロジスティック回帰分析を実施し、AUCを評価しました(表1)。その結果、hsa-miR-143-3pが最も高いAUCスコア(0.933、95% CI = 0.803-1.00)およびオッズ比(0.222、95% CI = 0.0645-0.475)を示しました。hsa-miR-143-3pの感度、特異度、正確度はそれぞれ100 ± 0.00%、93.3 ± 3.33%、96.6 ± 1.72%でした。
NEVsは細胞間コミュニケーションを介して、発生源となるニューロンおよび標的細胞における遺伝子発現に影響を与える可能性があります。miRNAの機能的役割を調査するため、グルタミン酸作動性ニューロン、GABA作動性ニューロン、およびアストロサイトにおいて発現する標的遺伝子を同定した。 Gene Ontology分析により、ROS 群で発現が変化した miRNA の標的遺伝子は、ニューロン投射の発達およびエンドソーム輸送に関連していることが明らかになりました。一方、CS群で発現が変化したmiRNAは、小胞体-核シグナル伝達経路およびシナプス後膜神経伝達物質受容体レベルの調節に関連していました。これらの知見は、統合失調症の発症期と慢性期においてmiRNAが異なる機能的影響を及ぼすことを示唆しています。
本研究は、統合失調症の発症直後におけるmiRNA発現をNEV(神経細胞由来細胞外小胞)を用いて解析した初めての研究であり、発症初期と慢性期で異なるmiRNAの病態メカニズムを示した点に大きな意義があります。これにより、統合失調症の神経発達的な異常が発症に深く関与することを改めて明らかにしました。
さらに、NEVを低侵襲な「脳の窓口」として利用できる可能性を示し、特に発症初期に変動したmiRNAが 早期診断のバイオマーカー候補となることを明らかにしています。これらの成果は、統合失調症の病態理解を進めるだけでなく、今後の治療・予防につながる研究の基盤を築くものです。