新型コロナウイルスや医学・生命科学全般に関する最新情報


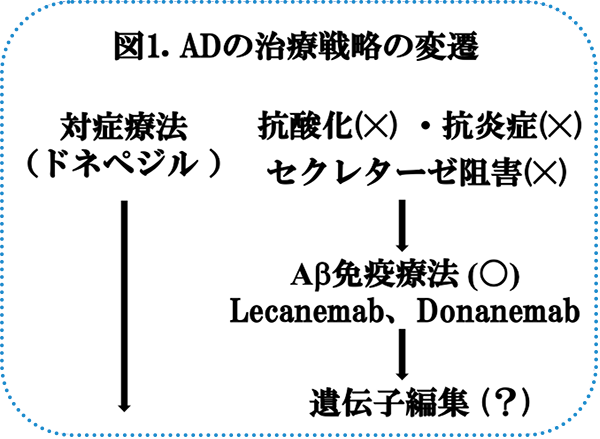
アルツハイマー病(AD)の病態においては、アミロイドβ(Aβ)ペプチドの凝集・蓄積による神経変性の促進が中心的な役割を担うとされています。従って、Aβを標的にした治療法が追求されてきました。最近、報告致しましたように(早期アルツハイマー病に対するLecanemab(レカネマブ)の治療効果〈2023/5/10掲載〉)、エーザイ/バイオゲンが開発したLecanemab(レカネマブ)による免疫療法が、早期ADの第III相臨床試験において認知機能の低下を有意に遅延することが示され、米食品医薬品局(FDA)から迅速承認されました(図1)。注目すべきことに、それに続いて、イーライリリー・アンド・カンパニー(米国)が開発したDonanemab(ドナネマブ)が、早期ADの第III相試験に成功し(図1)、FDAへ承認申請することになりました。このようなAβ免疫療法の治験が急展開した原因は必ずしも明らかではありませんが、モノクローナル抗体作成時に凝集しやすいタイプのAβを抗原に使ったこと、あるいは、早期ADを対象にして治療効果を評価したことなどが考えられています。現時点では副作用もわずかであり、今後、ADの根本治療が実現するのもそう遠くないと期待されます。ドナネマブの治験の成功が論文として発表されるまでしばらく時間を要しますから、今回は、リリーが発表したプレスレリース(文献1)を解説致します。
文献1.
Lilly 's Donanemab Significantly Slowed Cognitive and Functional Decline in Phase 3 Study of Early Alzheimer's Disease , May 3, 2023 Lilly News Release
, May 3, 2023 Lilly News Release
リリーは、2023年5月3日、ドナネマブが早期ADの方の認知機能および日常生活機能の低下を有意に遅延させることを示すTRAILBLAZER-ALZ 2試験(無作為化二重盲検プラセボ対照第III相試験)において肯定的な結果を得たと発表した。ドナネマブは、Integrated Alzheimer's Disease Rating Scale(iADRS)*1 のベースラインから18ヵ月までの変化量において、主要評価項目を達成した。主要評価項目であるiADRSは、認知および日常生活動作(金銭管理、運転、趣味活動、時事問題に関する会話など)を評価するものであるが、さらに、認知機能および日常生活機能の低下に関するすべての副次的評価項目も達成され、統計学的に有意な、主要評価項目と同程度の臨床的ベネフィットが示された。
この試験は、ADによる臨床的および機能的な低下を35%という高い水準で遅延させる効果を認めた初めての第III相試験である。