
ゲノム動態プロジェクトのYang Chi-Chun研究員、正井久雄所長らは「Cdc7はヒト細胞においてClaspimのChk1結合ドメインをリン酸化することにより複製ストレスチェックポイントを活性化する」について米国科学雑誌eLifeに発表しました。
DNA複製は、種々の内的外的要因によって阻害される。そのような場合細胞は、障害を除去し、複製を再開し、最終的にDNA複製を完了させるために、複製ストレスチェックポイントシステムを有する。この過程には進化的に保存されたATRキナーゼ-Claspin-Chk1キナーゼのシグナル伝達経路が関与する。Claspinは複製停止シグナルを上流のATRからエフェクターキナーゼChk1へと伝達する仲介分子として機能する。この過程には、Claspin分子上のCKBD(Chk1 binding domain)のリン酸化が必須であるが、そのリン酸化を行うキナーゼの詳細は不明であった。一方、複製開始に必須な役割を果たすCdc7キナーゼは、複製ストレスチェックポイントに要求されることを我々のグループは報告していた(Kim et al. Oncogene 27:3475-3282[2008])が、そのメカニズムは不明であった。
今回、私たちは、Cdc7は、ヒトがん細胞株においては、複製ストレスに応答して、CKBDをリン酸化することにより、複製ストレスチェックポイントを活性化することを明らかにしました。一方、ヒト正常細胞株ではCdc7より、カゼインキナーゼCK1γ1がCKBDリン酸化の主要な役割を果たすことも示しました。これらの発見は、複製チェックポイント活性化のメカニズムの一端を解明するとともに、がん細胞と非がん細胞において、異なる制御因子が関与することを示します。さらに、がん細胞と正常細胞の複製制御メカニズムの違いを利用し、がん細胞死を特異的に誘導する、新たな制がん技術の開発が可能です。
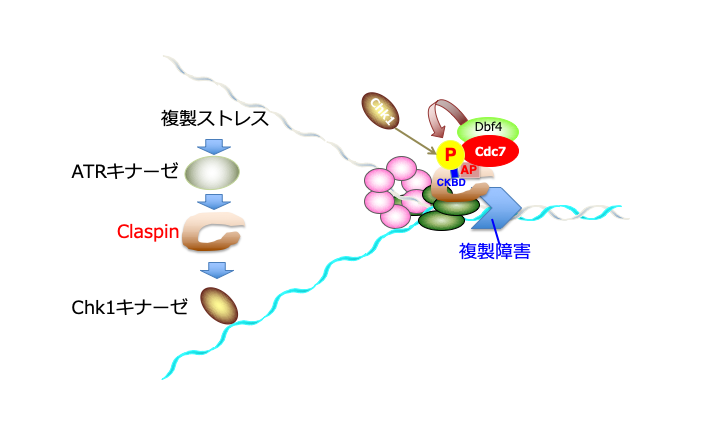
DNA複製が複製障害により停止すると、Cdc7キナーゼはAP(Acidic Patch; 酸性パッチ領域)を介してClaspinにリクルートされ、CKBD(Chk1結合ドメイン)をリン酸化する。このリン酸化に依存してChk1がClaspinに結合し、活性化される。