
Dysregulation of post-transcriptional modification by copy number variable microRNAs in schizophrenia with enhanced glycation stress.
Yoshikawa A, Kushima I, Miyashita M, Toriumi K, Suzuki K, Horiuchi Y, Kawaji H, Takizawa S, Ozaki N, Itokawa M, Arai M. Transl Psychiatry. 2021 May 28;11(1):331. doi: 10.1038/s41398-021-01460-1. PMID: 34050135
昨今のゲノム技術の進歩によって大規模なゲノム研究が推進されています。例えば、日本人集団サンプル[2458名の統合失調症(SCZ)及び、1108名の自閉症スペクトラム障害(ASD)の症例]を用いたゲノムワイドのCNV解析からは、稀なexonic-CNVsが幾つも同定されています[2]。また近年では、マイクロRNA(miRNA)を介した遺伝子発現制御がSCZやASD、知的障害などの病因とも関与していることが注目されています[3, 4, 5]。miRNAは一般に標的遺伝子の3'UTRを認識し、その結合を介して遺伝子発現のサイレンシングを担う一本鎖RNA小分子であり、CNV領域内に位置するmiRNA群(CNV-miRNAs)は様々な機能分子ネットワークの制御に重要な役割を担っている事が報告されています。私たちはこれまでペントシジン蓄積という特定の代謝経路障害を呈する約4割の統合失調症の亜集団[1]に着目し、表現型への寄与を説明する遺伝・環境因子を探索してきました。本研究では、稀なCNVを保有する209名の症例を対象にmiRNAsに焦点を当て、ペントシジン蓄積が亢進している統合失調症の病因に関する新しい洞察を得るための解析を行いました。
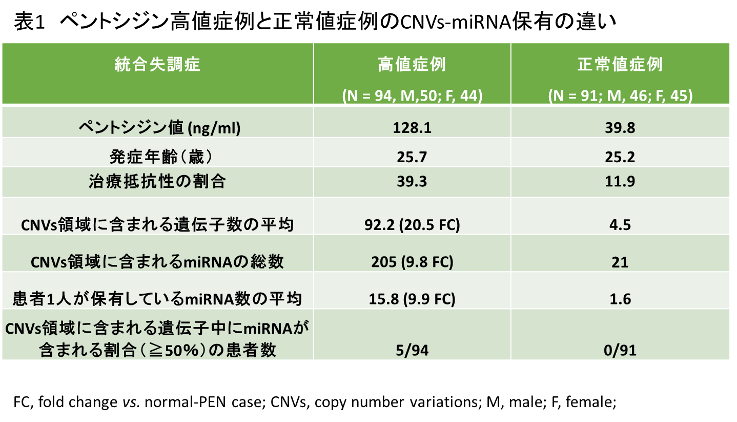
ペントシジン高値の症例では、CNV領域に含まれる遺伝子数が多く、その領域に含まれるmiRNA数がペントシジン正常値群に比べて約9.8倍集積していることを明らかにしました。また、一人の患者が保有しているmiRNA数も平均で約9.9倍の集積が認められました(表1)。
次に、同定されたmiRNAsがどのような標的遺伝子群を介して分子ネットワーク制御に関与しているのか検討を行いました。その結果、ペントシジン蓄積を特徴とする亜集団において特徴的なmiRNAsが同定され、特に、グルタミン酸やGABA受容体シグナル伝達に関与するシナプス神経伝達機能や抗酸化ストレス機能などに関与する遺伝子ネットワークがmiRNAによって影響を受けている可能性を発見しました(図1)。
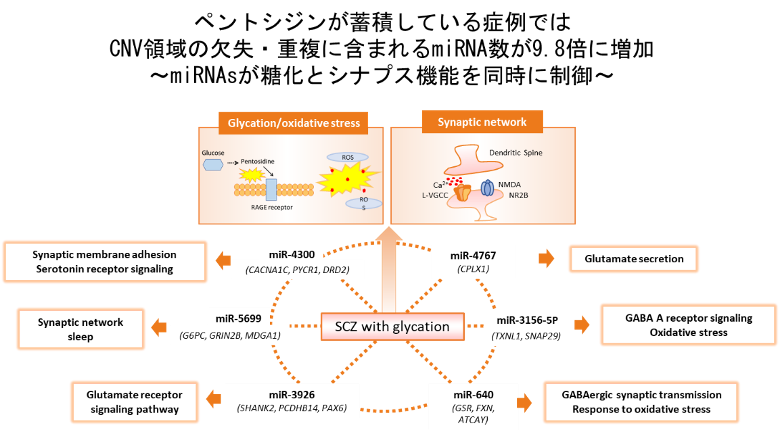
miRNA領域の欠失・重複が、標的遺伝子群の発現変動を介し、ペントシジン蓄積を惹起している可能性がある。標的遺伝子群は、シナプス可塑性、GABA神経伝達、グルタミン酸神経伝達、酸化ストレスと関連している。例えば、MIR 4300は、CACNA1C(calcium voltage-gated channel subunit alpha1 C)遺伝子やDRD2(Dopamine D2 Receptor)遺伝子のような再現性の高い統合失調症リスク遺伝子を標的としています。また、MIR4767はシナプス小胞エキソサイトーシスで機能するタンパク質であるCPLX1(Complexin 1)を標的とし、その他にもMIR5699が糖代謝制御に関わるG6PC(Glucose-6-phosphatase, catalytic subunit)遺伝子、MIR640が酸化ストレス制御に関わるGSR(glutathione-disulfide reductase)遺伝子を標的としています。
本研究は、ペントシジンが蓄積している症例においてmiRNAsが糖化・酸化ストレス、シナプス機能を制御していることを示唆する日本人ゲノムを用いた初めての研究成果です。本研究において、ペントシジンが蓄積する症例の病態に強い影響をもつmiRNAが患者で高頻度に見つかったことから、今後はペントシジン高値の統合失調症に対する治療アプローチのひとつとしてこれらのmiRNAを標的とした戦略が期待されます。