新型コロナウイルスや医学・生命科学全般に関する最新情報


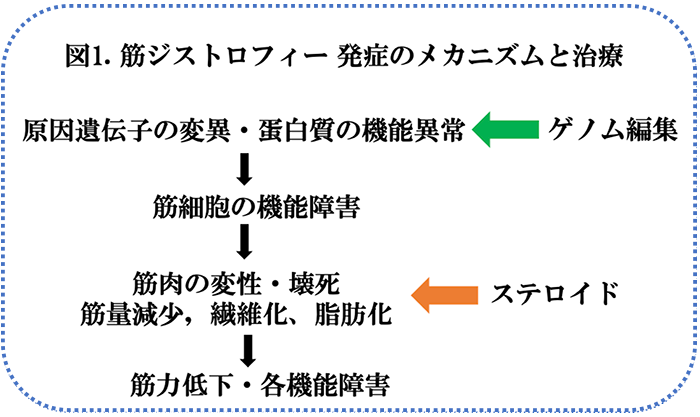
筋ジストロフィー症*1は、骨格筋の壊死・再生を主病変とする遺伝性筋疾患の総称であり、一般に、原因遺伝子に変異が生じると、タンパク質の機能が障害され、細胞の機能を維持できなくなり、筋萎縮や脂肪・線維化 が生じ、筋力が低下し運動機能など各機能障害をもたらします(図1)。筋ジストロフィー症の中でもっとも頻度が高いDuchenne型筋ジストロフィー症(DMD; Duchenne muscular dystrophy)は、幼児期から始まる筋力低下・動揺性歩行・登攀性歩行・仮性肥大を特徴とするX連鎖劣性遺伝病です。現時点で筋ジストロフィー症の根本的な治療法はありません。DMDでは、ステロイドの骨格筋障害への短期間投与の有効性が確立されていますが、原因となるジストロフィン遺伝子が同定されていますので、ゲノム編集による新しい治療方法の確立が望まれます。今回、Yale大学やMassachusetts大学を中心とした米国の研究チームは、DMD患者の個別化治療として、ジストロフィンの発現を亢進するdCas9-VP64*2トランスジーンを投与した結果、残念ながら、患者は、10日以内に死亡する転帰となったことを報告しました。その査読前論文(文献1)がmedRxivに掲載されましたのでこれについて紹介致します。DMDのゲノム編集による治療に関しては、今後の臨床試験は安全性を顧慮してより慎重なものになることが予想されます。
文献1.
Angela Lek et al., Unexpected Death of a Duchenne Muscular Dystrophy Patient in an N-of-1 Trial of rAAV9-delivered CRISPR-transactivator, medRxiv 2023-05-18 [preprint].
DMDは染色体に位置するジストロフィン遺伝子が突然変異により機能喪失することによって引き起こされる。したがって遺伝子治療によって、ジストロフィン遺伝子の機能を回復させることが治療に有効であると考えられる。現時点で、エクソン・スキッピング*3などの方法が、動物モデルでは成功しているが、臨床には反映されていない。したがって、本プロジェクトは、DMDの患者さんにおいて、ゲノム編集によるジストロフィン遺伝子の機能回復による治療効果を評価することを目的とする。
今回の結果は、CRISPRによる遺伝子編集によるものではなく、そのデリバリーに利用する高用量のrAAVにより、この被験者に特有の、毛細血管漏れを伴う免疫応答が引き起こされたことによると考えられる。