肝硬変治療薬の開発
肝硬変とは
肝硬変とは、種々の要因で慢性肝炎や肝障害が進行することで、肝臓が硬くなった状態をいいます。肝硬変は、重症度に応じて代償性肝硬変と非代償性肝硬変に分類されます。代償性肝硬変は肝機能が保たれて臨床症状がほとんど見られません。一方で、非代償性肝硬変では肝性脳症や腹水など肝不全で見られるような症状が認められます。一般に、肝硬変の重症度はChild-Pugh分類によって3段階に分けられ、グレードAは代償性肝硬変に、グレードB・C が非代償性肝硬変に該当します。
肝硬変になると肝がんの発症率が増加します。日本における肝硬変患者数は30万人以上と推定され、年間3万人が肝硬変や肝がんで死亡しています。また2016年以降、肝硬変の有病率は増加傾向にあり、世界人口の約1.3%が肝硬変に進行しているという報告もあります(Clin. Gastroenterol. Hepatol., 2024)。肝硬変を治療できれば、肝がんの発症リスクを軽減できると期待されます。しかし、現在肝硬変に有効な治療薬は存在していません。
肝硬変は、これまでC型肝炎ウイルスやB型肝炎ウイルス感染によるウイルス性の肝硬変が大部分を占めていましたが、最近ではアルコールや非アルコール性脂肪肝炎(NASH)といった非ウイルス性肝硬変の割合が約3分の2となり、逆転しました(Hepatol. Res., 2024)。特にNASH(MASH)肝硬変は世界的に急増しており、注目されています。
MASLD / MASHとは
非アルコール性脂肪性肝疾患(NAFLD)は世界で最も多い肝疾患で、全世界での有病率は約30%と推定されています。そのうち約10%は肝硬変や肝がんに移行する進行性の病態であるNASHと報告されています。NAFLDは肥満や糖尿病などの生活習慣病と密接に関連している肝疾患ですが、これまでその診断基準は肝臓への脂肪蓄積を引き起こしうる他の肝疾患の除外に基づいており、病態の中核をなす代謝機能異常は考慮されてきませんでした。NAFLDという病名が正確に病態を反映していなかったことから、新しい疾患概念が提唱され、2023年に代謝機能障害関連脂肪性肝疾患(MASLD)へと名称が変更されました。また、これまでNASHとされていた脂肪肝炎の病態は代謝機能障害関連脂肪肝炎(MASH)へと変更されました。日本や海外での研究において、NAFLD診断された方の96-99%はMASLDと一致すると報告されています(Hepatol. Res., 2024など)。
NASH / MASHに対する治療薬の開発は困難を極めてきましたが、2024年3月にFDAはResmetiromを経口治療薬として承認しました。Resmetiromは甲状腺ホルモン受容体β作動薬であり、肝臓内脂肪量の減少に伴いMASHを改善させることを主要目的としています。従って、MASH肝硬変は治療適用外であり、新たな薬剤の開発が求められています。
PRI-724のMASH肝線維症治療
PRI-724はβ-カテニンとCREB-binding protein(CBP)との結合を選択的に阻害しWntシグナルを阻害する化合物です。私たちはC型肝炎ウイルス誘発性肝線維化マウスにPRI-724を投与した結果、肝線維の減弱が認められることを報告しています(Sci. Rep., 2017)。
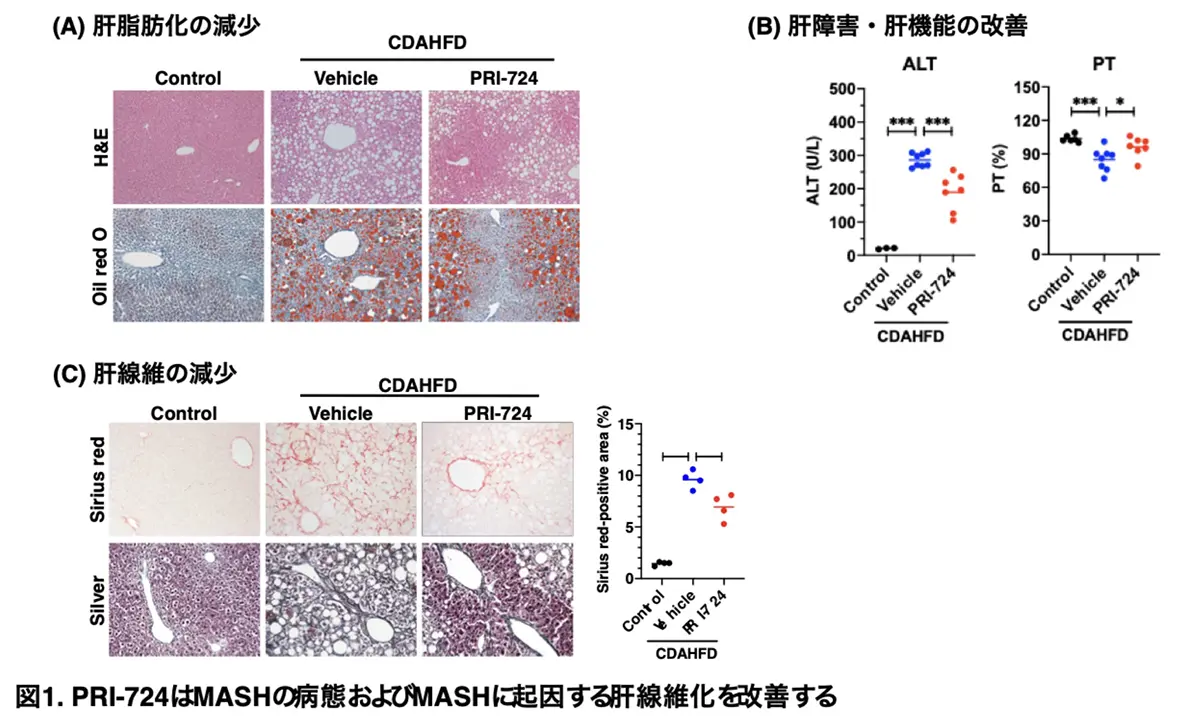
またコリン欠乏・メチオニン減量高脂肪食(CDAHFD)をマウスに14週間与えることで作製したMASH誘発肝硬変モデルにおいても、PRI-724(20 mg/kg, ip)を6週間投与した結果、肝脂肪化の減少(図1A)、肝障害や肝機能の改善(図1B)、肝線維の減少(図1C)が認められました。
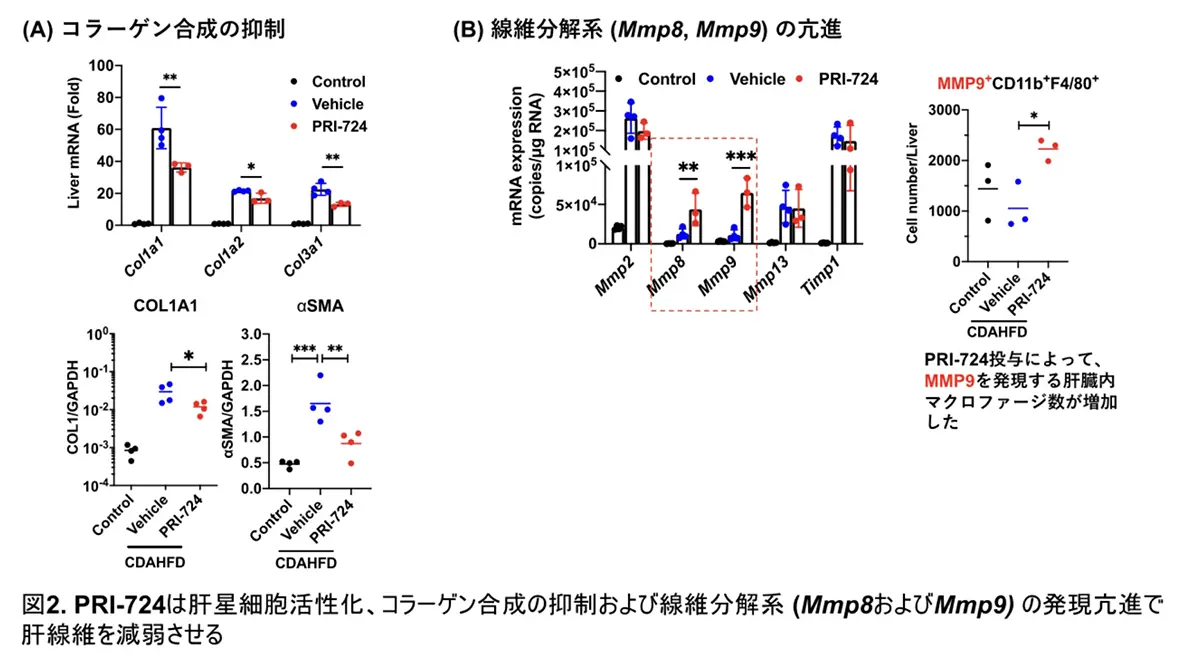
続いてPRI-724による肝線維減少の機序について解析しました。その結果、PRI-724は肝星細胞あるいは肝実質細胞のコラーゲン合成の抑制に加え、線維分解酵素(MMP-8, MMP-9)を産生する免疫担当細胞の誘導を介した脱肝線維化を亢進するという二つの作用により肝線維化を減弱することが明らかとなりました(図2)。
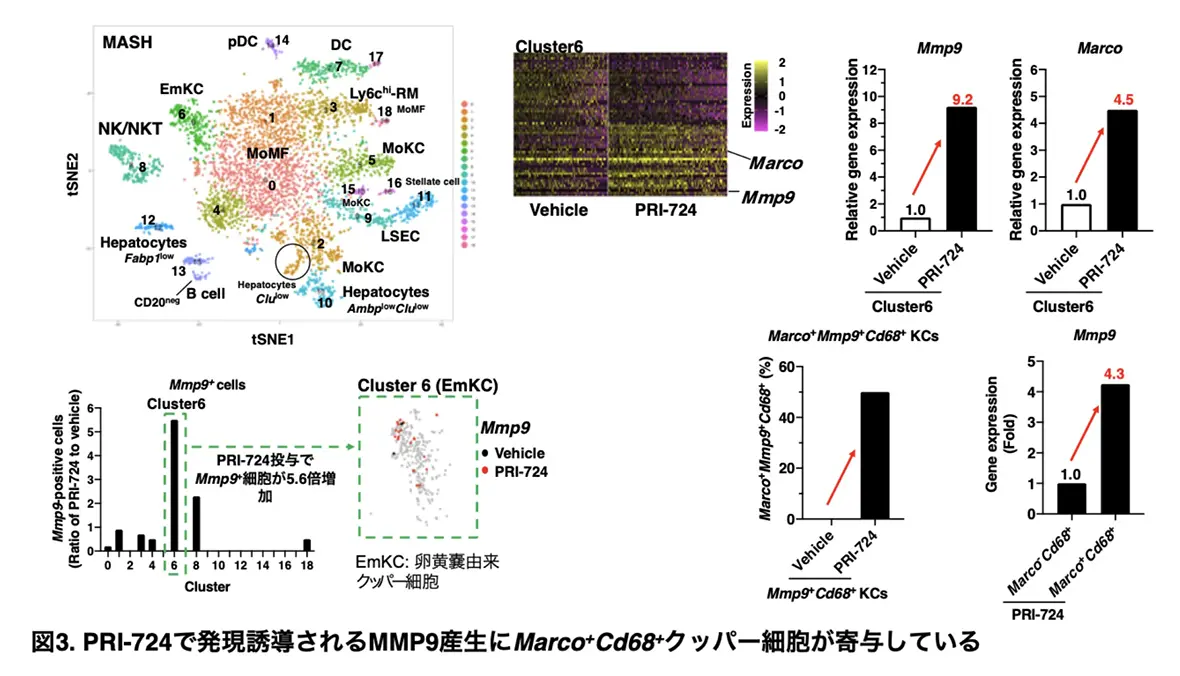
さらにPRI-724による病態の改善に寄与する細胞群を明らかにするため、PRI-724投与後の肝臓からリンパ球(主に肝臓内マクロファージ)を分離し、シングルセルRNAシーケンス解析を行いました。その結果、非炎症性のマクロファージである卵黄嚢由来のクッパー細胞 (EmKC) に該当するcluster 6においてMmp9陽性細胞の割合がPRI-724投与で2.0%から11.2%と5.6倍増加したことから、EcKCがPRI-724によるMmp9産生に寄与する細胞集団と考えられました(図3)。またcluster 6では1細胞あたりのMmp9およびMarcoの発現量がPRI-724投与によってそれぞれ9.2倍、4.5倍増加していたため、Mmp9とMarcoの関連に着目して解析を行いました。Mmp9発現クッパー細胞の50%はMarco陽性細胞であり、Marco陽性細胞では1細胞あたりのMmp9発現量が4.3倍増加していたことから、PRI-724で誘導されるMmp9の少なくとも一部は、Marco+Cd68+ クッパー細胞で産生されることが示唆されました (図3)。
以上の結果から、PRI-724はコラーゲン生成抑制と肝線維分解を亢進する両作用を示すことで進行した肝線維も消失させ、さらに肝機能の正常化も惹起する、これまでの肝線維化治療薬とは異なった薬剤であることが明らかとなりました。PRI-724はMASHに起因する肝線維化の治療薬となることが期待されます。
今後の展望
MASHモデル作製に使用した飼料 CDAHFDは体重増加、空腹時血糖値の増加やインスリン抵抗性を示さないなどヒトMASHと異なる点もあります。そこで、私たちはヒトMASHの病態に最も近いと報告されているGAN dietを用いたMASHモデルでの評価も行っており、PRI-724投与によって肝脂肪化や肝障害の減弱、肝線維化や肝機能の改善に加え、体重減少や高脂血症および高血糖が改善することを見出しています。これらの結果はPRI-724が肝線維化の減弱だけではなく、MASH病態の改善にも寄与することを示唆していますが、その詳細な機序は明らかとなっていません。現在作用機序の解析を進めています。
<発表論文>
- Tokunaga Y, Osawa Y, Ohtsuki T, et al. Sci Rep. 2017. 7(1):325.
- Yamaji K, Iwabuchi S, Tokunaga Y, et al. Biomed Pharmacother. 2023. 166:115379.

