新型コロナウイルスや医学・生命科学全般に関する最新情報


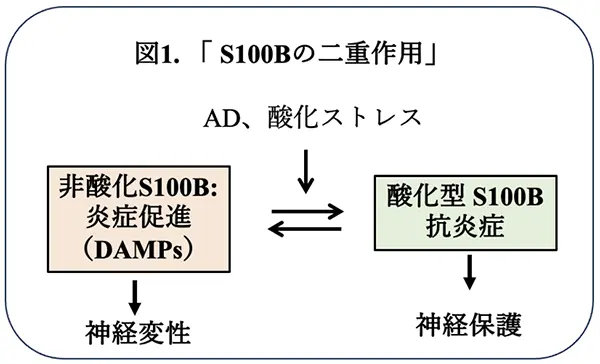
S100は、20種類以上のファミリーからなる2つのEF-handモチーフ*3を有する分子量10~13 kDaのカルシウム結合性タンパク質です。機能的には、細胞内カルシウム濃度を一定に保つバッファーとして働きますが、それ以外にも、細胞の増殖、転移、分化、アポトーシスを制御するなど、細胞内外で様々な作用を有しています。最近、S100*1は、病理学的にも重要であることがわかって来ました。例えば、先週の記事(「アルツハイマー病の危険因子としての腸内炎症」〈2024/2/20掲載〉)で述べました、腸の炎症マーカーであるカルプロテクチン(calprotectin)は、S100ファミリーに属します。また、脳で最も豊富な蛋白質の一つのS100Bは、脳虚血やADなどの神経変性疾患では、アストロサイトの異常活性化に伴って産生、分泌が亢進し、damage-associated molecular patterns(DAMPs)/アラーミンとして炎症を促進し、神経変性や神経細胞死に関わっている(図1)と推定されています。これとは対照的に、ADで発現が増加するS100Bは、アミロイドβ(Aβ)の凝集と神経毒性を抑制し、神経保護的に働くのではないかと考えられています(図1)。これに一致して、ポルトガル・リスボン大学のCoelho R博士らは、イン・ビトロの実験系において、酸化型S100Bは野生型S100B(非酸化型)よりもアミロイドβの凝集を抑制し、神経保護的に働くことを示して、その結果を報告しました(図1)(文献1)。このようなS100Bの持つ二重性のメカニズムを理解することはADの治療法開発においても重要であると思われますので、今回はこの論文を紹介いたします。
文献1.
Secondary Modification of S100B Influences Anti Amyloid-β Aggregation Activity and Alzheimer's Disease Pathology, Coelho R et al. Int J Mol Sci 2024 Feb 1;25(3):1787.
生理的な条件下では活性酸素はシグナル伝達分子として機能することが知られているが、Aβなどのアミロイド蛋白が蓄積する神経変性疾患では、活性酸素により、酸化ストレスが引き起こされるので、それを防御するメカニズムが重要になる。S100Bは、炎症促進性に働くDAMPs/アラーミンの一つであり、神経変性促進的に作用すると思われるが、これとは逆にAβの凝集・毒性を防御し、Aβによる神経変性を抑制するシャペロンとして働くことが明らかになっている。したがって、本研究の目的は、酸化ストレスの増強したAD脳を模倣した状態における、S100Bの神経変性に対する作用を解析することである。
本研究より、S100Bが非酸化型から酸化型にシフトすると炎症促進性から抗炎症性になることが示された。S100Bの神経炎症における両刃の剣の作用は、このようなメカニズムが鍵になっていると推定された。