新型コロナウイルスや医学・生命科学全般に関する最新情報


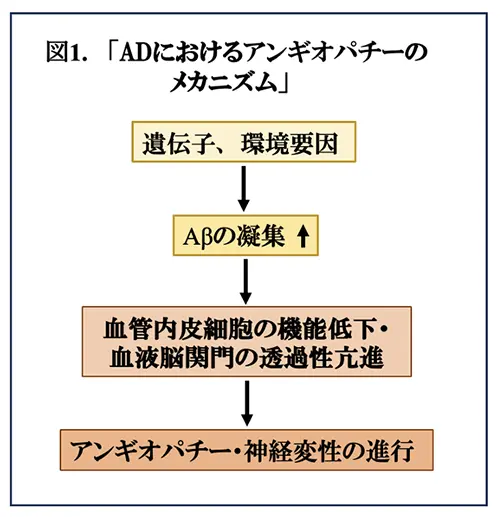
ADでは、脳の萎縮部位に一致して神経細胞の脱落と反応性グリオーシスによる慢性炎症が認められ、これらに伴って、アミロイド蛋白の凝集・蓄積による老人斑(senile plaque)や神経原線維変化(neurofibrillary tangle)などの異常な構造物が形成されることが病理組織学的特徴ですが、多くの症例でアミロイドアンギオパチーが見られることも注目されます。これはアミロイドβ (Aβ)の凝集物が血管壁に蓄積することにより血管内皮細胞の機能が低下し、血液脳関門*4の透過性が亢進する結果、Aβによる神経変性病態を進行させる機序が考えられます(図1)。しかしながら、現時点で詳細なメカニズムは、検討されていません。この問題に関して、中国上海の復旦大学(Fudan University)のYuhan Li博士及び共同研究者らは、Aβの低分子凝集物であるoligomersやprotofibrilsが血管内皮細胞の細胞間接着に重要であるカドヘリンの機能を阻害することがADにおける初期の現象であることを示し、最近Nature Communicationsに報告した論文(文献1)を紹介いたします。この研究は、ナノテクノロジーの研究分野において、ナノ分子がカドヘリンの機能を阻害することにより血管内皮細胞の機能障害を誘発する現象を応用したものであり、さらに、最近の研究で、protofibrilsが炎症に関与すること(Aβプロトフィブリルによる血液凝固因子XIIaの活性化〈2024/1/30掲載〉)、protofibrilsがADの治療標的として明らかになったこと(早期アルツハイマー病に対するLecanemab(レカネマブ)の治療効果〈2023/5/10掲載〉)を考慮すれば、非常に興味深いと思われます。
文献1.
Endothelial leakiness elicited by amyloid protein aggregation. Yuhuan Li, Nature Communications volume 15, Article number: 613 (2024)
興味深いことに、血管内皮細胞の機能低下はAβの蓄積にリンクしており、大部分(80~90%)のAD患者さんで脳にアミロイドアンギオパチーが見られることも注目されてきた。本プロジェクトは、そのメカニズムを理解することを研究目的とした。
この目的のため、ヒトの血管内皮細胞(HMVECs)及び、マウス脳の血管系において、アミロイド蛋白による血管内皮細胞の漏出促進に対する効果(APEL)を検討した。