医学・生命科学全般に関する最新情報


以前、「がんワクチン」について説明しました(がんについてNo.4)。
では、実際に現在、がんワクチンの研究はどこまで進んでいるのでしょうか。
がんに関係するワクチンとしては、すでに実用化されているものがあります。
たとえば、子宮頸がんの原因となるヒトパピローマウイルス(HPV)を防ぐワクチンです。これは、がんそのものではなく、がんの原因となるウイルス感染を予防するワクチンです。
一方で、すでに発症したがんを治療したり再発を防いだりするワクチンは、まだ日本では正式に承認されていません。
しかし世界中で研究が進んでおり、有望な結果も出始めています。今回はその一例として、メラノーマ(悪性黒色腫)に対する個別化mRNAがんワクチン (文献1)を紹介します。
今回紹介するのは、メラノーマ(悪性黒色腫)というがんです。
これは主に皮膚にできるがんで、見た目はほくろに似ていることがあります。日本では比較的少ないものの、患者数は増加傾向にあります。
メラノーマは、早期に見つかれば手術で治せることもありますが、進行すると再発や転移を起こしやすく、治療が難しくなります。
メラノーマの根治には現在でも手術が一番効果のある方法です。
ただし、手術で見えるがんを取り除いても、体内にごく少数のがん細胞が残っていることがあります。これが後に増えて、再発につながります。この再発に対する治療成績を大きく向上させた薬があります。
それが、キイトルーダやオプジーボです。
これらは「免疫チェックポイント阻害薬」と呼ばれます。
本来、キラーT細胞(がん細胞を攻撃する免疫細胞)には、過剰な攻撃を防ぐための“ブレーキ”があります。
がん細胞はこの仕組みを利用して、キラーT細胞の攻撃を弱めてしまいます。
キイトルーダやオプジーボは、このブレーキを外し、キラーT細胞が再び働けるようにする薬です。
ただし、この治療だけで全員が治るわけではありません。
免疫チェックポイント阻害薬は、すでに体内にいるキラーT細胞の働きを強める薬です。
一方、がんワクチンは、新たにがんを攻撃するキラーT細胞を増やすことが期待されます。
そこで免疫チェックポイント阻害薬にがんワクチンを併用することで、よりがんの再発が抑えられるのではないかと考えられました。そこで行なわれたのが今回の研究です。
進行したメラノーマ(ステージIIIB~IV)の患者で、手術によりがんを完全に取り除いたあと、2つの治療法が比較されました。
その結果、18か月後に再発せず生存していた人の割合は次の通りでした。
つまり、ワクチンを追加したほうが再発が少なかったのです。
これは、「すでにある免疫反応をキイトルーダが強め、さらにワクチンが新しい免疫反応を増やしたためではないか」と考えられています。
このことを説明する前に
まず、「がんワクチンとは何か」を整理しましょう。
がんワクチンの目的はがんを攻撃するキラーT細胞を新たに増やすことです。
がんについてNo.4で説明したように、まず、正常細胞にはなく、がん特異的なタンパク質断片、あるいはその設計図(mRNAなど)、すなわちがんワクチンを体の中に投与します。
投与されたワクチンは樹状細胞という免疫細胞に取り込まれます。それにより樹状細胞は目印(がん特異的タンパク断片)を細胞表面に提示します。mRNAのかたちでとりこまれても、樹状細胞が細胞内でタンパクをつくり、細胞表面に提示します。
その情報をうけたキラーT細胞は活性化し、その目印のある細胞、すなわちがん細胞をみつけだし攻撃します。このようにしてがんを攻撃するキラーT細胞を増やすことができます。
つまり
ワクチン投与
↓
樹状細胞が取り込み、キラーT細胞に情報をおくる
↓
キラーT細胞が活性化
↓
がん細胞を攻撃
簡単にいえば、がんワクチンとは「キラーT細胞に、がんの目印を教える治療」です。
ここが最も重要な点です。
がん細胞は、増殖する過程でDNAの複製を繰り返します。
その過程で、ミス(変異)が起こることがあります。
この変異は偶然に起こる部分が大きいため、
では、変異の内容が同じとは限りません。
DNAはタンパク質の設計図です。
設計図にミスがあれば、そこから作られるタンパク質も正常なものとは少し違った形になります。
この「がん細胞だけが持つ変化したタンパク質」が、キラーT細胞が攻撃する細胞を見つける目印になります。
AさんとBさんではDNAの変異が違うのでタンパク質の変化も異なります。すなわち、AさんとBさんではキラーT細胞の攻撃するための目印が違うのです。
つまり、がん細胞の目印が人によって違う以上、
全員に同じワクチンを使うより、その人のがんに合わせたワクチンのほうがより合理的
ということになります。
これが「個別化がんワクチン」です。
ここで、生物学の基本を少しだけ確認します。
細胞の中にはDNAがあります。
DNAはタンパク質の設計図そのものです。
しかし、DNAのすべての設計図が使われるわけではありません。その細胞に必要なタンパク質の設計図だけがコピーされます。
そのコピーがmRNAです。
そして細胞は、そのmRNAを読み取ってタンパク質を作ります。
流れで言えば、
DNA → mRNA → タンパク質
です。
患者のがん組織と正常組織を調べ、がん細胞にだけある変異を探します。
変異がDNAにあっても、使われていなければ意味がありません。
そこで、変異した部分がmRNAとして作られているか確認します。
mRNAが多いほど、そのタンパク質も多く作られている可能性があります。
すべての変異タンパク質が目印になるわけではありません。
細胞表面に出やすいもの、キラーT細胞が認識しやすいものなど、いくつか条件があります。
そこでAIなどを用いて、有望な候補を絞り込みます。
選ばれた複数の目印をもとに、その患者専用のワクチンを製造します。
目印そのもの(タンパク質断片)を注射する方法もあります。
しかし現在は、目印の設計図であるmRNAを使う方法が注目されています。
理由は主に2つあります。
mRNAワクチンは、基本の製造方法が共通です。
患者ごとに変えるのは、中に入れる配列(設計図)の部分です。
つまり、外枠は同じで、中身だけ差し替えればよい。
がんは時間とともに進行する可能性があるため、このスピードはとても大事です。
1つの腫瘍の中にも、少しずつ性質の違うがん細胞が混ざっています。
そのため、目印が1種類だけだと、一部のがん細胞を見逃す可能性があります。
mRNAワクチンでは、複数の目印を同時に入れやすいという利点があります。
今回の研究でも、多くの患者で34種類もの目印が使われました。
ただし、mRNAには弱点があります。
とても壊れやすく、そのまま体内に入れるとすぐ分解されてしまいます。
そこで使われるのが、LNP(脂質ナノ粒子)です。
これは脂質でできた非常に小さな粒子で、mRNAを包み込みます(図1)
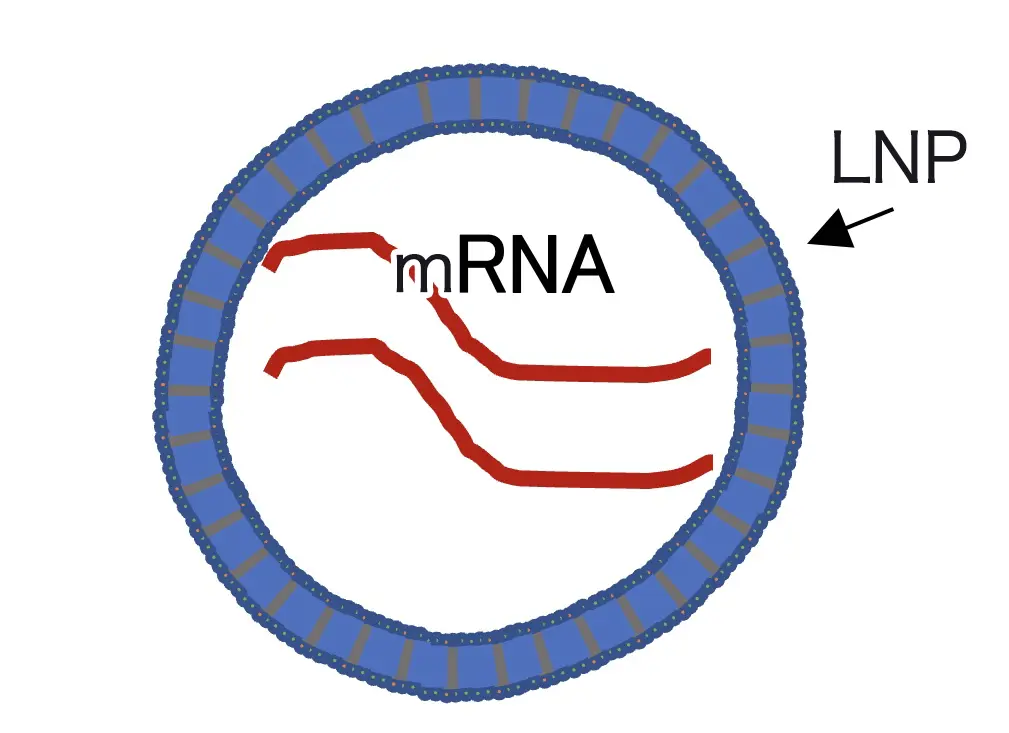
LNPには
mRNAをまもる
樹状細胞に取り込まれやすくする
細胞内でmRNAを放出する
といった役割があります。
更に、樹状細胞がキラーT細胞に情報を確実に伝達するには目印となるタンパク質断片を細胞表面に提示するとともに、
感染や細胞の破壊などが起きたときに出る「危険信号」を受け取って樹状細胞が活性化している必要があります。
LNPはこの危険信号の役割も果たしています。
この技術が、mRNAワクチン実現の大きな鍵になりました。
個別化mRNAがんワクチンは、まだ発展途上の技術です。
しかしメラノーマだけでなく、膵臓がん(文献2)、乳がん(文献3)などでも研究が進んでいます。
従来の「同じ病気には同じ治療」から、
一人ひとりのがんの特徴に合わせて治療を変える時代へ向かっているのです。