医学・生命科学全般に関する最新情報


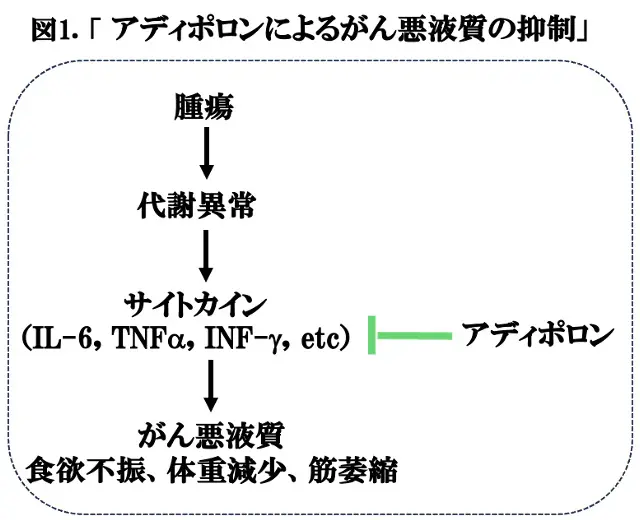
がんの患者さんは、病状の進行に伴い、体重減少、低栄養、消耗状態が徐々に進行していきますが、このような状態をがん悪液質といいます。がん悪液質の原因は、体内の代謝異常が関与しているが、代謝異常の原因の中心は炎症性サイトカインの過剰分泌であり、これに引き続いて、筋萎縮が進行すると考えられています(図1)。炎症性サイトカインによる代謝異常は、病期が比較的早い段階から認められ、食事摂取量が減少していない段階や体重減少がまだ認められない段階に起こります。したがって、がん悪液質において、食欲不振による摂取量減少は二次的な症状であり、経口摂取量の低下のみが原因の飢餓状態とは本質的に異なります。悪液質は、がんの患者さんの50~80%に合併しますが、がんの種類によって、例えば、肺がん、膵がん、胃がん、食道がんなどは発生頻度が高く、一方、乳がんでは頻度が少ないことが知られていますが、理由は不明です。悪液質は、患者さんのQOL*3を低下させるだけでなく、抗がん剤の治療効果を弱めたり、副作用を強めたり、さらには寿命にまで影響を及ぼすこともありますので、悪液質の病態生理に関する理解が深まり、それに基づいた治療法が確立されることが望まれています。この様な状況において、ベルギーのルーヴァン・カトリック大学のIsabelle S Massart博士らは、2つの大腸がん悪液質のマウスモデルにおいて、アディポネクチン受容体作動薬であるアディポロン投与により、悪液質が改善され、さらに、体重減少や筋萎縮が抑制されることを見出し、ヒトのがん悪液質にも適応できる可能性が期待されています。また、炎症、代謝異常やアディポネクチンは生活習慣病や神経変性疾患の病態でも重要であり、多くの視点からも興味深いと思われます。これらの結果がJ Cachexia Sarcopenia Muscleに掲載されていますので(文献1)、今回はそれを紹介いたします。
文献1.
Administration of adiponectin receptor agonist AdipoRon relieves cancer cachexia by mitigating inflammation in tumour-bearing mice, Isabelle S Massart et al, J Cachexia Sarcopenia Muscle 2024 Jun;15(3):919-933.
がん悪液質は、生命を脅かす、炎症による消耗性の症候群であり、現状では治療法が無い。最も豊富なアディポカインであるアディポネクチンは、炎症の調節だけでなく、いくつかの代謝過程で重要な役割を担っている。我々の目的は、アディポネクチン受容体作動薬である合成アディポロンを投与することにより、がん悪液質と、それに関連した筋萎縮を治療できるかどうか検討することである。
2つの異なるマウスの大腸がんモデルにおいて、がん悪液質に対するアディポロンの効果を研究した。一つ目は、7週齢、雄のCD2F1マウス*4でC26大腸がん細胞、または、溶媒を皮下に注入し、注入後、6日後から5日間連続、アディポロン(50 mg/kg)、または、溶媒で処理した。二つ目は、多数の腸ポリープが発生する遺伝的モデルであるApc Min/+マウス*5に5日間連続、アディポロン(50 mg/kg)を12週間、投与した。C57BL/6J野生型マウスをコントロールに用いた。両モデルともいくつかのパラメーターが評価された;体重、握力、血清パラメーター、及び、生体外(ex vivo);筋肉、肝臓、脂肪の分子的変化。
いずれの大腸がんマウスモデルにおいても、がん悪液質の進行に対するアディポロンの抑制効果が観察された。
この研究により、アディポロンは、マウスモデルにおいて、炎症やコルティコステロンの分泌を抑え、体重減少や筋萎縮を防ぐことにより、がん悪液質のフェノタイプを改善することが示された。したがって、アディポロンは、がん悪液質の治療に結びつく可能性があると考えられる。