医学・生命科学全般に関する最新情報


昨年の前半は、アルツハイマー病(AD)において、抗アミロイドbモノクローナル抗体による免役療法の第3相臨床治験が成功し、大きなニュースになりましたが、後半には、SCZにおいて、ムスカリン受容体作動薬であるKarXT が第3相臨床治験に成功・承認され、話題になりました。少し前になりますが、Natureで発表されたニュース(文献1)を要約して紹介いたします。
文献1.
New schizophrenia drug could treat Alzheimer’s disease, Half a dozen drugs are in trials for conditions of the brain, but success is not guaranteed., By Diana Kwon, Nature eNEWS 21 November 2024
精神病の薬物治療は、1950 年代に、SCZの治療にドパミン D2 受容体拮抗薬として作用するクロルプロマジンが用いられたのが最初であると言われているが、今回、数十年ぶりに異なる作用機序を持つSCZの治療薬が承認され、研究者たちは、精神医学における新しい時代の到来を宣言した。しかしながら、SCZ, ADや脳に関連した疾患の大多数は、臨床試験の初期段階にあり、必ずしも、治療効果が確立されたわけではない。実際、先週、非常に期待されていたSCZ治療薬について、期待はずれの結果が報告された。
この数十年間、SCZ の治療薬は、基本的に同じ作用機序を持つものであった。それらは、障害の特徴的な症状である幻覚や妄想の原因となるドーパミンの働きを鈍らせることにあった。新しく登場した治療薬KarXTは、Cobenfyという商品名で販売されており、ムスカリン受容体を刺激して、抗精神病的に作用し、認知機能を改善する。「私の経歴において、これほどまでに、騒々しい興奮させた精神医学の新しいアプローチはありませんでした」と、テネシー州ナッシュビルにあるヴァンダービルト大学のジェフリー・コーン薬学博士は言う。KarXTがSCZの第3相試験に成功し、米国の規制当局の承認を得たことで、ムスカリン系薬に対する興味が再燃した。KarXTの開発に参加したオーストラリア・メルボルンにあるモナッシュ大学のアーサー・クリストポロス分子薬学博士は、「創薬*3 が精神医学に戻って来ました」と言う。しかしながら、新薬の開発は険しく長い道のりである。11月11日にイリノイ州ノースシカゴの製薬会社アビューは、SCZ の治療薬エムラクリジンがプラセボの効果を上回ることはできなかったと発表した。「この残念な結果が開発中の他のムスカリン系薬に対して何を意味するのかを判断するのは、まだ、時期尚早です。」とクリストポロス博士は言う。
KarXT開発も決して平坦な道のりではなかった。KarXTの一つの活性成分であるキサノメリンは1990年代に開発されてADの精神症状を減弱させることが示された。しかしながら、臨床治験において多くの患者さんは、悪心・嘔吐やその他の副作用のため、この薬の服用を続けることが出来なかった。ムスカリン受容体は脳だけでなく、全身に発現しているため、多くの作用を生じてしまうのではないかと考えられた。KarXTは開発中の多くのムスカリン系薬とともに棚上げされた。KarXT開発の背後にある会社の共同創設者の一人であるコン氏は、「誰もが、ムスカリン受容体アゴニストを治療に用いるのは不可能だろうと思いました。」と言う。
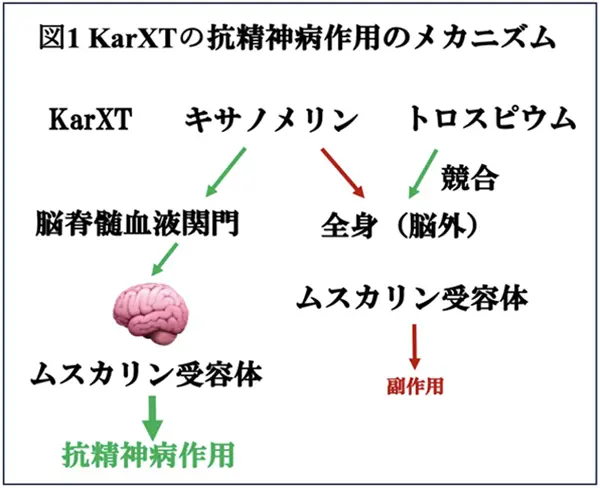
2009年にマサチューセッツ州、ボストンにあるカルナ・セラピュークス社はキサノメリンと別の化合物であるトロスピウムの合剤KarXTを開発した。トロスピウムはムスカリン受容体を遮断するが、脳血液関門を通過しないため、キサノメリンの脳以外の作用を抑えると考えた(図1)。予想通り、SCZの臨床試験では、キサメリン単独の場合に比べて、KarXTの副作用は、減弱することが観察された。
キサノメリンのほとんどの作用は5種類のムスカリン受容体(M1~5)のうち、M1とM4の2つを通して作用する。動物実験によれば、M4は、抗精神病作用に、M1は、認知機能に関係していると思われる。開発中のSCZ治療薬の多くは、一つのタイプの受容体を標的にする。「研究者は、副作用は少なくて、より大きい治療効果に繋がることを望んでいる。」と英国グラスゴー大学の神経科学者アンドリュー・トビンは言う(トビンはダブリンを基点にしてムスカリン薬剤の開発を行うケルテックファルマテラピューティクス社の共同創設者で最高責任者の一人である)。
5種類のムスカリン受容体はリガンド結合部位が似ているため、選択的に作用させることは簡単でない。この目的のために、より類似性の低いリガンド結合部位の外部の部分を通して作用する、いわゆる、アロスティックモデュレーター*4 について研究が行われているとトビンは言う。
エムラクリジンはM4を標的にしたアロスティックモデュレーターであり、ムスカリン製薬の中では最も開発が進んだ薬剤である。「エムラクリジンがアビュー社主導の第2相臨床治験に失敗したことは、KarXTのように、M1とM4の両方の受容体を標的にする必要があることを示唆しているのかも知れません。」とオーストラリア・パークビーユにあるフローレンス神経科学メンタルヘルス研究所の生化学者ブライアン・ディーンは言う。
ニュージャージー州プリストンにある大手製薬会社のブリストルマイヤーズスクイブ(BMS) は、3月にカルナ社を買収し、KaXTがADに見られる精神症状の治療に役立つかどうか、また、双極性障害の患者さんに効果があるかどうかを調査する臨床研究を開始している。
BMS は、さらに、M1受容体の認知機能に対する役割を考慮して、ADの認知機能減弱の改善を目的にした薬剤を設計している。「研究者は、ムスカリン製剤がADの進行を遅らせるのではないかと期待している。」とトビン博士は言う。2016年にトビン博士と共同研究者は、M1受容体を特異的に刺激するとADのマウスモデルの神経変性が改善されたことを報告している。また、ムスカリン受容体は報酬系回路にも多く発現しており、この経路の阻害が鎮痛薬に対する依存症に効果があることが実験動物で示されている。さらに、パーキンソン病に関してもムスカリン経路の刺激による治療効果が検討されている。
「KarXTを巡って、興奮が渦巻いていますが、現時点では、実世界においてどれほど役立つか予測出来ません。特に、臨床試験中の患者さんは入院しており、結果を左右する要因の一つと考えられる環境の影響を受けにくい事を考慮する必要があります。」とテキサス・ダラスにあるUTサウスウェスタンメディカルセンターの精神科医・神経科学者のキャロル・タミンガは言う。(タミンガ博士は、カルナ社の科学顧問としてKarXTの臨床治験に関与した。)
先月、BMSは、2年間KarXTで治療して外来で追跡したSCZ患者さんのデータを公表した。その間、症状は改善し続けたが、11~18%の患者さんは、副作用のため服用を中止した。薬の服用を中止することは、利用出来る他の抗SCZ薬で問題になることがわかっている。「我々は、これらの薬剤について多くを知らなければいけません。」と、タミンガは言う。