医学・生命科学全般に関する最新情報


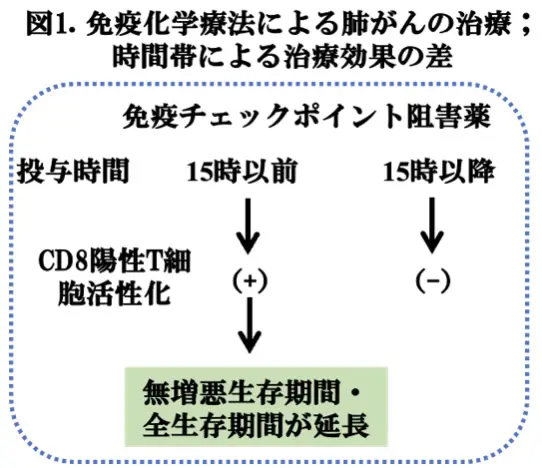
前回、糖尿病の幹細胞移植治療における概日リズムの重要性についてお伝えしましたが(糖尿病の再生医療における概日リズムの重要性〈2026/2/27掲載〉)、これを主に司るのが体内時計*4で、脳の視交叉上核にあります。体内時計は、薬の体内動態にも影響を及ぼすため、投薬時間をうまく調節することで、薬効を最大にし、副作用を軽減させる可能性があります。例えば、がんの治療において、免疫化学療法を日中早期に行う方が、日中後期に行う場合に比べて、より有効性を向上させるのではないかと経験的に言われてきました。しかしながら、これらの考えは、厳密に証明された訳ではありません。この様な状況で、中国湖南省・中南大学のZhe Huang博士らは、ステージIIIC-IVの肺がん患者さん(n=210)の免疫チェックポイント阻害薬投与による点滴治療において、投与時刻によって効果が異なるかどうかを調べるための前向き無作為化対照試験(第3相臨床試験)を行いました。その結果、午後15:00時以前に最初の4サイクルの治療を終えたグループは、午後15:00以降に治療を開始したグループに比べて、生存期間が延長することがわかりました。さらに、この抗腫瘍効果は、細胞傷害性T細胞の特性の増強と関連しており、少なくとも一つのメカニズムとして、免疫力の活性化が重要かも知れないと推測されました。これらの結果は、がん免疫化学療法において、時間帯による治療の重要性を証明するものであり、最近のNature Medicine誌に掲載されましたので、今回は、この論文(文献1)を報告いたします。一般的に、がん免疫療法の副作用は少ないとされますが、まったく無いと言うわけではないでしょう。したがって、投与した直後の様子をフォローする必要があるという意味でも、早い時間帯に治療を開始することが推奨されます。
文献1.
Time-of-day immunochemotherapy in non-small cell lung cancer: a randomized phase 3 trial., Huang Z et al. Nat Med. 2026 Feb 2. Online ahead of print.
これまでの研究により、がんの免疫化学療法は、日中早期に投与開始することで、より治療の有効性が期待できるのではないかと示唆されていた。本プロジェクトでは、これを前向き無作為化対照試験で検討することを研究目的とした。
これを証明するため、ランダム化肺タイム-C01試験(ClinicalTrials.gov NCT05549037; 第3相臨床試験)を実施した。すなわち、ドライバー変異*5を持たない(分子標的治療の適応とならない)ステージIIIC-IV非小細胞肺がんの患者さん (n=210)が、早期時間帯治療、または、後期時間帯治療の群に1:1の比でランダムに割り付けられた(それぞれ、n=105)。2つの群は、15時以前、あるいは、以降に、抗PD-1剤(免疫チェックポイント阻害薬)の最初の4サイクルを投与することで定義された。主要評価項目はPFSであり、二次評価項目にはOSが含まれていた。
以上から、早期時間帯治療群では、後期時間帯治療群と比較して、免疫化学療法はPFSおよびOSを実質的に改善した。これは、CD8+T細胞特性の増強と関連していることが示された。