医学・生命科学全般に関する最新情報


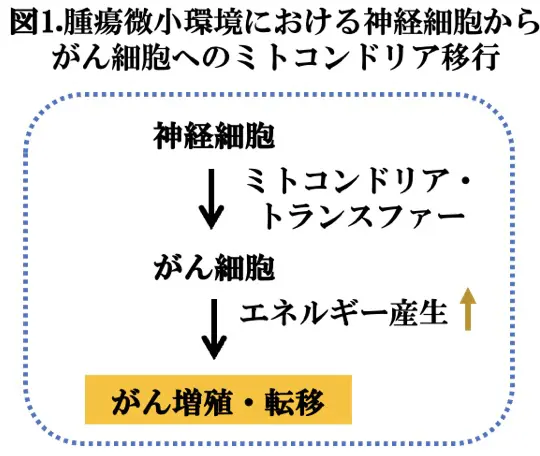
近年、がんの研究分野で注目されていることの一つに腫瘍微小環境(TME)*3におけるがん細胞と周囲の細胞との相互作用(図1)があります。すなわち、がん細胞は独自に増殖、進展するのではなく、周囲のマクロファージなどの免疫細胞や血管新生やがんの増殖を促進する線維芽細胞など多くの細胞が関与することがわかってきました。これに関連して、TMEに神経細胞が多く存在するほど、がん細胞の増殖性が強くなることから、神経細胞が腫瘍の代謝促進に働いている可能性が指摘されていましたが、具体的なメカニズムは、はっきりしませんでした。この様な状況で、米国・サウスアラバマ大学のGregory Hoober博士と共同研究者は、がんの転移はがんの多くの機能の中でも、特に、莫大なエネルギー(ATP)を必要とする過程であることから、神経細胞が転移時に腫瘍のエネルギーを著しく改善するのではないかと考えました。この仮説を乳がんの神経遮断モデル、神経細胞と癌細胞の共培養モデルにおいて確認しました。さらに、著者らは、ミトコンドリア転移のレポーターであるMito TRACERを開発し、ミトコンドリアが移行したがん細胞の転移部位における選択的濃縮が広がったことが明らかになりました。これらの結果は、TME内の神経細胞からミトコンドリアを受け取ることにより、がん細胞の転移能力が強化されることを示唆するものであり、昨年のNature誌に掲載されましたので、今回は、この論文(文献1)を報告いたします。がんの転移の予防は、がんの治療における核心的な部分ですが、治療法はありません。もし、神経細胞よりのミトコンドリア・トランスファーが治療標的になれば、大きな進歩と言えるでしょう。
文献1.
Nerve-to-cancer transfer of mitochondria during cancer metastasis., Hoober G et al. Nature 644, pages 252–262 (2025)
神経系はがん生物学において極めて重要な役割を果たしており、これまでの研究により腫瘍内神経密度とがん転移との関連が示されている。神経へのがん依存が強くなっていることが指摘されてきたが、神経媒介性がんの進行を促進する根本的なメカニズムについては、十分に理解されていない。本プロジェクトでは、これをミトコンドリア・トランスファーに焦点を当てて検討することを研究目的とした。
以上の結果は、原発腫瘍内の神経細胞からミトコンドリアを受け取るがん細胞の転移能力の強化を示唆するものであり、神経系が「エネルギー供給者として」がんの代謝や転移をサポートしているという新たな知見を提供する。