※世界各国で行われている研究成果をご紹介しています。研究成果に対する評価や意見は執筆者の意見です。
一般向け
研究者向け
2024/9/5
パーキンソン病の治療研究;
G2019S LRRK2キナーゼ阻害剤によるミトコンドリアDNA損傷の回復
文責:橋本 款
今回の論文のポイント
- LRRK2遺伝子の変異は家族性パーキンソン病(PARK8)*1の原因になる。これまでの研究では、LRRK2の活性化の亢進が病態に関係することが示されており、LRRK2を阻害することが治療に結びつくと考えられている。
- 本研究では、G2019S LRRK2(最も高頻度の遺伝子変異体)の選択的阻害剤*2であるEB-42168は、細胞レベルでLRRK2のリン酸化を抑制し、ミトコンドリアDNA損傷を有意に回復することが示された。さらに、この効果は、可逆的に認められた。
- これらの結果から、ミトコンドリアDNAの損傷の薬理学的な動態は、LRRK2キナーゼの変化を示すバイオマーカーとして有用であると推定する。
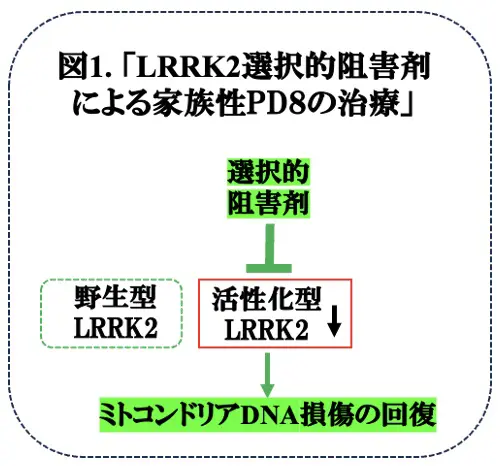
現在、パーキンソン病(PD)においては、モノクローナル抗体(Mab)による受動免疫(モノクローナル抗体Prasinezumabを用いたパーキンソン病の免疫療法〈2024/8/20掲載〉)だけでなく、いくつかの臨床試験が行われていますが、今週はLRRK2阻害剤に焦点を当てたいと思います。LRRK2遺伝子の変異は家族性PD(PARK8)の原因であり、これまでに報告された家族性PDの原因遺伝子のうち、最も高頻度に認められます。また、興味深いことに、LRRK2遺伝子変異を有するPD患者さんには、孤発性PD患者さんと臨床症状が類似しており、LRRK2のリン酸化による活性化が亢進しています(図1)。したがって、LRRK2遺伝子変異による神経変性機構を解析することは、PDの病態解明、及び、治療に結びつく可能性があり、特に、LRRK2の活性を抑制することが治療に結びつくと予想されることから、LRRK2を阻害する化合物の開発、臨床試験が試みられています。
この様な状況で、米国・デューク大学のNicholas Pena博士らは、LRRK2 の遺伝子変異による家族性PD8型は常染色体優性のため、ヘテロ接合性LRRK2の正常機能を維持することが重要と考え、最も高頻度で見られる変異であるG2019S LRRK2キナーゼに対する選択的阻害剤をLRRK2細胞モデルに投与したところ、非選択的阻害剤に比べて、ミトコンドリアDNA損傷の回復が有意に観察されました。この結果は、LRRK2阻害剤によるPDの治療開発に意義深いものであり、npj Parkinson’s disease誌に掲載されましたので(文献1)、今回はそれを紹介いたします。
文献1.
G2019S selective LRRK2 kinase inhibitor abrogates mitochondrial DNA damage, Nicholas Pena et al., npj Parkinson’s disease volume 10, Article number: 49 (2024)
【背景・目的】
- 最近、我々は、G2019S変異型LRRK2キナーゼは、ミトコンドリアDNAの損傷に関与しており、LRRK2を脱リン酸化する阻害剤により、家族性PD8型患者由来細胞のミトコンドリアDNAの損傷は健康な対象者レベル由来細胞まで回復することを見出していた(Sci Transl Med 2023)。
- 家族性PD8型は、常染色優性であり、変異型(G2019Sなど)と野生型のLRRK2キナーゼをコードした遺伝子のヘテロ接合である。したがって、変異型LRRK2キナーゼを選択的に阻害することが治療に有効であると考えられる。この仮説を証明するため、G2019S LRRK2選択的阻害剤が、LRRK2非選択的阻害剤に比べて、ミトコンドリアDNAの損傷回復作用が大きいことを示すことを本プロジェクトの研究目的とした。
【方法】
この目的のため、G2019S LRRK2を発現したHEK293細胞モデル、家族性PD8型の患者さん(及び、健常者コントロール)由来のリンパ芽球細胞を用いて、G2019S LRRK2選択的阻害剤:EB-42168、とLRRK2非選択的阻害剤:MLi-2の効果をLRRK2 の抗リン酸化抗体(Ser935 and/or Ser1292)による定量的ウェスタンブロット、ミトコンドリアDNAの損傷アッセイ*3により解析した。
【結果】
- EB-42168は、野生型LRRK2に比べ、G2019S LRRK2のリン酸化を選択的に阻害した。一方、MLi-2は野生型、及び、G2019S LRRKのリン酸化を同等に阻害した。
- EB-42168による急性期治療は、選択的リン酸化阻害作用と同じタイムフレームでG2019S LRRK2によるミトコンドリアDNAの損傷をコントロールの細胞レベルまで回復させた。
- LRRK2阻害剤を、洗い流して2時間以内のミトコンドリアDNAの損傷は可逆的であった(元通りまで憎悪した)ことから、ミトコンドリアDNAの損傷は非常に動的な現象であると考えられた。
- このタイムフレームでG2019S LRRKのミトファジーは緩和されなかったことから、ミトファジーはミトコンドリアDNAの損傷に影響しないと推定された。
【結論】
- G2019S LRRK2選択的阻害剤EB-42168により、ミトコンドリアDNAの損傷が抑制されたことは、これが、G2019S LRRK2のPD患者さんに対するプレシジョンメディシン*4になるかも知れない。
- また、ミトコンドリアDNAの損傷の薬理学的な動態は、低分子量化合物開発の臨床試験でLRRK2キナーゼの変化に対するバイオマーカーとして有用である可能性を示唆している。
用語の解説
- *1.PARK8
- PARK8はわが国で見いだされた常染色体優性遺伝様式のPDで、発症年齢、PDの4主徴候(振戦、筋固縮、無動・寡動、姿勢反射障害)、薬物の効果などの臨床像は孤発性PDと極めて類似している。また、PARK8が遺伝性パーキンソニズムの中でも特に頻度が高い。また、病因遺伝子であるLRRK2が遺伝子配列から多彩な機能を示すタンパク質であり、孤発性PDの病因解明への手掛かりとなる可能性が示唆される。
- *2. LRRK2 阻害剤
- LRRK2 (Leucine-rich repeat kinase 2) は、セリン-スレオニン (Ser/Thr)プロテインキナーゼ活性と自己リン酸活性を有する2527個のアミノ酸残基からなる巨大タンパク質であり、多くの哺乳動物組織でその発現が確認されている。そのLRRK2のG2019Sをコードする部分の遺伝子変異が、PD患者さんに高い頻度で検出されている。このことから、近年ではLRRK2を標的とした阻害剤 (特にG2019S変異型選択的な阻害剤)が家族性PD治療薬としてだけでなく、LRRK2の機能を調べるための有用なツールとしても注目されている。
- *3.ミトコンドリアDNA損傷アッセイ(Mito DNADX assay)
- 2023/10/29 -Duke Health研究チームが開発した新しい血液検査で、末梢血を材料にしたPCRによりPDにおけるミトコンドリアDNA損傷のバイオマーカーとして利用できる(Science Translational Medicine, 2023)。
- *4.プレシジョンメディシン(Precision Medicine)
- プレシジョンという言葉には、「精密」、「正確」、「的確」などの意味があり、「プレシジョン・メディシン」は「精密医療」と訳されることが多い。「それぞれの患者に合った最適な治療を行う医療」のことで、がんの患者さんだけでなく、あらゆる病気の患者が対象とされる。例えば、がんの領域では、がん細胞の遺伝子を次世代シークエンサーで解析し、がんの原因となった遺伝子変異を見つけ、その遺伝子変異に効果があるように設計した分子標的薬を使用するといった手法が用いられ、テーラーメード医療や個別化医療の一種とされる。
- 文献1
- G2019S selective LRRK2 kinase inhibitor abrogates mitochondrial DNA damage, Nicholas Pena et al., npj Parkinson’s disease volume 10, Article number: 49 (2024)