当研究所幹細胞プロジェクトの原孝彦参事研究員と鈴木輝彦主席研究員らは、押村光雄博士(株式会社Trans Chromosomics・代表取締役)、香月康宏准教授(鳥取大学)らと共同で、「コンディショナルノックアウト細胞をワンステップで高効率に作製する技術」を開発し、英科学誌Nucleic Acids Researchに発表しました。本研究は、日本学術振興会科研費及びJST-CREST(JPMJCR18S4)の支援を受け実施しました。

2020年のノーベル化学賞にも選ばれたCRISPR/Cas9(クリスパー/キャス9)によるゲノム編集技術は標的遺伝子を簡単に破壊することが可能であるため、疾病に関わる遺伝子などの分子機能を解析する上でとても重要な技術となっています。しかし標的とする遺伝子が細胞の生存に必須な機能を持つ場合は遺伝子を壊すと細胞が死んでしまうため、遺伝子破壊細胞をクローニングして分子機能を解析することができません。このような場合には組換え酵素の認識配列で標的遺伝子を挟み、解析を行う際に組換え酵素を発現させて遺伝子を破壊するコンディショナルノックアウト(cKO)法が利用されます。しかし、従来のcKO細胞作製法ではクローニング操作を4回も繰り返さなければならないため、研究資材の準備に多くの時間と労力が必要になるという問題がありました。
そこで私達は一度のクローニング操作で標的遺伝子をcKOすると同時に、標的遺伝子にタグを付加し、さらにその発現を緑色蛍光タンパク質EGFPで検出することができるAll-in-one cKO法を開発しました(図1)。本手法を用いて私達が研究を行っている必須遺伝子Ddx1のcKO マウス胚性幹細胞(ESC)を作製したところ、DDX1にはFLAGタグが付加されており、その発現をEGFPで検出することができました。またこのDdx1cKO ESCに組換え酵素FLPと変異エストロゲン受容体ERT2を融合させたFLP-ERT2を発現させたところ、タモキシフェン依存的にEGFPの発現が消失し、DDX1タンパク質の発現もなくなることが確認できました。次にDdx1cKO ESCを利用してDDX1の分子機能を解析したところ、Ddx1が欠損するとリボソームRNAのプロセッシングが正常に進行せず、核小体ストレス経路を介してがん抑制遺伝子p53が活性化されてアポトーシスが誘導されることが分かりました。
図1
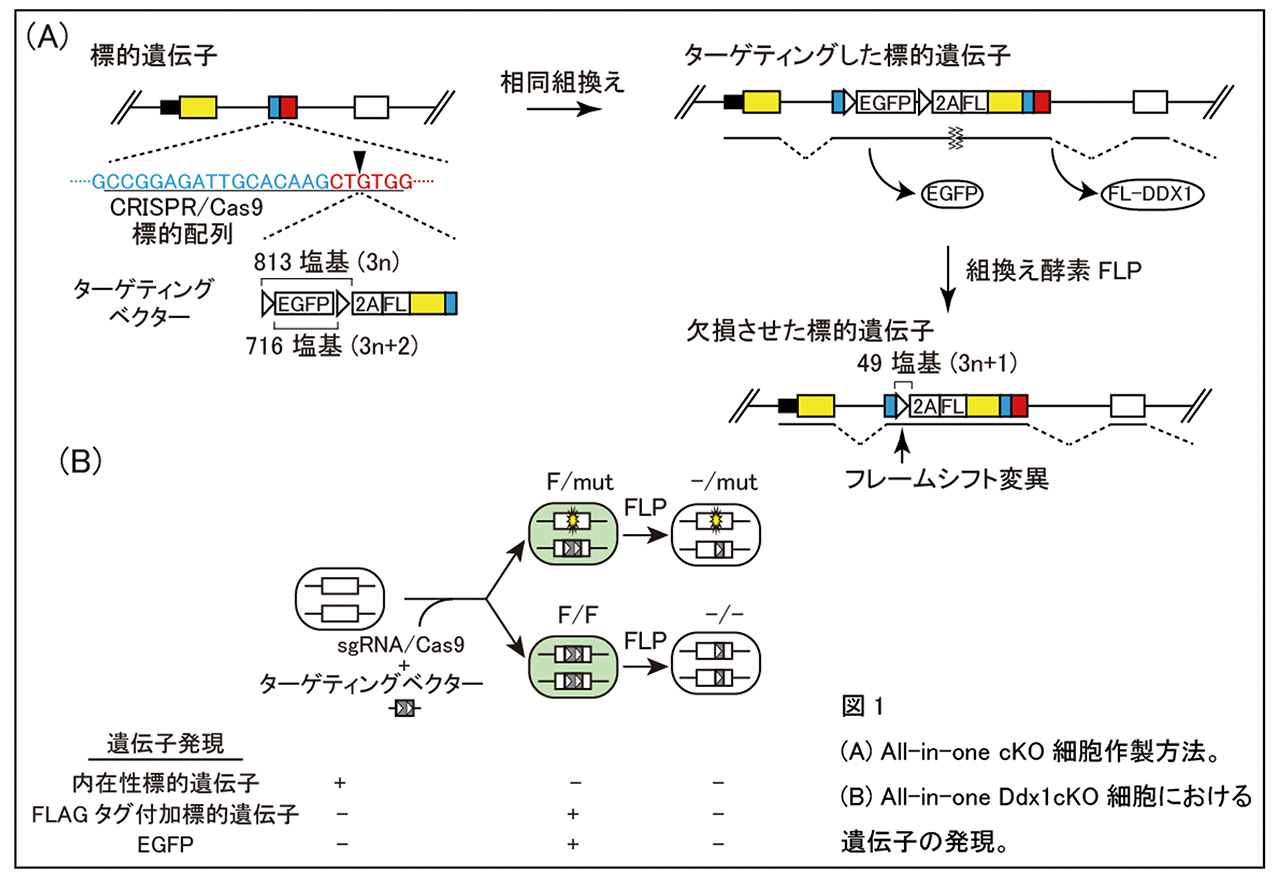
All-in-one cKO法はDdx1以外の様々な遺伝子のcKO細胞も簡便に調製することが可能で、EGFPの発現を指標にクローニングすればESCだけでなく通常の培養細胞株でも63〜96%の効率でcKO細胞を単離することができました(表1)。これまでに報告されているcKO細胞作製法の効率はおよそ5%であることからAll-in-one cKO法は非常に効率のよい技術であり、今後様々な遺伝子の分子機能解析に貢献する技術になると期待されます。

これまでの研究からDDX1はがんの発症やウイルス感染に寄与していることが示唆されています。Ddx1cKO細胞を用いてこれら疾病の発症にどのようにDDX1が寄与しているのかを明らかにしていくことができれば、新たな疾患治療法の開発にも貢献できると期待されます。