分子医療プロジェクトの入江敦主任研究員(現カルパインプロジェクト)、芝崎太参事研究員(現病院等連携支援センター 客員研究員)は、東京理科大学・薬学部 和田猛教授のグループとの共同研究で、和田研究室が開発した人工オリゴ糖(*1)化合物とホスホロチオエート修飾(*2)RNAを組み合わせることにより、siRNA(*3)を顕著に安定化する手法を発見しました。本研究成果は、siRNA医薬品開発への応用が期待されます。
本研究成果は、2020年9月9日(水曜日)10時(英国標準時)に英国科学誌「Scientific Reports」にオンライン掲載されました。

現在実用化されている医薬品の多くは、体の中で病気の原因となっている分子の働きを阻害することによって、治療効果を発揮します。しかし、体内には既存の医薬品によって働きを抑えることができない分子が沢山あり、未だに治療が難しい病気が多く存在します。人工的に合成した核酸RNAの一種であるsiRNAは、生体内に取り込まれると任意のタンパク質の産生を抑制する(遺伝子発現を抑制する)ように設計することができます。そこで、今までの医薬品には果たすことができなかった、多くの病気の原因分子の産生をブロックすることが期待でき、新しい医薬品として開発が進められています。
しかし、siRNAは体内でRNA分解タンパク質(リボヌクレアーゼ: RNase)によって簡単に分解されやすい性質を持ち、siRNA医薬品の実用化の障害となっています。このsiRNAの欠点を克服するために、現在まで、様々な化学的に分子構造に改良を施した(化学修飾した)siRNAが開発されています。しかし、siRNAに化学修飾を加えても、まだなおリボヌクレアーゼにより分解されやすく、さらに化学修飾によりsiRNAの遺伝子発現抑制作用が減弱してしまう、大量に投与すると体内で毒性がある、といった欠点があり、さらなる改良が望まれています。
siRNA分子は、相補的な塩基からなる2本のRNA鎖によって構成されており、DNA二重鎖と同様に、らせん状の形をした「二重らせん構造」となっています。共同研究者の和田教授らのグループは、RNA二重らせんに特異的に結合し、RNA二重鎖構造を安定化することによってsiRNAの分解を防ぐ化合物を幾つか開発し、それらの中でも、カチオン性(プラスの電荷を帯びた)オリゴアミノ糖からなる人工化合物・オリゴジアミノガラクトース4量体(ODAGal4)が、特に強くRNA二重鎖に結合することを見出しました。
和田教授らのグループと私達の研究グループは共同で、ODAGal4が数多くの種類のsiRNAの二重らせん構造を安定化し、リボヌクレアーゼによる分解を防ぐことを見出しました。次に、修飾型核酸の一種であるホスホロチオエート修飾を施したsiRNAとODAGal4を組み合わせると、飛躍的にリボヌクレアーゼによる分解が抑制されることが明らかとなり、その効果は、既存の修飾型核酸によるsiRNA分解抑制効果を上回るものでした。さらに、ODAGal4とホスホロチオエート修飾型siRNAの組み合わせは、いろいろな種類のsiRNAの遺伝子発現抑制活性にほとんど影響を及ぼしませんでした。また、ODAGal4とホスホロチオエート修飾型siRNAは、細胞内に取り込まれても毒性を示しませんでした。
本研究から、ODAGal4とホスホロチオエート修飾RNAを組み合わせることにより、今まで知られていた修飾型核酸によるsiRNA安定化効果を上回る、高い安定化効果を発揮できることが明らかとなりました。また、修飾型核酸の欠点であるsiRNA遺伝子発現抑制活性の阻害や、細胞毒性を示さないことも特徴として挙げられます。
今後この研究成果を足がかりとして、ODAGal4とホスホロチオエート修飾の組み合わせによるsiRNA安定化の研究がさらに発展すれば、将来的にはsiRNA医薬品開発に適応でき、より安定性の高いsiRNA医薬品の製造につながる可能性があります。
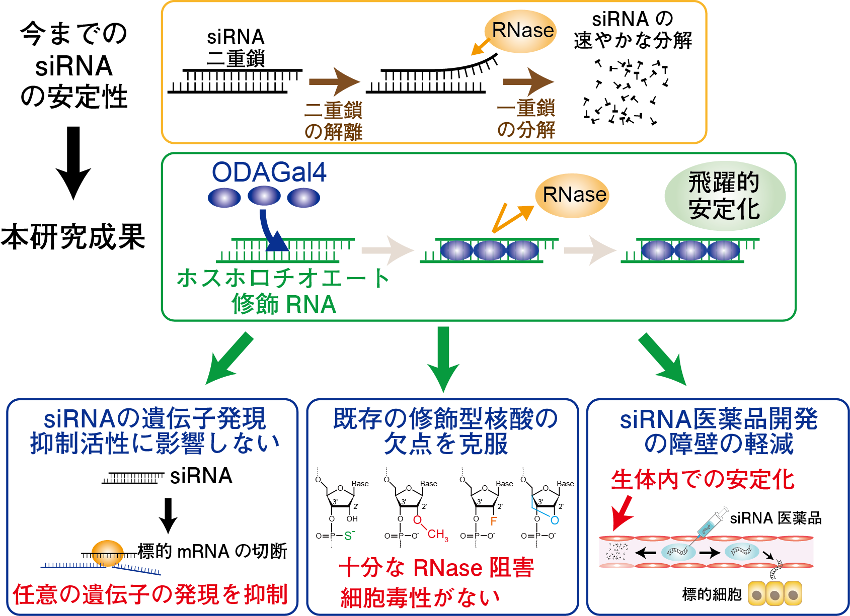
ODAGal4はsiRNAを効果的に安定化し、特にホスホロチオエート修飾RNAを飛躍的に安定化する。