カルパイングループ 主席研究員 久恒 智博
カルパインプロジェクトリーダー(当時) 小野 弥子
当研究所カルパイングループの久恒智博主席研究員、小野弥子プロジェクトリーダー(当時)らは、肢帯型筋ジストロフィーR1(LGMDR1)の責任遺伝子産物“カルパイン3”の筋細胞における動態の解明とその基質の同定に成功しました。
本研究成果は、4月23日付け発行の米国科学雑誌「Journal of Biological Chemistry」のオンライン版に掲載されました。
「肢帯型筋ジストロフィー R1」は、およそ 10 万人に約2人という割合で発症する希少な病気です。患者さんの多くは思春期以降に筋肉の力が徐々に低下し、30 歳前後で車椅子が必要になることもあります。現在のところ、根本的な治療法は見つかっていません。
この病気の原因は、「カルパイン3」というタンパク質がうまく働かないことだと分かっていました。カルパイン3は、他のタンパク質を分解する「プロテアーゼ」という酵素の一種です。しかし、このカルパイン3が「筋肉の中でいつ、どこで、どのように活性化し、一体何を分解しているのか」という肝心な部分が、これまで詳しく分かっていませんでした。この「いつ、どこで、何を」という謎を解くことが、病気のメカニズム解明の鍵だったのです。
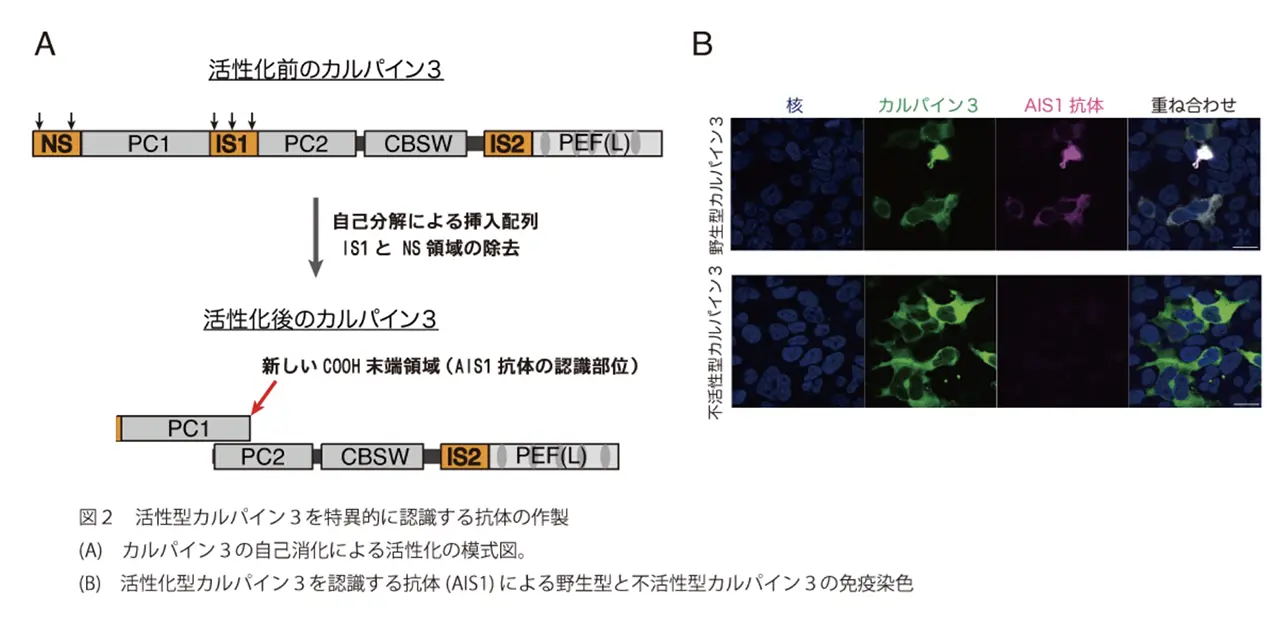
研究グループは、カルパイン3が活性化するときに起こる「自己消化」という現象に注目しました。
カルパイン3が活性化して自己消化を起こすと、その形が少しだけ変化します。研究チームは、この「変化したカルパイン3」だけを特異的に見つけ出す新しい抗体(AIS1 抗体)の開発に世界で初めて成功しました。これにより、今まで難しかったカルパイン3が筋肉の細胞の中で「いつ、どこで、活性化しているのか」を直接観察できるようになったのです。
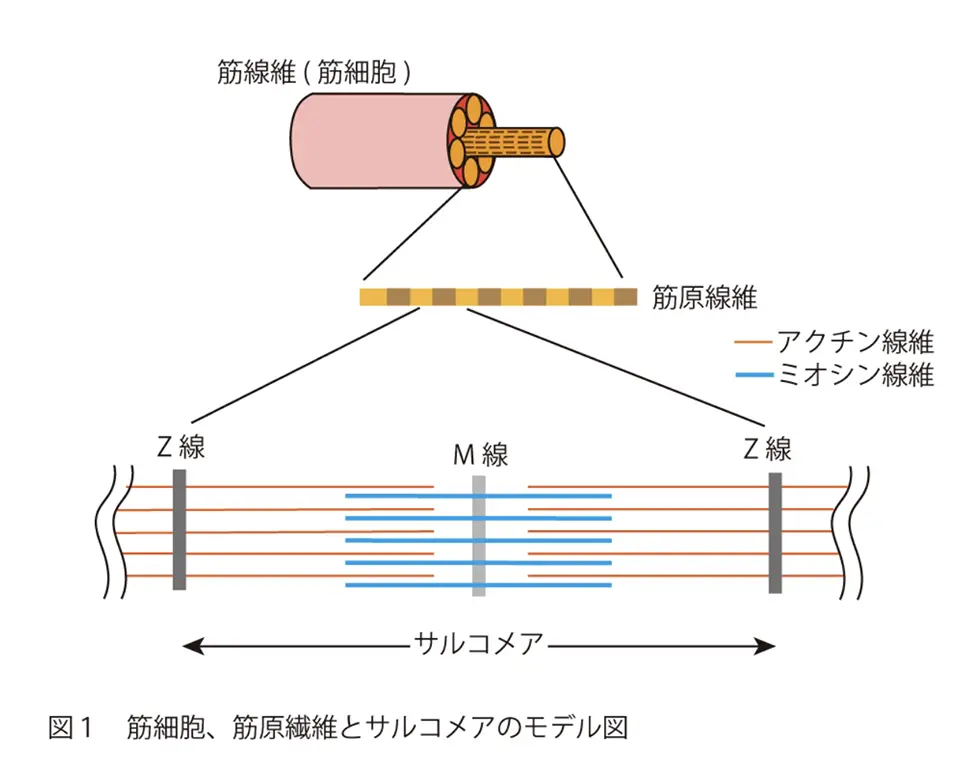
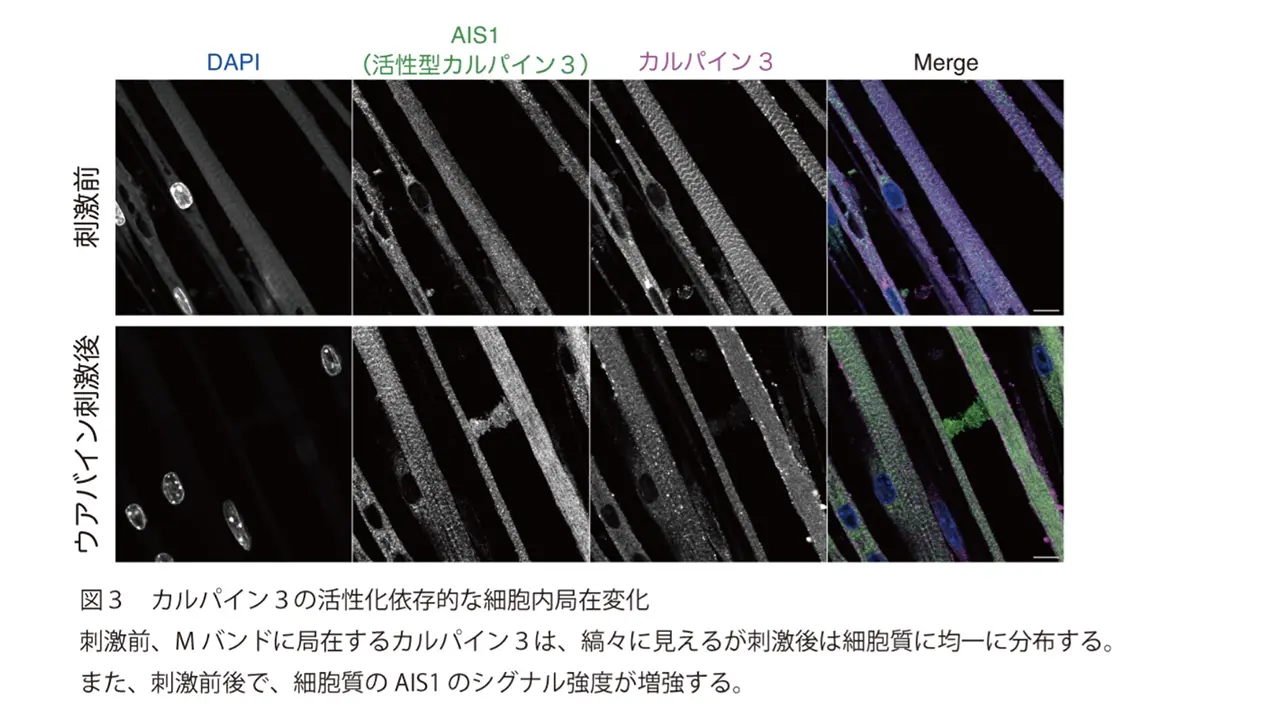
この新しい抗体を使って調べた結果、普段、筋細胞の特定の場所(サルコメアの M バンドという筋収縮で重要な役割を果たす部位)にいるカルパイン3が、ごくわずかなカルシウム濃度の変化が引き金となって活性化し、そこから細胞内全体(細胞質)へ移動することが分かりました。そして、カルパイン3の「自己消化」がこの局在変化に欠かせないことも判明しました。
さらに研究を進めた結果、活性化したカルパイン3が細胞質に移動した後、「スペクトリン」と「タリン」という2つのタンパク質を分解していることを突き止めました。これらは筋肉の形を保つ「細胞の骨組み(細胞骨格)」に関わる重要なタンパク質です。つまり、カルパイン3が正常に働かないと、これらの骨組みの分解・再構築が適切に始まらず、筋肉の機能に異常が生じると考えられます。
今回の研究で、カルパイン3が筋肉の中でどのように活性化し、どこに移動して、何を分解するのかという、これまで不明だった「動き」と「役割」が具体的に明らかになりました。カルパイン3の活性化には微少かつ継続的なカルシウム濃度の増加が必要であり、このようなカルシウム動態は筋収縮とも密接に関連しています。また、「スペクトリン」や「タリン」の不適切な分解が、この病気(LGMDR1)の発症メカニズムの一部となっている可能性が強く示唆されました。
これらの発見は、「肢帯型筋ジストロフィー R1」の根本的な原因を理解する上で非常に重要な手がかりとなります。今後は、今回明らかになったカルパイン3の活性化の仕組みや、分解する相手(基質)に関する知見をさらに深めることで、病気の進行を止める、あるいは筋機能を回復させるような新しい治療法や薬剤の開発につながると期待されます。