ゲノム医学研究センター 主任研究員 齊藤 紗希
センター長 川路 英哉
ゲノム医学研究センターの齊藤紗希 主任研究員、川路英哉 センター長らの研究グループは、ヒト肝細胞を用いて、薬の副作用メカニズムに関連する新たなエンハンサーを同定し、その機能を明らかにしました。
この研究成果は、2025年4月29日(火)18時(日本時間)に科学誌 Nature Communications オンライン版に掲載されました。
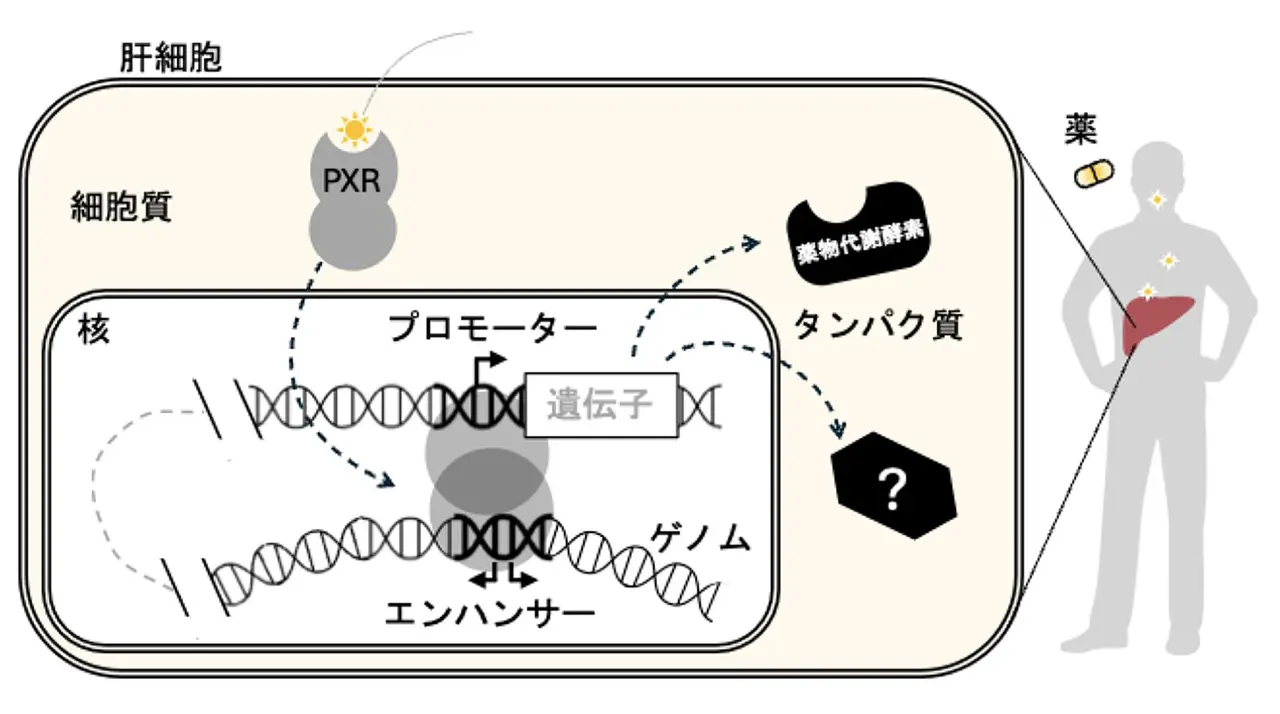
薬の効果や副作用の発現における個人差には遺伝要因が深く関与しており、これまでタンパク質をコードする領域の遺伝子多型と薬剤応答性の関係に着目した研究が実施されてきました。しかし近年、体質や疾患に関わる一塩基多型の多くが、タンパク質をコードしない遺伝子発現制御領域 (シス制御エレメント) に集積していることが明らかになり、遺伝子発現のオン・オフを行うスイッチとして働くエンハンサーに大きな注目が集まっています。肝臓では、薬剤応答性転写因子 PXR がシス制御エレメントに結合し、薬物代謝酵素などの遺伝子発現を調節することが知られているものの(図1)、ゲノム全体の中で PXR が認識する部位の全体像は不明でした。今回、我々は PXR が制御する新しいエンハンサーの同定を通じて、薬の効果や副作用の発現に関わる分子メカニズムの一端を明らかにしました。
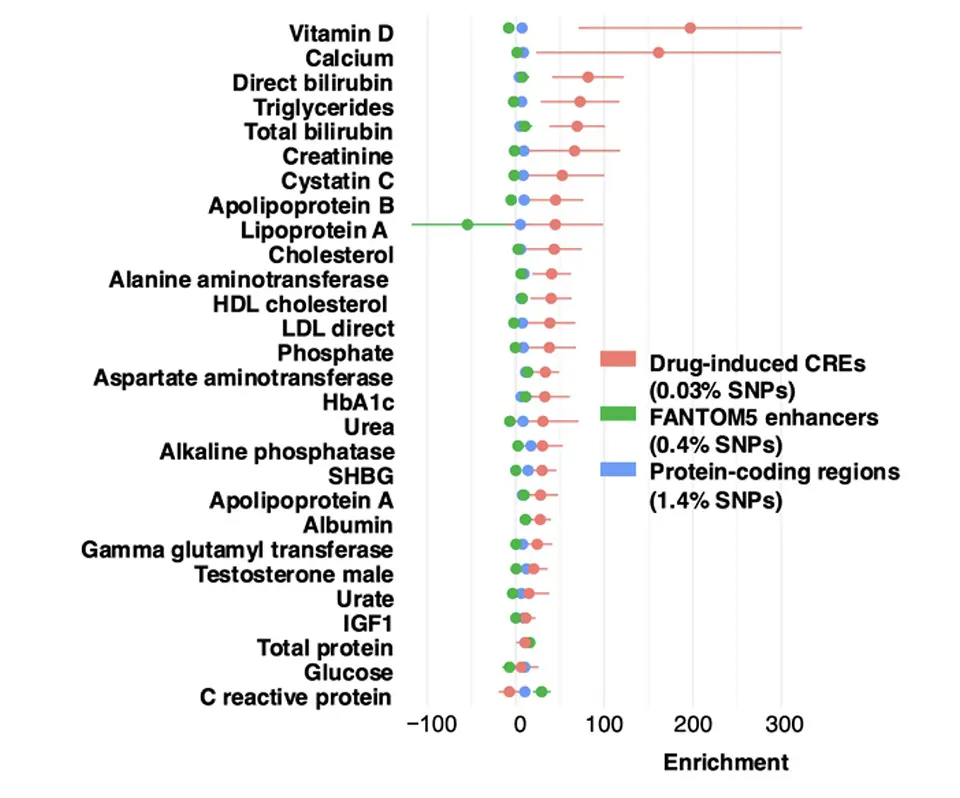
ヒト肝細胞モデルに転写活性の網羅的定量法を適用し、薬剤によって誘導されるシス制御エレメント候補を網羅的に同定しました。同定されたエレメントには、生体内ビタミンD 濃度に関する表現型と相関する一塩基多型が顕著に集積しており(図2)、特に活性型ビタミンD の不活性化酵素である CYP24A1 遺伝子の近傍にある機能不明な領域が含まれていました。機能解析の結果、この領域がCYP24A1 遺伝子のエンハンサーとして機能し、その発現を左右する一塩基多型がこの中に含まれることを特定しました。さらに、これまでビタミンD 代謝の研究において全く着目されていなかった TSKU 遺伝子が、ビタミンD 代謝に関連する遺伝子群の発現に影響を与えること、および TSKU 遺伝子の発現を薬剤誘導的に増加させる新規エンハンサーの存在も明らかにしました。一部の薬剤では副作用としてビタミンD 欠乏症が報告されていますが、本研究の結果はその分子的機序を初めて示唆する知見となります。
UGT1A1 遺伝子はイリノテカンなどの抗がん剤の代謝に関与し、それらの副作用と密接に関連することが知られています。本研究で同定した薬剤誘導性のシス制御エレメント中から、UGT1A1 遺伝子の発現を増加させる2カ所の新規エンハンサーを突き止めました。さらに、これらのエンハンサー内に UGT1A1 遺伝子の発現を左右する一塩基多型が存在することを明らかにしました。この研究結果は、特定の抗がん剤の副作用リスクの予測や、患者ごとに最適化された抗がん剤治療の実現に寄与するものと期待されます。
本研究により、薬剤応答性に関わるシス制御エレメントと、薬の副作用発現に関わる分子メカニズムの一端が明らかになりました。薬の効果や副作用発現の個人差を予見し、適切に制御することは、最適な治療計画を立てる上で極めて重要です。本成果は、このような個人差を分子レベルで正確に把握するための手掛かりを提供し、個別化医療の高度化へ向けた基盤となることが期待されます。また、ヒトゲノムの 98 〜 99% を占める非コード領域の役割は、未だ十分に解明されていません。今回の研究で確立した方法論を適用することで、この非コード領域を含めたヒトゲノム全体の機能的理解が一層進むことが期待されます。