HOME > 広報活動 > 刊行物 > October 2014 No.015

October 2014 No.015
特集
研究紹介
開催報告
お知らせ・編集後記
研究紹介
脂肪細胞から分泌される脂質代謝酵素による肥満の新しい調節機構の発見
米国科学誌「Cell Metabolism」に脂質代謝プロジェクトリーダーの村上誠参事研究員、佐藤弘泰研究員、武富芳隆研究員らの研究成果が発表されました。
脂質代謝プロジェクト 研究員佐藤 弘泰
世界的に問題となっているメタボリックシンドロームの病態基盤であるインスリン抵抗性※1は肥満に伴うことが多く、組織内に脂質が過剰に蓄積されると脂肪毒性が生じ、小胞体ストレス※2や慢性炎症を引き起こしインスリン抵抗性の要因となります。細胞内外における脂質代謝の異常は肥満・高脂血症・インスリン抵抗性などの病態に密接に関与していますが、その全体像は十分には理解されていません。
今回我々は、肥満により発現誘導される2種類の脂質代謝酵素(分泌性ホスホリパーゼA2)※3「PLA2G5」と「PLA2G2E」を見つけ、更にそれぞれの酵素を欠損させたマウスの解析を通じて、この2種の酵素が全身の代謝制御に関わる「メタボリック分泌性ホスホリパーゼA2」として機能することを発見しました。(図)
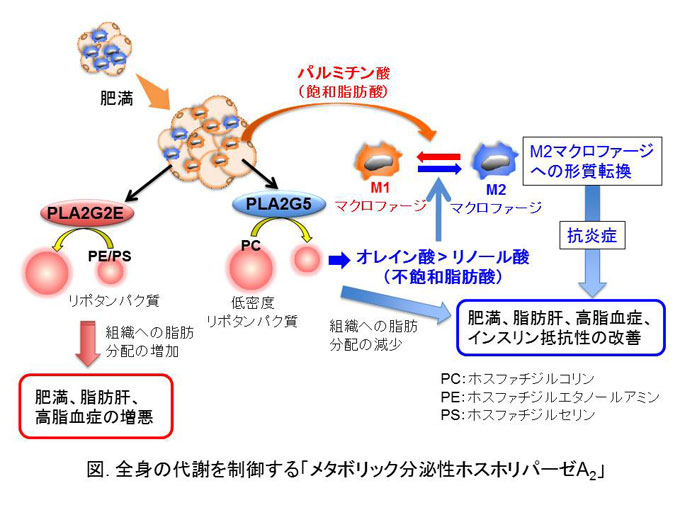
高脂肪食を与えたPLA2G5欠損マウスでは脂肪組織において対照マウスよりも脂肪の蓄積が進行し症状が悪化しました。PLA2G5の作用を解明するためにリピドミクス (脂質の網羅解析) により分析を行うと、脂肪細胞から分泌されたPLA2G5は血漿LDL※4中のリン脂質に作用し、オレイン酸、リノール酸などの不飽和脂肪酸を遊離させました。更にこの不飽和脂肪酸は、飽和脂肪酸(パルミチン酸)による炎症を促進するM1マクロファージ※5の誘導に拮抗し、炎症を抑えるM2マクロファージ※6を優位にさせることを突き止めました。また、PLA2G5がTh2応答※7を促進させる機能をもつこともわかりました。一方、高脂肪食を与えたPLA2G2E欠損マウスでは肥満や高脂血症の軽減が見られました。リピドミクス解析により、PLA2G2Eはリポタンパク質中に存在するPLA2G5の標的リン脂質とは別の種類の微量リン脂質を分解していることが判明しました。
以上より、PLA2G5はリポタンパク質の主要なリン脂質から不飽和脂肪酸を分離し、肥満に伴う慢性炎症を抑制する役割を持ち、一方、PLA2G2Eはリポタンパク質の微量リン脂質の量を調節することで脂肪組織や肝臓への脂質の運搬・貯蔵を促進することが明らかとなりました。本研究は、同一細胞より分泌される2種の分泌性ホスホリパーゼA2の基質特異性の違いが異なる影響を及ぼすことを同一の病態条件で示した初めての成果であると同時に、分泌性ホスホリパーゼA2によるリポタンパク質の代謝の生理的意義の初めての解明、肥満の新しい制御機構の発見など、脂質生物学および代謝の研究領域に新しい概念を導入するものです。
内臓脂肪組織における分泌性ホスホリパーゼA2の量や不飽和脂肪酸の量は新しい肥満の診断マーカーとなる可能性があります。また分泌性ホスホリパーゼA2を標的とした創薬は、新しいメタボリックシンドロームの予防と治療法の開発に繋がることが期待されます。
- ※1 インスリン抵抗性:
- 受容体やシグナル伝達系の異常などによりインスリンの血糖値低下作用が効きにくい状態。
- ※2 小胞体ストレス:
- 細胞内に網目状に連なる膜性の袋状器官(小胞体)に異常なタンパク質等が蓄積され細胞に悪影響を与える。
- ※3 分泌性ホスホリパーゼA2:
- リン脂質を分解して脂肪酸を遊離させる酵素の一群。
- ※4 LDL:
- 低比重リポタンパク質。中性脂肪およびコレステロールを運搬する血漿中の粒子。
- ※5 M1マクロファージ:
- 肥満において脂肪組織で増加する免疫細胞(マクロファージ)の一集団で脂肪組織の慢性炎症を増悪する役割をもつ。
- ※6 M2マクロファージ:
- 脂肪組織に構成的に存在するマクロファージの一集団で脂肪組織の慢性炎症を抑制する役割をもつ。
- ※7 Th2応答:
- リンパ球の一種であるT細胞のうち、Th2サイトカインと呼ばれるタンパク質を分泌する細胞(Th2細胞)が関わる免疫反応。アレルギー反応の悪化に関わる一方で、抗炎症性のM2マクロファージを誘導することにより肥満や動脈硬化を抑制する。
参考文献
Sato H, Taketomi Y, Ushida A, Isogai Y, Kojima T, Hirabayashi T, Miki Y, Yamamoto K, Nishito Y, Kobayashi T, Ikeda K, Taguchi R, Hara S, Ida S, Miyamoto Y, Watanabe M, Baba H, Miyata K, Oike Y, Gelb MH, Murakami M.
The adipocyte-inducible secreted phospholipases PLA2G5 and PLA2G2E play distinct roles in obesity.
Cell Metab. 20, 119-132 (2014). doi: 10.1016/j.cmet .2014.05.002

