2025年5月23日
幹細胞プロジェクトの種子島 幸祐 主席研究員(現ゲノム動態プロジェクト)、SBIバイオテック株式会社の江指 永二 研究開発部長らは「抗がん活性を持つDNAの作用機序が明らかに〜今後の新しいがん免疫療法のシーズとして期待」についてJournal of Immunology に発表しました。
抗がん活性を持つDNAの作用機序が明らかに
〜今後の新しいがん免疫療法のシーズとして期待
幹細胞プロジェクトの種子島 幸祐 主席研究員(現ゲノム動態プロジェクト)、原 孝彦 プロジェクトリーダー、SBIバイオテック株式会社(以下、SBIバイオテック)の江指 永二 研究開発部長らは、CpG ODN と呼ばれる抗がん活性をもつDNAのがん免疫誘導活性が、CXCL14と呼ばれるケモカインとの相互作用によるものであることを解明しました。
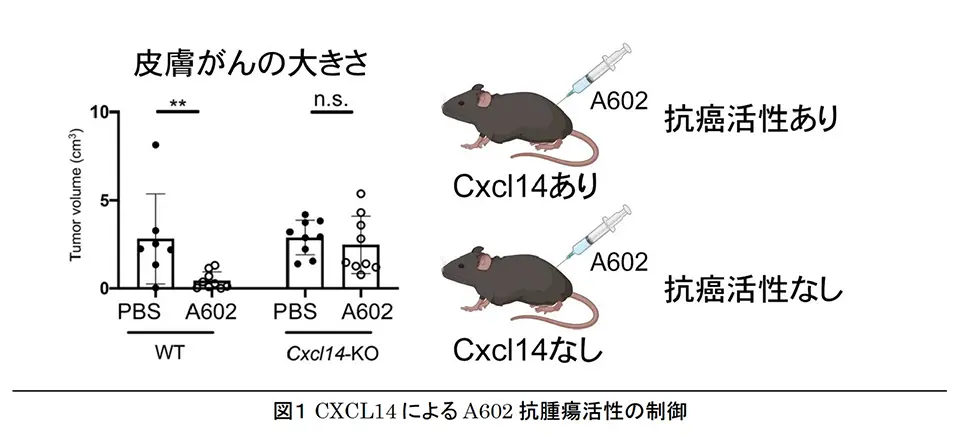
本研究では、これまで免疫増強活性が示されていたCpG ODNと呼ばれるDNA配列を改変し、より強い活性を持つものを探索しました。そこで得られたCpG ODN (A602) はこれまで知られていたCpG ODNが抗癌活性を示しづらかったがん種のマウスモデルにおいても強力な腫瘍抑制効果を示しました。これまで幹細胞プロジェクトでは、ケモカインCXCL14がCpG ODNに結合し、その樹状細胞(注1)への取り込みを介して、自然免疫(注2)の誘導や炎症反応を大幅に増強するという新たな機能を発見していました。そこで、A602の抗腫瘍活性に対するCXCL14の関与を調べたところ、CXCL14はA602による抗腫瘍免疫に関与するサイトカイン誘導を大幅に増強し、Cxcl14-KOマウスではA602の抗腫瘍活性が消失しました。これらの結果は、抗がん活性を持つDNAの新たな作用機序を示すものであり、CpG ODNの抗腫瘍活性が有効な患者の特定や、より強い効果を得る分子メカニズムの解明につながるものと考えられます。この成果は、国際学術誌『Journal of Immunology』(電子版)に日本時間 2025年5月23日に掲載されました。
論文情報
- <論文タイトル>
- “CXCL14 is an essential modulator of TLR9-agonist induced anti-tumor immune responses.”
(CXCL14はTLR9アゴニストが誘導する抗がん免疫反応の必須な制御因子である) - <発表雑誌>
- Journal of Immunology
URL:https://doi.org/10.1093/jimmun/vkaf080
研究の背景
ケモカイン(注3)は細胞の遊走を促進する分泌タンパク質であり、白血球を呼び寄せることで炎症反応などに寄与していることが知られています。このケモカインの一般的な機能に加えて、2017 年に幹細胞プロジェクトの研究により、ケモカインの一種である CXCL14 が CpG DNA(注4)と呼ばれる細菌の DNAに多く含まれる DNA 配列に結合し、その樹状細胞(注1)への取り込みとその細胞内受容体である TLR9の活性化を介して、自然免疫(注2)の誘導や炎症反応を大幅に増強するという新たな機能を発見していました。一方で、この CpG DNA の免疫活性化能に着目して、短い (20-25 bp) 程度の合成 DNA(CpG Oligonucleotide: CpG ODN) を用いて抗腫瘍免疫を誘導する試みがなされていましたが、その効果が不十分であることから、実用化には至っていませんでした。
研究の概要
SBIバイオテックでは CpG ODN の活性を高めるため、それまで分解を防ぐために一般的に行われていたCpG ODNの Phosphorothioate 化(S 化) を改変し、部分的に野生型のリン酸結合に改変した CpG ODNについて活性を検討しました。すると、ある特定の形で S 化を改変した CpG ODN (A602) がヒト樹状細胞およびマウスマクロファージ、樹状細胞に対して高いサイトカイン誘導活性を持つことがわかりました。また、この A602 はマウスの大腸がん、リンパ腫、皮膚がんモデルなど、さまざまながん種への抗腫瘍効果を示しました。本研究所幹細胞プロジェクトの種子島・原らは A602 が CXCL14 と高親和性で結合し、CXCL14が A602 のマクロファージや樹状細胞への取り込みを増強させ、抗腫瘍活性に関連するサイトカインの誘導も大幅に増強させることを見出しました。A602 の抗腫瘍活性と CXCL14 の複合体形成の関連性を調べるため、Cxcl14 をノックアウト (KO) したマウスに皮膚がん細胞(メラノーマ)を移植して抗腫瘍効果を検討しました。すると、Cxcl14-KO マウス (Cxcl14 がないマウス) にメラノーマを移植した際には A602 の抗腫瘍効果が消失しており、CpG ODN の抗腫瘍効果に CXCL14 との協調的な作用が必須であることが明らかとなりました。これらの発見は、抗がん活性を持つ DNA の生体内における新たな作用機序を明らかとするものであり、CpG ODN の抗腫瘍活性が有効な患者の特定や、より強い効果を得るための分子メカニズムの解明につながるものと考えられます。
社会的意義と今後の展望
本研究では、抗がん活性を持つ DNA とケモカイン CXCL14の相互作用とその分子メカニズムを詳細に解明しました。この知見は、がん免疫療法の新たな地平を切り開く可能性があります。本研究で明らかにした CXCL14 と CpG DNA の協調的な作用機序は、従来の免疫療法では効果が限定的であった難治性がんに対しても有効な治療アプローチの開発につながると考えております。特に、患者個々の CXCL14 発現量などを指標とした治療効果予測バイオマーカーの開発を進めることで、CpG ODN ベースの治療が特に効果的な患者群を特定できるようになるかもしれません。これにより、治療効果を最大化しつつ、不必要な副作用を回避することが可能となるほか、医療費の削減にも貢献することができると考えます。
本年度より開始した東京都特別研究「発がんメカニズム解明と新規がん免疫療法等の研究推進」の研究の中でも、この研究成果をさらに発展させ、基礎研究から臨床応用への橋渡しを加速していきます。 CXCL14/CpG DNA 複合体を基盤とする新規免疫賦活剤の開発や、その詳細な作用機序の解析等を通じて、革新的ながん治療法の確立を目指した研究をおこなっていく予定です。
東京都医学総合研究所は、この研究を通じて得られる科学的知見を都のがん対策施策に還元し、「誰一人取り残さないがん対策」を基本理念とする東京都がん対策推進計画の実現に貢献してまいります。がん患者の生活の質向上と生存率改善を目指し、病院連携を含め、基礎研究から臨床応用までの一貫した研究推進体制を構築することで、都民の健康増進に寄与する所存です。
本研究の主な助成事業
本研究は、文部科学省研究費補助金 JSPS KAKENHI(18K07313, 21K07208, 24K10443)、SBIバイオテックの支援を受けて行われました。
用語説明
- (注1)
- 樹状細胞 :生体に侵入した病原体を取り込み、そのタンパク質をプロセシングすることにより T細胞へと抗原提示する細胞。活性化すると様々な免疫応答を増強するサイトカインおよび増殖因子を発現する。
- (注2)
- 自然免疫: 病原体などに特徴的な分子を認識して、免疫反応を活性化する仕組み。現在では、自然免疫の活性化が抗体産生などの獲得免疫活性化の引き金となっていることが明らかとな っている。本研究では細菌に特徴的な非メチル化 CpG DNA を Toll-like receptor 9 が認識する仕組みに着目している。
- (注3)
- ケモカイン:白血球の遊走を誘導する分子量の小さい (8-10 kDa) 塩基性のタンパク質。50 種類以上のケモカイン分子が報告されている。
- (注4)
- CpG DNA:シトシンとグアニンの連続配列を持つ非メチル化 DNA。哺乳類ではメチル化されることが多いのに対して、細菌やウイルスではメチル化されていない(非メチル化)ことが知られている。 非メチル化 CpG DNA は細胞内に存在する Toll-like receptor 9 を活性化してさまざまな免疫応答を引き起こす。
