HOME > 広報活動 > 刊行物 > April 2014 No.013

April 2014 No.013
特集
研究紹介
開催報告
編集後記
特集
手足口病の原因 エンテロウイルス71の感染機構の解明
東京都医学総合研究所 ウイルス感染プロジェクトリーダー小池 智

エンテロウイルス71(以下EV71)はピコルナウイルス科エンテロウイルス属という仲間に分類されるウイルスです。ウイルス粒子はエンベロープを持たず、4種類のカプシドタンパク60個と1本のRNAゲノムからなっています。ピコルナウイルス科の仲間にはヒトの小児マヒの原因ウイルスであるポリオウイルス、A型肝炎ウイルス、鼻風邪の原因となるライノウイルス、ヒト以外を宿主とするウイルスとしては家畜に甚大な被害を与える口蹄疫の原因ウイルスFoot-Mouth Disease virus (FMDV)などがあります。EV71はヒトの手足口病の原因ウイルスの一つとして知られています。手足口病はコクサッキーウイルス(以下CV)A16、CVA6などのEV71の近縁のウイルスなどによっても起こる病気で、主に5歳未満の子供で春から夏にかけて見受けられる、発熱や文字通り手、足、口の発疹などを主徴とする感染症です。我が国においても手足口病の流行は見られ、原因となるウイルスは順番に入れ替わりながら流行を繰り返しています。手足口病自体は予後もよいため、これまでは非常に重要な感染症であるとは認識されていませんでした。
ところが1990年代後半から台湾、マレーシア、中国本土などの東アジア地域を中心としてEV71を原因とした手足口病の大きな流行があり、その際に患者の中には、確率は低いものの、無菌性髄膜炎、急性脳炎、急性弛緩性マヒ、神経原性肺水腫などの中枢神経合併症が報告されました。中国本土では2008年から2011年の間に2000人弱の死亡が報告されていて、流行はカンボジアやベトナムにも拡大しています。EV71以外のウイルスが原因となった場合には、中枢神経合併症が見られる率はEV71と比較するとずっと低いことが知られています。そのためEV71は神経向性を示す危険な新興感染症として注目を集めるようになってきました。しかし、このウイルスに関する基礎的な研究は進んでおらず、実用化されたワクチンも抗ウイルス薬もありません。ウイルスに対する対策を立てるにあたり、このウイルスの感染機構が不明であったため、合理的な対策を立てることは困難な状況にありました。
我々はこれまで近縁のポリオウイルスを扱ってきた経験を生かし、このウイルスの感染初期過程を明らかにすることを目標に研究を行ってきました。
ウイルスの感染は感染する細胞にウイルスが結合し、その後細胞内に侵入、ウイルスゲノムRNAを感染細胞の細胞質内に放出(脱殻と呼ばれています)、ウイルスタンパク質の合成、RNAの複製、ウイルスタンパク質とウイルスRNAの集合という過程を経て、子孫ウイルスができ、感染細胞を破壊します。 ウイルスは本来ウイルスのために存在している訳ではない生体分子を巧妙にウイルス増殖のために利用しています。 ウイルス受容体と呼ばれる分子もその一つで、ウイルスの細胞表面への結合、細胞内侵入、脱殻などの過程に関わり、感染の宿主域(感染可能な動物種の範囲)や臓器特異性(増殖して病変を生ずる臓器はウイルスによって異なっており、ウイルスの選り好みがあります)などに大きな影響を持っています。 我々はEV71の受容体を同定し、それを元にこのウイルスの防御戦略を立てることを考えました。
マウスのL929という細胞はEV71に感染しませんが、ウイルスRNAをトランスフェクションして細胞内に導入すれば子孫ウイルス粒子が産生されるので、この細胞でウイルスが感染しないのは結合、侵入、脱殻などのステップに関与する分子が欠損しているからだと推測されました。 そこでヒトの全DNAをこの細胞に遺伝子導入するとヒトDNAの一部分を持った細胞が多数できますが、約七万個のヒトDNAの一部を持った細胞群から2個のウイルス感受性を獲得した細胞を得ました。 この細胞のDNAを調べ、ヒト由来のDNAを検索することによって最終的にヒトのScavenger Receptor B (SCARB)が存在しているとマウス細胞がウイルス感受性になることが判りました(参考文献1)。 このSCARB2は本来リソソームにあるべき酵素が生合成されるとその酵素をリソソームへと輸送する働きを持っていて、多くはリソソームに存在しています。 しかし、ごく一部は細胞膜上にも存在していて、そこでEV71に出会うとウイルスと結合してしまいます。 マウスにもSCARB遺伝子は存在していますが、両者を比較すると約60アミノ酸の部分がヒトとの相同性が低く、ヒトSCARB2のこの部分がウイルスの結合に関与していて、種特異性を決めていることがわかりました(参考文献2)。 さらにこの分子はウイルス粒子を細胞に侵入させたり、細胞侵入後にエンドソームのpHが酸性になると脱殻反応を起こす引き金となっていることも明らかになりました(参考文献3)(図1)。 また、手足口病を起こす近縁のウイルスの中でもCVA16, CVA14, CVA7はこの受容体を使って感染することがわかりました(参考文献4)。
図1
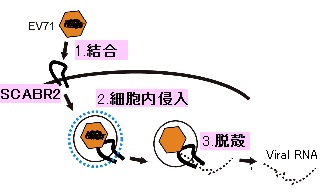
ワクチンや抗ウイルス薬の開発には動物実験が欠かせません。 このウイルスはSCARB2との結合性などの起因する種特異性が存在し、サルであればウイルスの感染はするものの、マウスなどの小型動物ではウイルスを無理やり馴化させる、或いは免疫不全のマウスを使うことにより何とか乳飲みマウスに感染させることができましたが、一般的に正常な成獣に感染を成立することはできませんでした。 この受容体分子が同定できたことで、種特異性の壁を越えた動物モデルが作製できました。 ヒトSCARB2を発現するトランスジェニックマウスを作製したところ、マウスはEV71を感染させると中枢神経系で増殖し、ヒトとよく似た病理学的変化、症状を再現することができました(参考文献5)(図2)。 マウスモデルはまだいくつかの点に改良を加える必要はありますが、小型動物を用いて実験を容易に行うことができるようになった点は大きな進歩です。 マウスモデルを用いて、発症に至る過程の解明やウイルスの毒力を正確に測定することなどができる可能性が開けました。 我々の研究以外でもこのウイルスに対する関心の高まりから、ウイルスの粒子構造の決定、不活化ワクチンの開発などがアジアの国を中心に活発化してきています。
図2
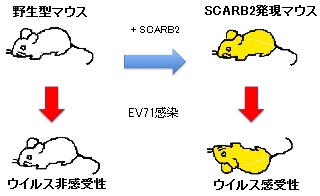
マウスモデルは、抗ウイルス薬やワクチンの有効性試験に有効であると思います。 現在このウイルスの感染症では、手足口病を起こすウイルスの中でなぜEV71だけが神経向性を持ち重症化するのか? 重症化が起こっている国で流行している国では、手足口病しか発生していない国と比べて毒力の強いウイルスが流行しているのか? そうであればどのような変異が強毒化に結び付くのか? 軽症で終わるヒトと重症化するヒトはなにが違うのか?重症化例がアジアに多いのは人種的な違いがあるのか?などが不明です。 マウスモデルを用いるとこのようなウイルス側の因子や宿主側の因子についての情報が得られると考えられます。 この研究で平成25年度の東京都職員表彰をいただき、関係者の皆様に感謝いたします。 今後もますます研究を発展させることができるように、全力を挙げて取り組んでいきたいと考えております。
参考文献
- Fujii K, Nagata N, Sato Y, Ong KC, Wong KT, Yamayoshi S, Shimanuki M, Shitara H, Taya C, Koike S.
Transgenic mouse model for the study of enterovirus 71 neuropathogenesis.
Proceedings of the National Academy of Sciences of the United States of America.
2013 Sep 3;110(36):14753-8. doi: 10.1073/pnas.1217563110. - Yamayoshi S, Iizuka S, Yamashita T, Minagawa H, Mizuta K, Okamoto M,
Nishimura H, SanjohK, Katsushima N, Itagaki T,Nagai Y, Fujii K, Koike S.
Human SCARB2-dependent infection by coxsackievirus A7, A14, and A16 and enterovirus 71. - Yamayoshi S, Koike S.
Identification of a human SCARB2 region that is important for enterovirus 71 binding and infection.
Jounal of Virology. 2011 May;85(10):4937-46. doi: 10.1128/JVI.02358-10. - Yamayoshi S, Ohka S, Fujii K, Koike S.
Functional comparison of SCARB2 and PSGL1 as receptors for enterovirus 71.
Jounal of Virology. 2013 Mar;87(6):3335-47. doi: 10.1128/JVI.02070-12. - Yamayoshi S, Yamashita Y, Li J, Hanagata N, Minowa T, Takemura T, Koike S.
Scavenger receptor B2 is a cellular receptor for enterovirus 71.
Nature Medicine. 2009 Jul;15(7):798-801. doi: 10.1038/nm.1992.

