HOME > 広報活動 > 刊行物 > October 2014 No.015

October 2014 No.015
特集
研究紹介
開催報告
お知らせ・編集後記
研究紹介
がん代謝におけるmTOR複合体2の役割について
英国科学雑誌「Cell Trends in Endocrinology & Metabolism」に病院等連携研究センター・神経病理解析室の増井憲太研究員の研究成果が発表されました。
神経病理解析室 主席研究員増井 憲太
がん細胞は正常の細胞と異なり、物質の代謝経路を自身に都合の良いように再構成して、過酷な環境下でも生き延びることが知られています。具体的には、解糖系と呼ばれる細胞内の呼吸経路が、通常では酸素が少ない状態で活性化されますが、がん細胞では酸素の濃度に関わらず常にこの経路が活性化され、急速に増殖するために必要な材料およびエネルギーががん細胞に供給されると考えられています。これは、「がん代謝(またはワールブルグ効果)」として知られ、生体に有害である一方、がん細胞の生存には有利に働きます。そこで、がん代謝の仕組みを明らかにしてがん代謝を抑えることで、ヒトの体へ影響を与えることなく、がん細胞のみを殺すことができるような治療法を開発することが、私たちの目指すところです。
私たちのがん代謝研究は、mTOR複合体という分子に注目しています。mTOR複合体は細胞の代謝を調節する中心的な存在であり、mTOR複合体1(mTORC1)とmTOR複合体2(mTORC2)に分類されます。これまでの研究により、mTORC1はがん代謝を亢進させる悪玉分子であることが知られています。一方、mTORC2も、がんの成長に必要であるということが報告されていますが、がん代謝との関係はこれまで明らかにされていませんでした。
私たちの研究により、このmTORC2もがん代謝を亢進させる悪玉分子であることが分かりました(文献1)。がん代謝の調節に必要なc-Mycという分子の発現レベルをmTORC2が上昇させることによって、悪性脳腫瘍のがん代謝が促進されることが明らかになりました。また、mTORC2によるがん代謝により、脳腫瘍患者さんの予後が悪くなることも分かりました。これまで、がん代謝を亢進させる因子としてはAKTという分子が知られており、AKTを阻害することでがんを治療しようとする試みが検討されていました。しかし、私たちが発見したmTORC2経路は、このAKT経路とは独立してがん代謝を制御していました。つまり、AKTを抑制することでがん代謝を阻害し、がんを治療しようとしても、がん細胞はmTORC2経路を利用してがん代謝を維持し、生き延びることが分かったのです(図1)。これは、がんが治療に抵抗する仕組みの一つであると考えられ、今後克服すべき問題です。
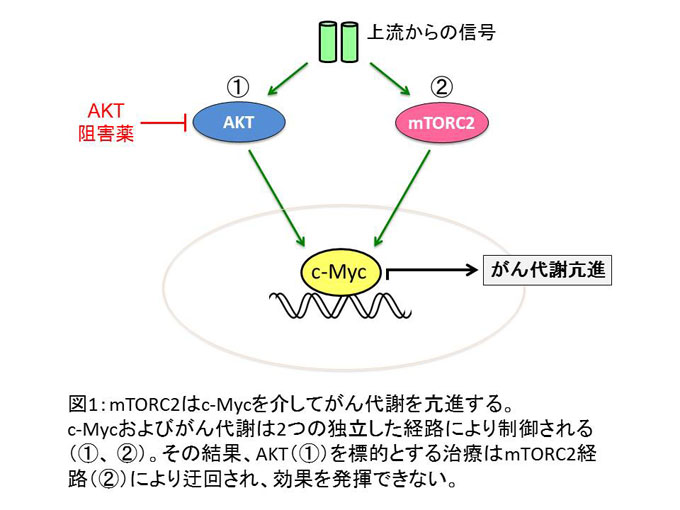
続いて私たちは、前述したc-Mycとの関わりを通して、がん代謝におけるmTORC2の様々な役割(解糖系、アミノ酸代謝、脂質代謝、核酸および活性酸素代謝)を説明する総説を執筆しました(文献2)。そこでは、治療が難しい悪性脳腫瘍である膠芽腫(グリオブラストーマ)に特に注目して、がん代謝についてまとめています。近年、DNAの変化によらずに遺伝子の発現を制御するエピジェネティクスという現象が、がんの成長に重要であることが分かってきました。驚くべきことに、mTORC2によるがん代謝は、エピジェネティクスにも影響し、がんの成長を助けることが分かってきました。つまり、がん細胞の生存に必要なあらゆる現象に、mTORC2が関与することが明らかになってきたわけです(図2)。
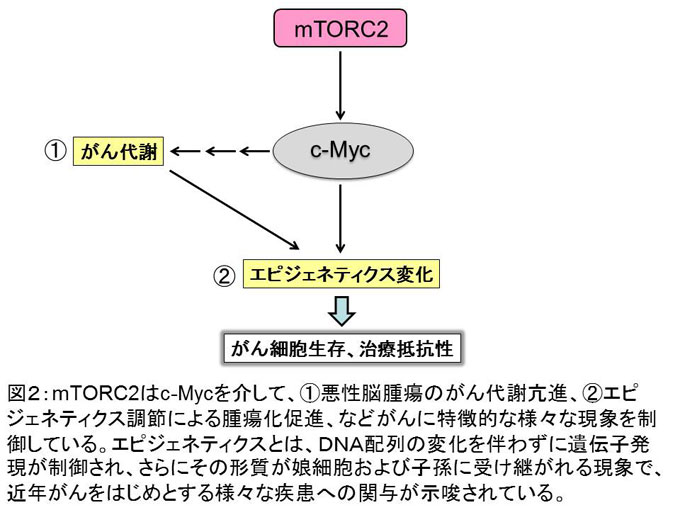
がんが活発に増殖する際に細胞内の代謝がどのように利用されているか、ということに関してはまだまだ学ぶべきことが多々ありますが、研究を進めて知識を集積していくことで、治療が難しいがんに対しても、がん代謝を標的とする新しい治療法を確立していくことが可能になると考えています。
参考文献
- Masui K, Tanaka K, Akhavan D, Babic I, Gini B, Matsutani T, Iwanami A, Liu F, Villa GR, Gu Y, Campos C, Zhu S, Yang H, Yong WH, Cloughesy TF, Mellinghoff IK, Cavenee WK, Shaw RJ, Mischel PS.
mTOR complex 2 controls glycolytic metabolism in glioblastoma through FoxO acetylation and upregulation of c-Myc.
Cell Metabolism. 2013 Nov 5;18(5):726-39.
doi: 10.1016/j.cmet.2013.09.013. - Masui K, Cavenee WK, Mischel PS.
mTORC2 in the center of cancer metabolic reprogramming.
Trends in Endocrinology & Metabolism. 2014 Jul;25(7):364-73.
doi: 10.1016/j.tem.2014.04.002.

