
2019年10月10日
ユビキチンプロジェクトの小谷野史香 主任研究員及び松田憲之 副参事研究員らは 「ユビキチンがミトコンドリア - ペルオキシソーム間輸送シグナルとして機能する」 ことを 「EMBO Reports」に発表しました。
ユビキチンがミトコンドリア - ペルオキシソーム間輸送シグナルとして機能する
当研究所 ユビキチンプロジェクトの小谷野史香 主任研究員及び松田憲之 副参事研究員らは、ParkinによってMITOLのK268がユビキチン化されると、これがシグナルとなり、p97/VCPによってミトコンドリア外膜からMITOLが引き抜かれて、Pex3, Pex16依存的にペルオキシソームに輸送されることを初めて明らかにしました。この結果は、ユビキチンがミトコンドリア - ペルオキシソーム間輸送シグナルとして機能することを世界で初めて示したものです。
本研究は、2019年10月10日「EMBO Reports」on-line版に掲載されました。
- <論文名>
- ”Parkin‐mediated ubiquitylation redistributes MITOL/March5 from mitochondria to peroxisomes”
(ユビキチンがミトコンドリア - ペルオキシソーム間輸送シグナルとして機能する) - <発表雑誌>
- EMBO Reports
DOI : 10.15252/embr.201947728
URL:https://www.embopress.org/doi/10.15252/embr.201947728
研究の背景
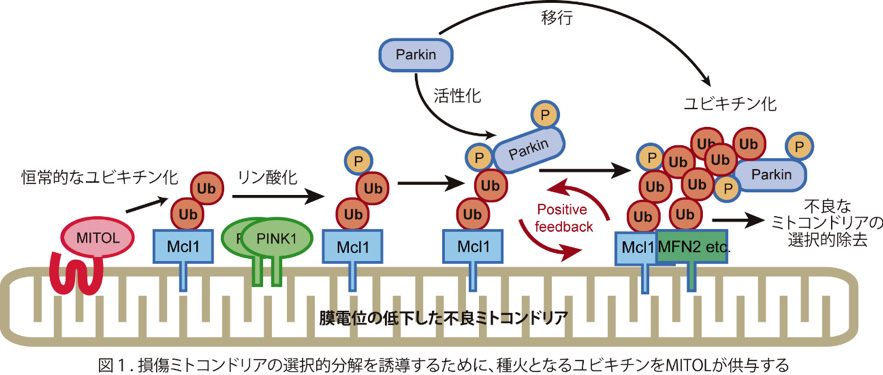
我々は、遺伝性パーキンソン病の原因遺伝子産物であるPINK1 (Ser/Thr kinase) とParkin (Ubiquitin ligase: E3) が低品質なミトコンドリアをユビキチン化して除去することでミトコンドリアの品質管理を行うことを示してきました(Matsuda et al, JCB., 2010)。さらに、この過程においてPINK1がユビキチンをリン酸化することや、リン酸化ユビキチンがParkinの活性化因子であることを明らかにしてきました(Koyano et al, Nature, 2014)。このプロセスにおいては、PINK1によるユビキチンのリン酸化と、リン酸化ユビキチンによって活性化されたParkinによるユビキチン化が positive feedback loop を形成することでシグナルが増強されます(Okatsu et al, JCB., 2015)(図1)。しかしながら、膜電位低下直後にParkinを活性化するためのユビキチンが供給されるメカニズムは未解明でした。そこで、マイトファジーが誘導される環境下において、Parkinと協調して働くミトコンドリア局在型E3の探索を試みました。また、ミトコンドリア損傷時にオルガネラ間で生じる膜蛋白質のダイナミックな動態変化についても研究を行いました。
研究の概要
複数のミトコンドリア局在型E3のなかで、4回膜貫通型蛋白質であるMITOLをノックダウンすることでParkinの活性化と損傷ミトコンドリアへの移行が遅延することが分かりました。また、Parkinによるミトコンドリア蛋白質のユビキチン化も遅延しました。これらのことから、MITOLがミトコンドリアに少量のユビキチンを恒常的に付加することによって、マイトファジー初期のParkinの活性化とミトコンドリアへの動員を効率化することを明らかにしました(図1)(Koyano et al, JBC., 2019)。
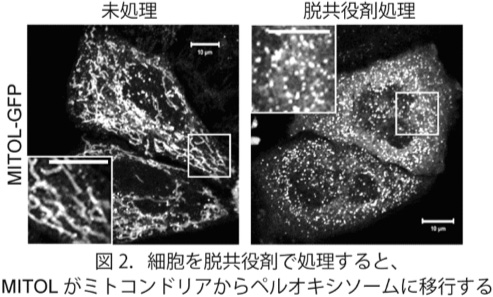
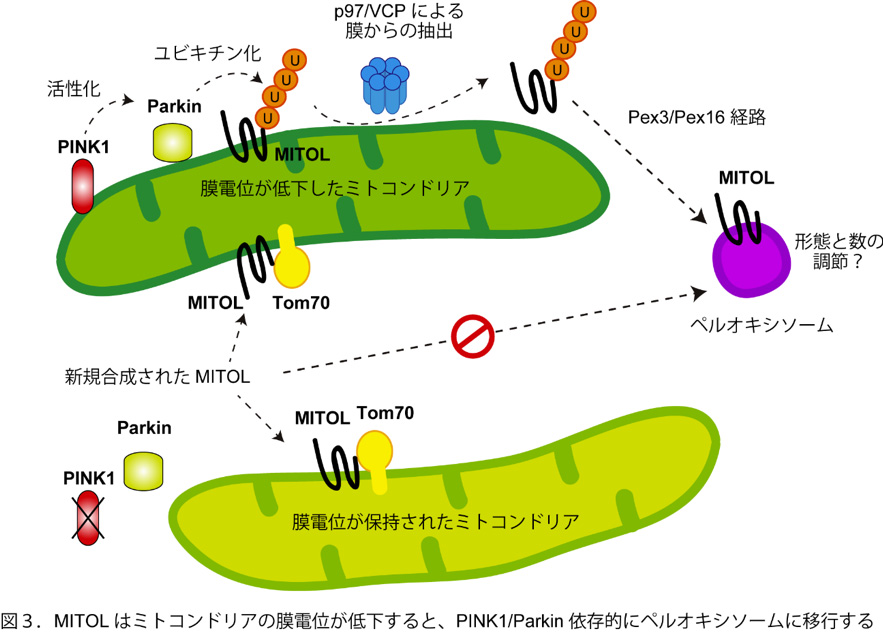
非常に興味深いことに、上記の実験を進める過程でMITOLが予想外の挙動を示すことを発見しました。つまり、ミトコンドリアの膜電位が低下した状態が継続すると、MITOLの局在が損傷ミトコンドリアからペルオキシソームに変化する現象を見出しました(図2)。また、この現象はミトコンドリアの膜電位低下に加えて、PINK1とParkinの活性に依存することが判明しました。質量分析および変異体解析から、ParkinによってMITOLのK268がユビキチン化されると、これがシグナルとなり、p97/VCPによってミトコンドリア外膜からMITOLが引き抜かれて、Pex3, Pex16依存的にペルオキシソームに輸送されることを初めて明らかにしました(図3)(Koyano et al, EMBO Rep., 2019)。
今後の展望
膜蛋白質がミトコンドリアからペルオキシソームへと移行するオルガネラ間輸送において、ユビキチン化という翻訳後修飾がシグナルとして機能するという報告は過去に例がなく、新奇の現象として非常に興味深いものです。
上述のようにMITOLが損傷ミトコンドリアからペルオキシソームに移行する際にはp97/VCPが関与しますが、AAA ATPaseであるp97/VCPは複数のcofactorと協調して、標的蛋白質上のユビキチン鎖を認識し、膜から蛋白質を抽出することが知られています。今後は、ミトコンドリア膜からMITOLが選択的に引き抜かれる現象が、p97/VCP cofactorのどの分子に依存するのかについて調べたいと思っています。また、ペルオキシソームに輸送されたあとに、MITOLがユビキチン化する基質蛋白質も探索する予定です。


