
HOME > 身近な医学研究情報 > 糖尿病合併症から身を守る
糖尿病合併症から身を守る
3.糖尿病による神経系の障害
糖尿病性神経障害
3大合併症の中で、糖尿病発症から最も早期に出現し、頻度の高いのが神経障害です。頭から足趾(足の指)・足底(足の裏)まで多彩な臨床症状を呈します。
中枢神経系と末梢神経系
神経系は中枢神経系と末梢神経系に区分されます。末梢神経系は12対の脳神経と31対の脊髄神経からなり、身体の末梢各部からの情報を中枢神経系に伝える(求心性)とともに、中枢神経系からの情報を末梢に伝える役目(遠心性)を担っています。中枢神経系は脳と脊髄から構成され、末梢神経系から送られてきた情報を統合・処理し、適切な応答を送るための作業がおこなわれる場所です。糖尿病では末梢神経系がおかされやすいことから、「糖尿病神経障害」といえば通常は末梢神経疾患に分類されます。しかしながら先述したグリケーションとの関連や、動脈硬化に伴う脳血管病変や低血糖性脳障害などにより、糖尿病患者では認知機能の低下や痴呆等の中枢神経の障害も起こりやすいということもわかってきました。
末梢神経系の構造と機能
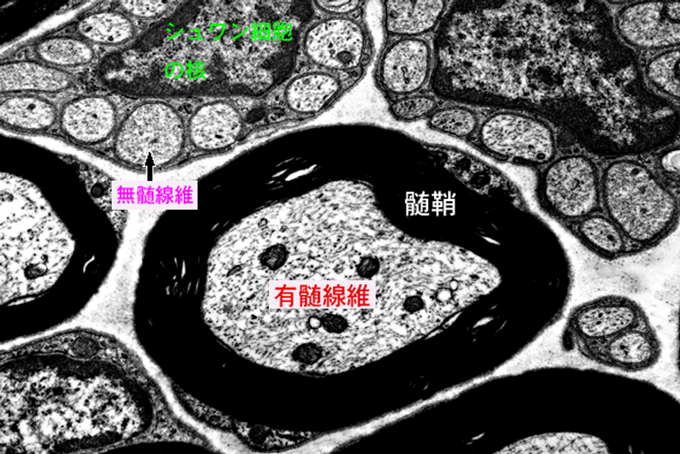
末梢神経は、痛み、温度感覚(温かさ、冷たさ)、触覚などを伝える感覚神経、手や足の動きを司る運動神経、内臓や内分泌器官などの働きを調節する自律神経(交感神経と副交感神経)に大別されます。末梢神経系を構成する主な細胞は、神経細胞とシュワン細胞です。神経細胞は長い突起を出して上位(中枢側)もしくは下位(末梢側)からの情報を受け取り、さらにその情報を下位もしくは上位へと伝えます。一般に、情報を受け取り細胞体へ伝搬する側の突起を樹状突起、細胞体から次の神経細胞あるいは筋肉などの効果器に向けて送信する側の突起を軸索といいます。軸索の終末は細かく枝分かれしており、他の神経細胞の樹状突起や細胞体との間にシナプスを形成します。神経細胞内ではすべての情報が電気信号(活動電位)として伝えられる(伝導)のに対し、シナプスでは軸索終末に届いた電気信号が化学的信号(神経伝達物質)に置き換えられて、次の神経細胞へと送られます(シナプス伝達)。シュワン細胞は軸索の周囲を取り囲み、髄鞘を形成します。髄鞘に囲まれた神経線維を有髄線維、髄鞘を持たない線維を無髄線維といいます。複数の無髄線維は一つのシュワン細胞の膜に包まれています(図10)。また外傷や手術などによって末梢神経が損傷された際には、シュワン細胞から多くの神経栄養因子、サイトカイン等の活性物質が放出され、神経線維の再生を促し機能修復にはたらくものと考えられています。活動電位を伝える速さ(神経伝導速度)は神経線維の直径に比例し、太い線維ほど伝導速度が速いことになります。また有髄線維の方が無髄線維より伝導速度が速くなります。一般に太い感覚神経線維(大径有髄線維)は振動覚や深部感覚を、細い感覚神経線維(小径有髄線維、無髄線維)は痛覚や温度感覚を伝えます。糖尿病では太い線維、細い線維ともに障害され、さまざまな感覚神経障害の原因となります。
図10. 有髄線維と無髄線維の電子顕微鏡像
※ 東京都医学研・糖尿病性神経障害プロジェクトでは、神経細胞やシュワン細胞の培養系を用いて、神経の再生や変性機構、糖尿病神経障害をはじめとする末梢神経疾患の病態などについて研究しています(図11)。
図11. 神経細胞とシュワン細胞株の共培養による髄鞘形成誘導
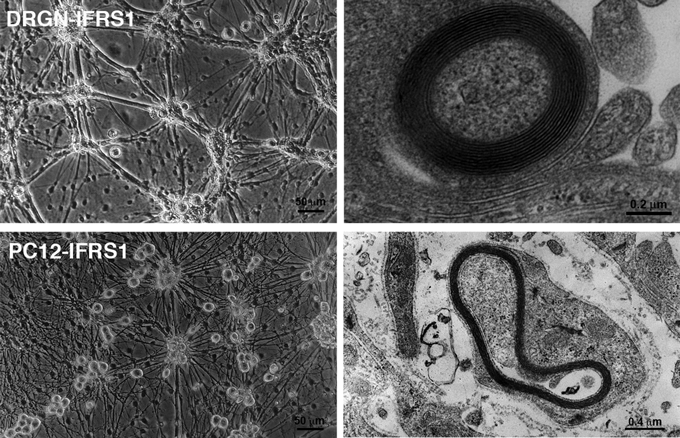
成熟ラットの感覚神経細胞 (DRGN)や株化神経細胞(PC12)と株化シュワン細胞 (IFRS1)との共培養系を4週間維持することにより、髄鞘の形成がみられた(右:電子顕微鏡像)。この系を用いて、神経変性・再生に関与する因子の解析を進めている。(上段左:Sango et al., J Neurosci Res 2011, 上段右:Exp Diabetes Res 2011, 下段:Histochem Cell Biol 2012; 出版社の許可を得て転載)
神経障害の成因
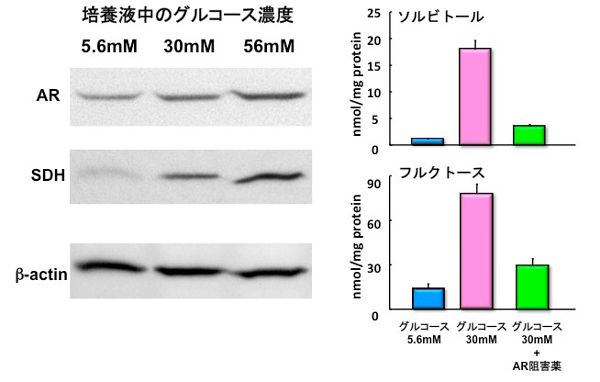
前述の通り、ポリオール代謝亢進、糖化、プロテインキナーゼC活性異常、酸化ストレス等の代謝異常が、神経障害の発症・進展に深く関与していると考えられています。末梢神経ではシュワン細胞にARが強く発現しており、シュワン細胞におけるポリオール代謝の亢進が糖尿病神経障害の発症に深く関与するものと考えられています。私たちの研究でも、株化シュワン細胞を高グルコース濃度 (≧30 mM)で維持することにより、ARやSDHのタンパク発現が上昇し細胞内ソルビトール・フルクトース量の著増がみられました。また高グルコースに伴うソルビトール・フルクトース量の増加は、AR阻害薬を加えることにより抑制されました(図12)。現在このシュワン細胞を用いて新たなAR阻害薬の薬効について検討しており、従来の薬剤に比べより低容量でソルビトール・フルクトース量の増加を抑制しうる結果が得られています。
図12. 高グルコース負荷に伴うポリオール代謝の亢進:株化シュワン細胞による検討(Sango et al., J Neurochem 2006を一部改変)
その他、神経障害に特有の病態として軸索輸送の障害、神経栄養因子の作用不足、イオンチャネル異常等が報告されています。
- 軸索輸送の障害:
- 神経の軸索にはリボゾームが存在せず、タンパク質が合成できません。したがって軸索の構造や機能を維持するには、細胞体で合成したタンパク質を軸索の終末まで運搬する必要があります。この機構を軸索輸送(順行性輸送)といいます。逆に軸索の終末で取り込まれた物質を細胞体に運ぶ逆行性輸送の機構も存在し、ともに微小管と呼ばれるレールの上で物質が運搬されます。実験糖尿病ラットの軸索では順行性、逆行性の輸送ともに低下がみられており、前者は細胞骨格タンパクの供給不足から軸索の萎縮や変性を、後者は神経栄養因子などの作用不足から細胞機能障害を引き起こします。
- 神経栄養因子の作用不足:
- 神経成長因子 (Nerve growth factor (NGF))をはじめとする神経栄養因子群は、皮膚や末梢組織で作られ軸索の末端から取り込まれた後、逆行性の軸索輸送によって神経の細胞体に運ばれます。NGFは感覚神経や交感神経の機能維持、軸索再生、神経ペプチドの発現等に深く関与しています。糖尿病ではNGFの産生低下や軸索輸送の障害によって神経細胞体への作用不足が生じ、感覚障害、軸索再生遅延、自律神経機能異常の要因となることが示唆されています。糖尿病性神経障害の治療薬としてNGFの臨床治験が進められましたが、副作用等により開発中止となりました。
- イオンチャネル異常:
- 痛覚に関与する小型感覚神経細胞では、高血糖に伴うナトリウムチャネルやカルシウムチャネルの機能異常が報告されています。これらの異常は神経の興奮性を高め、痛覚過敏(後述)や自発痛などに関係すると考えられます。
神経障害の病型
糖尿病神経障害は、左右対称性びまん性神経障害(感覚神経障害・自律神経障害)と単神経障害に大別されます。前者の方が圧倒的に頻度が高く、臨床的にも重要です。
- 左右対称性びまん性神経障害:
- 左右対称性に出現し、足趾や足底部が最初におかされやすく感覚障害が優位(運動障害は認めないか、あっても軽度)、という特徴があります。さらに早期から下肢の振動覚やアキレス腱反射が低下し、多くの例で自律神経症状を伴います。
- 単神経障害:
- 神経を栄養している血管の障害が深く関与していると考えられており、急激に発症し多くは1年以内に症状の改善がみられます。比較的頻度の高い動眼神経麻痺では、「物が二重に見える」、「まぶたが下がる」などの症状がみられます。その他、脳神経(外転神経、滑車神経、顔面神経)や四肢の運動神経(尺骨神経、腓骨神経)の麻痺、糖尿病性筋萎縮などがあります。
感覚神経障害
- 異常感覚:
- 長時間の正座をした時のようなジーンとした感覚や、電気が走るようなビリッとした感覚を認めることがあります。「足の裏にもう一枚皮があるような感じ」、「足の上を蟻がはうような感じ」というのもよく聞く訴えです。
- 疼痛:
- 足の先から「刺すような」あるいは「焼けるような」強い痛みを認めます。昼間(活動時)よりも夜間に痛みが増強することが多く、睡眠障害やうつ状態に陥ることもあります。
- 痛覚過敏:
- 痛覚に関係する神経線維が興奮しやすい状態になっており、健常者では痛みと感じない程度の刺激を認識してしまいます。
これらの刺激症状は非常に煩わしいものですが、必ずしも糖尿病性神経障害の進行度とは並行せず、血糖コントロールによって改善可能です。 - 感覚鈍麻(感覚神経の麻痺):
- 神経障害が進行すると、痛みなどの刺激に対する反応が低下します。足先の感覚が鈍くなり、重症の患者さんでは割れたガラスを踏んだり熱湯でヤケドをしても気が付かず、大きなケガにつながります。無痛性心筋梗塞を起こす危険も高くなります。
自律神経障害
- 起立性低血圧:
- 急に立ち上がった時に、立ちくらみやめまいが生じます。姿勢の変化に伴う血圧の調節機構が障害されているために起こります。
- 発汗異常:
- 汗腺の機能を調節する交感神経が障害されることによって起こります。発汗量の減少は皮膚乾燥の原因となり、手や足の「ひび割れ」「あかぎれ」を生じ感染が起こりやすくなります。また発汗は低血糖の重要なサインの一つなので、発汗が減少していると低血糖が自覚しにくくなります
- 無自覚性低血糖:
- インスリン注射などで血糖値が70 mg/dL以下まで低下すると、インスリン拮抗ホルモン(グルカゴンやアドレナリン)の分泌を促し血糖上昇に向かわせる生体防御機構が作動します。また交感神経優位の状態となって、発汗、ふるえ、動悸、不安感等の警告症状が出現します。ところがインスリン拮抗ホルモンの分泌が障害されたり交感神経系の反応が低下したりすると、警告症状なしに重症低血糖をきたす(突然意識を失って昏睡に陥る)おそれがあります。特に自動車の運転中に意識を消失すると交通事故につながる危険が高く、注意が必要です。2013年6月に改正道路交通法が成立し、自動車の運転に支障をきたす可能性がある病気の患者が、運転免許証の取得や更新時に虚偽の申告をした場合の罰則規定が新設されました。対象となる疾患には、無自覚性低血糖も含まれます。
- 胃腸障害:
- 消化管の運動を調節する自律神経が障害されて起こります。胃から腸へ食物を送り込む機能が低下し、いつまでも消化されない(胃無力症)、便秘や下痢を交互に繰り返す、などの症状がみられます。
- 膀胱障害:
- 膀胱の収縮力が低下して排尿が困難になります。これに加えて感覚神経障害が進行すると尿意を感じにくくなり、排尿回数が減少します。導尿が必要になる場合があります。
- 勃起障害(ED):
- 勃起に関係する神経や筋肉、血管の障害で起こります(器質的ED)が、心因性の場合も考えられるので、治療にはまずその鑑別が必要です。
神経障害の検査・診断
診察ならびに神経学的検査により糖尿病神経障害の有無や程度を知ることが、治療を進める上でも重要です。進行して不快な症状が前面に出てからでは、改善は容易ではありません。
- 感覚機能検査:
- 触覚検査(筆を用いて触覚が減弱している部位を調べる)、痛覚検査(ピンなどを用いて痛覚過敏や減弱部位を調べる)、振動覚検査(くるぶしに音叉をあてて振動の感じ方を調べる)(図13)等で感覚神経障害の程度を評価します。
図13.音叉による振動覚検査
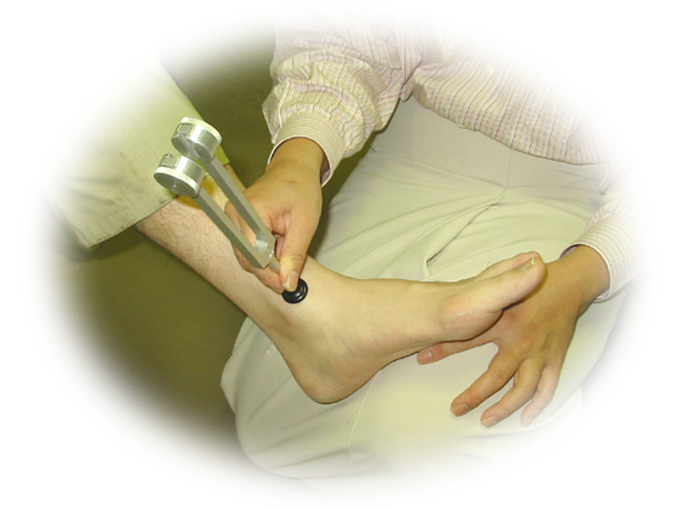
音叉をハンマー等で叩いて振動させ、柄の部分を被検者の内くるぶし(内踝)に当てる。被検者に「振動が感じられなくなった時点」で合図してもらい、振動が感じられなくなるまでの時間(秒)を測定する。
- 腱反射:
- 糖尿病性神経障害では下肢の腱反射、特にアキレス腱反射(図14)が低下もしくは消失していることが多く、早期診断に有効です。
図14.アキレス腱反射
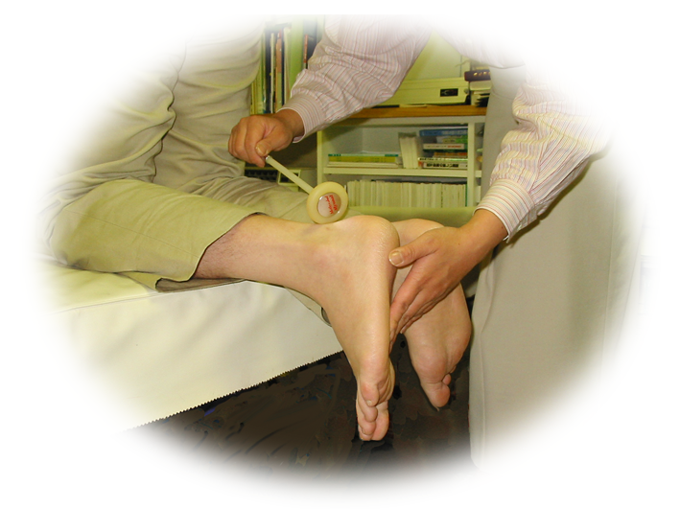
被検者に立て膝(膝立位)で椅子やベッドの上にのってもらい、ハンマーでアキレス腱を叩く。「反射消失」、「減弱」、「正常」、「やや亢進」、「亢進」、「著明な亢進」の6段階で評価する。
この他、神経伝導検査や自律神経機能検査(専門施設で実施)も、神経障害の評価に有用です。他の末梢神経疾患の可能性を除外した上で、自覚症状や検査所見などを総合的に評価して「糖尿病神経障害」と診断します。糖尿病内科医、神経内科医を中心とした神経障害の専門家で組織された「糖尿病性神経障害を考える会」によって、一般の医師にも使いやすい簡易診断基準(表4)が作成されています。
(表4)
糖尿病性多発神経障害 (distal symmetric polyneuropathy) の簡易診断基準
[Peripheral Nerve 末梢神経第31巻1号(2020年7月発行)より許可を得て転載]
糖尿病性神経障害を考える会
1998年9月11日作成
2000年3月24日改訂
2002年1月18日改訂
2019年8月31日改訂
必須項目
以下の2項目を満たす。
- 糖尿病が存在する。
- 糖尿病性多発神経障害以外の末梢神経障害を否定しうる*。
[*: 鑑別診断プロトコルを参照(図1・表1)]
条件項目
以下の3項目のうち2項目以上を満たす場合を “神経症状あり”とする。
- 糖尿病性多発神経障害に基づくと思われる自覚症状
- 両側アキレス腱反射の低下あるいは消失
- 両側内踝の振動覚低下
注意事項
- 糖尿病性多発神経障害に基づくと思われる自覚症状とは、
- 両側性
- 足趾先および足底の“しびれ” “疼痛” “異常感覚”のうちいずれかの症状を訴える。
上肢の症状のみの場合および“冷感”のみの場合は含まれない 。 - アキレス腱反射の検査は膝立位で確認する。
- 振動覚低下とはC128音叉にて10秒以下を目安とする。
- 高齢者については老化による影響を十分考慮する。
参考項目
以下の参考項目のいずれかを満たす場合は、条件項目を満たさなくても ”神経障害あり” とする。
- 神経伝導検査で2つ以上の神経でそれぞれ1項目以上の検査項目(伝導速度、振幅、潜時)の明らかな異常を認める。
- 臨床症候上、明らかな糖尿病性自律神経障害がある。しかし、自律神経機能検査で異常を確認することが望ましい。
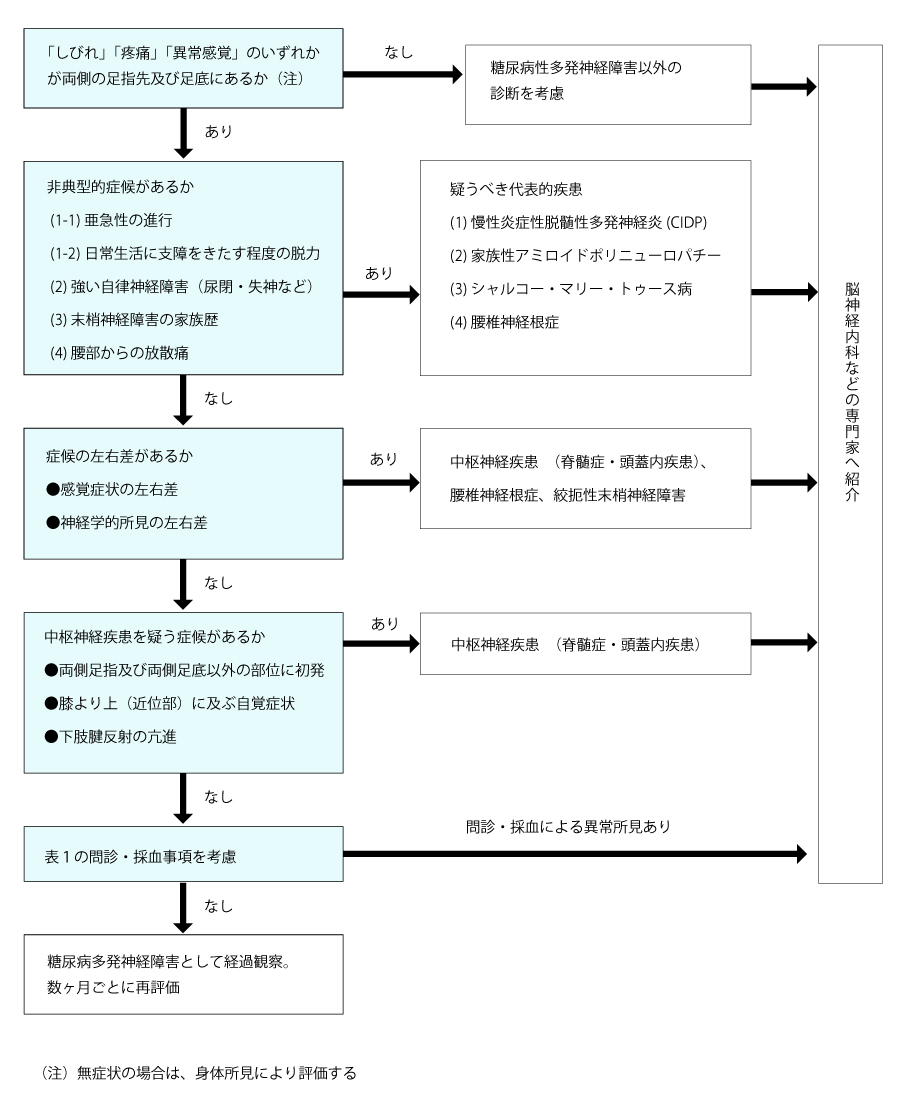
図1.鑑別診断フローチャート
| 腎疾患などのスクリーニング | 問診:腎不全や透析の有無 採血:一般生化学/血算 |
|---|---|
| アルコール性・ビタミン欠乏・毒物・薬物 | 問診:
|
| 他疾患 | 問診:
|
表1:糖尿病性多発神経障害と併発しうる、あるいは鑑別が困難な末梢神経疾患に推奨される問診と採血事項
参考文献
- England JD, Gronseth GS, Franklin G, et al. Evaluation of distal symmetric polyneuropathy: the role of laboratory and genetic testing (an evidence-based review). Muscle Nerve. 2009;39(1):116–125.
- Callaghan BC, Price RS, Feldman EL. Distal Symmetric Polyneuropathy: A Review. JAMA. 2015;314(20):2172–2181.
- Pop-Busui R, Boulton AJ, Feldman EL, et al. Diabetic Neuropathy: A Position Statement by the American Diabetes Association. Diabetes Care. 2017;40(1):136–154.
糖尿病の足病変
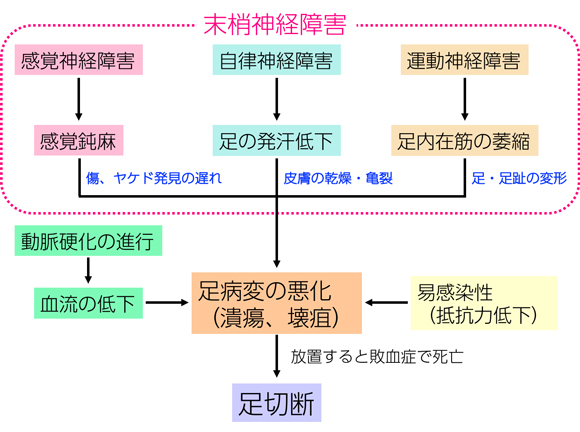
糖尿病患者は高血圧症や高脂血症を合併している場合も多く、動脈硬化が進行しており、足先への血流が低下しています。そのため、足にできた傷を治すのに十分な栄養を供給できなくなっています。また糖尿病では細菌などの病原体に対する抵抗力が低下しているので、ひとたび傷口が化膿すると病変が悪化しやすく、潰瘍や壊疽(えそ)を起こします。壊疽とは組織が腐っていくことで、放置すると感染が全身に拡がり敗血症で死亡します。そのため足を切断しなければいけなくなることもあります(図15)。交通事故などの外傷を除くと、足を失う原因で最も多いのは糖尿病です。
血流障害、抵抗力の低下に加え、神経障害の進行も足病変の悪化に深く関与しています。感覚神経の障害は痛覚や温度感覚の鈍麻を招き、足に傷やヤケドを負っても気がつかず、発見の遅れにつながります。また皮膚の汗腺に分布している自律神経は、汗の排出を調節しています。この障害により足の発汗量が低下し、皮膚の乾燥や亀裂、またタコやウオノメなどの小さな病変が生じやすくなります。糖尿病では感覚神経、自律神経に比べて運動神経の障害はあまり目立たないのですが、それでも進行すると足の筋肉が萎縮し、足や足の指が変形しやすくなると言われています。
糖尿病から足を守るためには、毎日足をよく観察して状態をチェックし、以下のような細かいケアを怠らないことが大切です。
- 足に合った靴をはく。
ヒールの高い履物やつま先の窮屈なものは避ける。ウォーキングシューズタイプか運動靴で、かかとがしっかり固定できるものを選ぶ。 - 風呂でヤケドをしないように、湯の温度に気をつける(約40℃に調節し、入浴前に湯加減を肘などでチェックする)。
- こたつや電気カーペットはヤケドの原因になるので、部屋全体を暖める暖房器具を使用した方が良い。
- ケガを防ぐため素足を避け、通気性の良い靴下をはく。
- 爪の手入れをする(深爪をしない)。視力に障害があれば、家族に爪を切ってもらう。
- 清潔を保つ(刺激の少ない石鹸を用いて足浴する)。
- マメやウオノメは自分で処置せず、医師に相談する。
(国立病院機構京都医療センター 河野茂夫先生の都民講座講演資料を参考に作成しました)
図15. 糖尿病の足病変
治療後神経障害 (post-treatment neuropathy)
長期にわたり放置された、もしくはコントロール不良だった糖尿病患者に短期間で急激な血糖是正をおこなうと、痛みやしびれなどの神経症状が出ることがあります。原因は不明ですが、ブドウ糖代謝や血流の急速な変化によるものと考えられています。同様に短期間の厳格な血糖コントロールで網膜症が悪化することがあるので、コントロールの極めて不良な患者には時間をかけて高血糖を是正する必要があります。
中枢神経系の障害
末梢神経系と異なり、中枢神経系では高血糖に伴うポリオール代謝の亢進は顕著ではありません。しかしながら血流異常や糖化、酸化ストレス等の代謝異常は脳でも進行していることが示唆されており、これらの異常は脳の老化や血管病変を促進する因子となりえます。これに加えて、無自覚性低血糖の持続により脳のブドウ糖量が低下し、認知機能低下や痴呆を引き起こす(低血糖性脳障害)可能性が示唆されています。
- 認知症:
- これまでに蓄積されてきた疫学研究により、高齢者糖尿病では認知症の合併が多いことが報告されています。認知症の2大原因である脳血管性認知症とアルツハイマー病の相対危険度は、脳血管性認知症では2.0~3.4、アルツハイマー病に関しても1.3~3.4と糖尿病患者では認知症の発症が多くなることがわかりました。原因としても、先述した動脈硬化による血管の障害、酸化ストレスやタンパクの糖化が直接神経細胞に影響しているほか、脳におけるインスリンの神経保護作用が低下する可能性等が示唆されています。
神経障害の治療
神経障害の治療の基本は、他の合併症と同様に血糖コントロールを長期にわたってしっかりおこなうことです。これに成因に基づいた治療薬を併用することで、症状が軽減する場合もあります。
- アルドース還元酵素阻害薬:
- ポリオール代謝経路の最初のステップ(ブドウ糖からソルビトールへの変換)を遮断して、ソルビトールの上昇を抑えます。初期の神経障害に対し有効性が示されていますが、血糖コントロール不良例や病期の進行した神経障害には効果が乏しいこともわかっています。
- 血流改善薬:
- プロスタグランジン製剤や抗血小板薬は、神経血流の改善を目的として処方される場合があります。
- ビタミンB12製剤:
- 軸索輸送を促進して、神経再生能を高める効果があります。
- ビタミンE製剤:
- 抗酸化作用があります。
自覚症状が強い場合は対症療法が必要になります。激しい痛みに対しては、抗不整脈薬、抗けいれん薬、抗うつ薬などが処方されてきましたが、効果が充分でないケースも多く課題とされてきました。最近、新たな疼痛治療薬としてプレガバリンとデュロキセチンが、糖尿病性の疼痛にも使用可能となりました。プレガバリンは、主に神経系に分布するカルシウムイオンチャネルに結合し、各種神経伝達物質の放出を抑制することで鎮痛作用を発揮します。デュロキセチンは、痛みの抑制に関与するセロトニンとノルアドレナリンを増やすことで,鎮静効果を発揮すると考えられています。

