2026年5月14日
川路英哉ゲノム医学研究センター長らの研究グループは、東京科学大学 総合研究院、九州大学、フライブルク大学と共同で「「壊れた脳は治らない」を覆す-脳が自然に治る力を持続させる方法を発見!-」についてNature に発表しました。
「壊れた脳は治らない」を覆す
-脳が自然に治る力を持続させる方法を発見!-
論文情報
- <論文タイトル>
- “Sustaining microglial reparative function enhances stroke recovery”
- <著者>
- Jun Tsuyama, Seiichiro Sakai, Kumiko Kurabayashi, Ayaka Nakamura, Eri Tanaka, Yuichiro Hara, Ito Kawakami, Makoto Tsuda, Takahiro Masuda, Marco Prinz, Hideya Kawaji, and Takashi Shichita
- <発表雑誌>
- Nature
DOI:https://doi.org/10.1038/s41586-026-10480-0
URL:https://www.nature.com/articles/s41586-026-10480-0
研究のポイント
- 脳卒中を起こして脳組織が損傷しても、失った脳機能を取り戻すための回復メカニズムが働くことを発見しました。
- 脳卒中患者さんの脳は、この回復メカニズムを発症2ヵ月程度で失ってしまいますが、その原因となる因子がZFP384というタンパク質であることを突き止めました。
- 研究チームはZFP384の働きを抑える薬(核酸医薬品)を開発し、回復メカニズムを失わせずに持続させられることを発見しました。
- 脳に備わっている「治る」ためのメカニズムを、失わせずに持続させられることから、脳の病気の後遺症を減らす(なくす)治療薬の開発が期待されます。
概要
脳が病気によって壊れると、手足が動かなくなる、言葉が話せなくなる等、脳機能を失います。しかし脳が壊れても、リハビリテーションなどによって、失った脳機能を部分的に取り戻すことができます。このような脳機能回復は多くの患者さんで見られますが、脳が壊れてから2ヵ月程度で回復力を失ってしまう(後遺症が残ってしまう)ことが知られていました。「どうして回復力を失ってしまうのか」、東京科学大学(Science Tokyo)総合研究院 難治疾患研究所 神経炎症修復学分野の津山淳助教と七田崇教授らの研究グループは、東京都医学総合研究所、九州大学、フライブルク大学(ドイツ)と共同で、この長年の謎に挑みました。
研究チームは今回、脳細胞が回復力を獲得して失うまでの一連のメカニズムを解明しました。脳細胞は脳が壊れた後、1ヵ月程度は回復力を持ち続けますが、次第に脳が正常な(脳が壊れる前の)状態に戻ろうとする影響を受けて、ZFP384(用語1)というタンパク質が作られることが分かりました。失った脳機能をまだ十分に回復できていないのに、ZFP384が脳細胞の回復力を失わせてしまっていたのです。
研究チームは、ZFP384の働きを防ぐ薬(アンチセンス核酸、用語2)を開発しました。これをマウスに投与すると、脳が壊れてから1週間後~1ヵ月後に治療開始した場合でも、回復力を失わせずに持続させられることを発見しました。本研究による成果は、「臓器に備わった自然な回復力を、失わせずに持続させられる」ことに成功したものです。これまで回復が困難とされてきた脳をはじめとして、臓器の機能を取り戻す治療法開発に新たな道を開くものです。
本成果は、5月13日付(英国時間)の「Nature」誌に掲載されます。
背景
日本や世界では高齢化社会の形成が進んでおり、脳の血管が詰まったり破れたりすることで起こる脳卒中は65歳以上の高齢者に多い病気です。脳卒中は認知症と並んで、要介護になる主要因であり、認知症を発症したり悪化させたりする原因になることもあります。脳卒中の約8割が脳梗塞という病気で、脳に血液が通わなくなり、酸素や栄養が不足することによって脳組織が死んで(壊れて)しまいます。脳には非常にたくさんの神経細胞があり、身体を動かす、物事を考えるなど、さまざまな脳機能を司っています。そのため神経細胞が死んでしまうと、手足が動かなくなる、言葉が出なくなるといった神経症状が現れ、死んだ神経細胞は元には戻らないため後遺症を残します。この後遺症が脳卒中患者さんを生涯にわたり苦しめ、医療・社会福祉にとっても大きな負担となっています。
本研究は、脳卒中の後遺症を減らす・なくすための治療薬を作る目的で行ったものです。脳卒中患者さんはリハビリテーションなどに取り組むことによって、失った脳機能を部分的に取り戻すことができます。しかし、どうして脳が治るのかは分かっていなかったため、治療薬を作ることが難しい状況が続いていました。
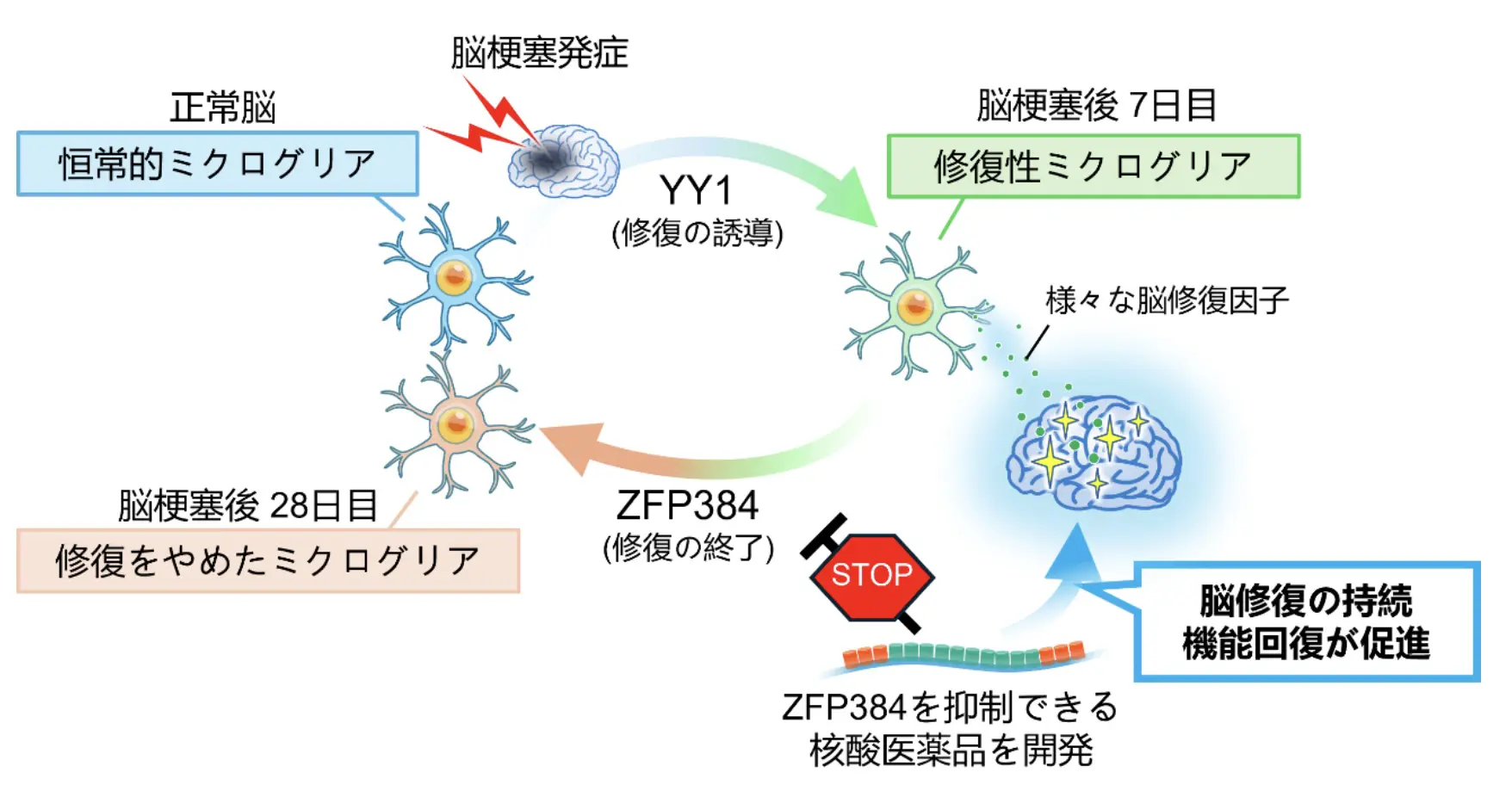
研究チームは、脳の中でお医者さんの役割を持つ、ミクログリア(用語3)と呼ばれる細胞に着目しました。ミクログリアはインスリン様成長因子1(略称:IGF1、用語4)などの神経栄養因子を分泌し、神経のつなぎ目(シナプス)を再構築したり、神経線維を覆う絶縁体(髄鞘)を修復したりします。ミクログリアは、脳卒中で壊れてしまった脳をどうやって治しているのか、本研究はこの重要な謎に挑みました。
研究成果
1. ミクログリアが脳を治すメカニズムを決定
IGF1は、ミクログリアが神経細胞を治すために作る栄養因子として有名ですが、正常な脳内では、ミクログリアはIGF1を作っていません。脳が壊れたことが引き金になって、ミクログリアはIGF1を作り始めますが、そのメカニズムは未解明でした。研究チームは特殊な遺伝子改変マウス(用語5)を使って、脳内でIGF1を作るミクログリアを蛍光で光らせ、脳梗塞を起こした脳から集めて調べることにより、ミクログリアが脳を治し始めるメカニズムを解明することに成功しました。ミクログリアはIGF1のほかにも、脳修復を促進する神経栄養因子(SPP1など)をたくさん作っていることが判明し、このようなミクログリアが回復力を獲得する引き金が、神経栄養因子を作らせるYY1(用語6)と呼ばれるタンパク質の働きであることを突き止めました。YY1は転写因子(用語7)と呼ばれる機能を持っており、遺伝子の発現をコントロールしています。YY1の働きを失わせると、ミクログリアは神経栄養因子を作ることができなくなりました。また、IGF1を作るミクログリアを脳から除去すると、脳梗塞後に本来見られるはずの自然な脳機能回復が認められなくなることが分かりました。
研究チームは、このようにミクログリアが壊れた脳を治すメカニズムを発見したのですが、この時にもう1つ重要な発見をしました。
2. ミクログリアは回復力を失っていく
脳卒中患者さんはリハビリテーションに取り組むことによって、失った脳機能を部分的に取り戻すことが可能ですが、発症2ヵ月程度で回復力が失われてしまい、残存した症状は生涯にわたる後遺症となります。マウスも同様で、ミクログリアは脳梗塞発症後、1ヵ月程度は神経栄養因子を作っていますが、2ヵ月後には回復力を失っていたのです。ここで、回復力を失った細胞がその後どうなるのかという疑問が生じました。すなわち、脳から消失するのか、それとも残存するのかという点です。
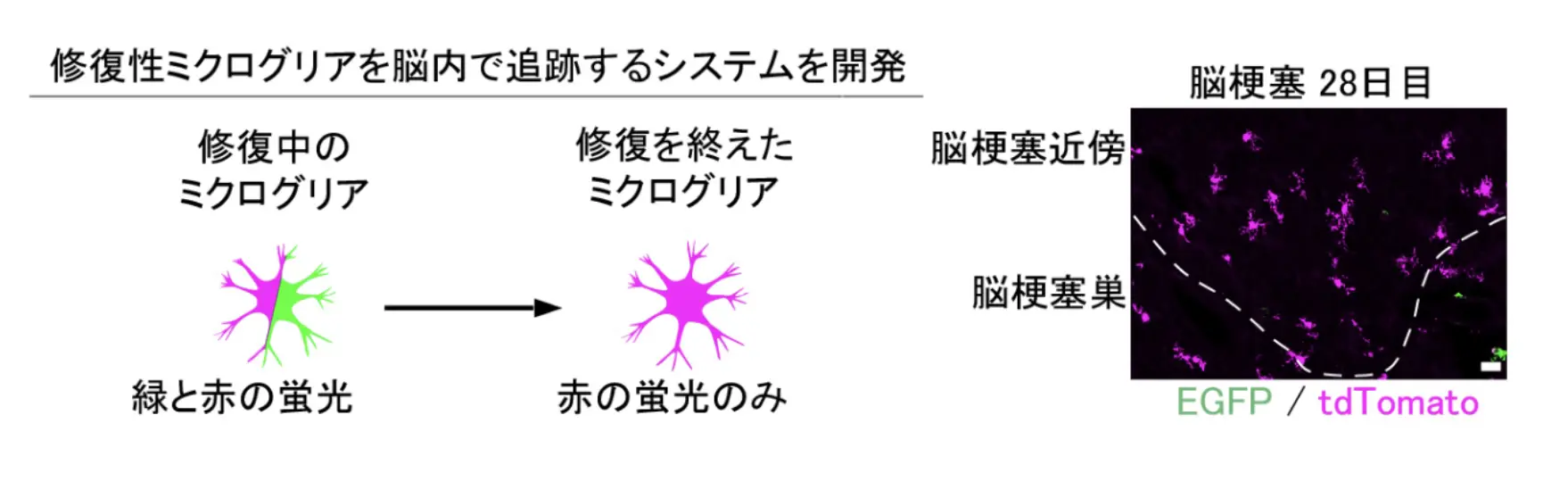
研究チームは、IGF1を作るミクログリアに「色の目印」を付与して追跡できるシステムを開発しました(図2)。IGF1を作っている時は緑色と赤色の両方に光り、作らなくなると赤色のみが光るという仕組みです。マウスが脳梗塞を発症して1ヵ月後の脳を解析したところ、赤色のみを示す細胞、すなわち回復力を失ったミクログリアを見つけたのです。このことから、回復力を獲得した脳細胞が死滅することによって、壊れた脳が回復力を失うのではないことが分かりました。ミクログリアが回復力を失うメカニズムを突き止めれば、失わせずに回復を持続させられる可能性が示唆されます。
3. ミクログリアが回復力を失うメカニズム
先に述べたように、ミクログリアに神経栄養因子を作らせるのはYY1という転写因子であったため、研究チームは神経栄養因子を作れないようにする転写因子を探しました。脳梗塞発症1ヵ月後にミクログリアで働いている、いくつかの転写因子の機能を調べていくと、ZFP384という転写因子がIGF1を作れないようにすることが分かりました。脳梗塞を発症して1ヵ月が経過すると、元の(脳が壊れる前の)状態に戻ろうとする働きが脳に生まれます。この働きは脳内でTGFβというタンパク質が増えることによってもたらされますが、TGFβには壊れた組織を傷跡に(瘢痕化)したり、脳の血管の状態を正常化したり、健常な脳の状態(恒常性)を保つ働きがあります。TGFβがミクログリアに作用すると、ZFP384を増やすことによってYY1の働きを止めることが分かりました。YY1が働かなくなって神経栄養因子を作れなくなり、ミクログリアを元の状態に戻してしまっていたのです。
ミクログリアがZFP384を作れないようにしたマウスを調べると、脳梗塞発症1ヵ月後もミクログリアが神経栄養因子を作り続けるようになり、神経症状が顕著に改善しました。以上の発見は、ZFP384の働きを阻害する薬を作ることができれば、ミクログリアの回復力を失わせずに持続させられることを意味しています。
4. ASO-Zfp384は脳の回復力を持続させる
そこで研究チームは、ZFP384の働きを阻害する薬の開発に取り組みました。アンチセンス核酸は、特定の遺伝子のみに作用して阻害することが知られており、脳の難病を治す薬としての応用が期待されています。ZFP384を阻害するアンチセンス核酸(ASO-Zfp384)を創り出すことができたため、脳梗塞を発症したマウスに発症1週間後、または発症1ヵ月後に投与したところ、神経症状の改善を認めることができました(図3)。ASO-Zfp384を脳室内に投与(用語8)すると、発症1ヵ月後もミクログリアが神経栄養因子を作り、回復力を維持できていることが分かりました。また、神経のつなぎ目(シナプス)や神経線維を覆う絶縁体(髄鞘)の回復が促進されることによって、神経症状の改善が認められたことが分かりました。
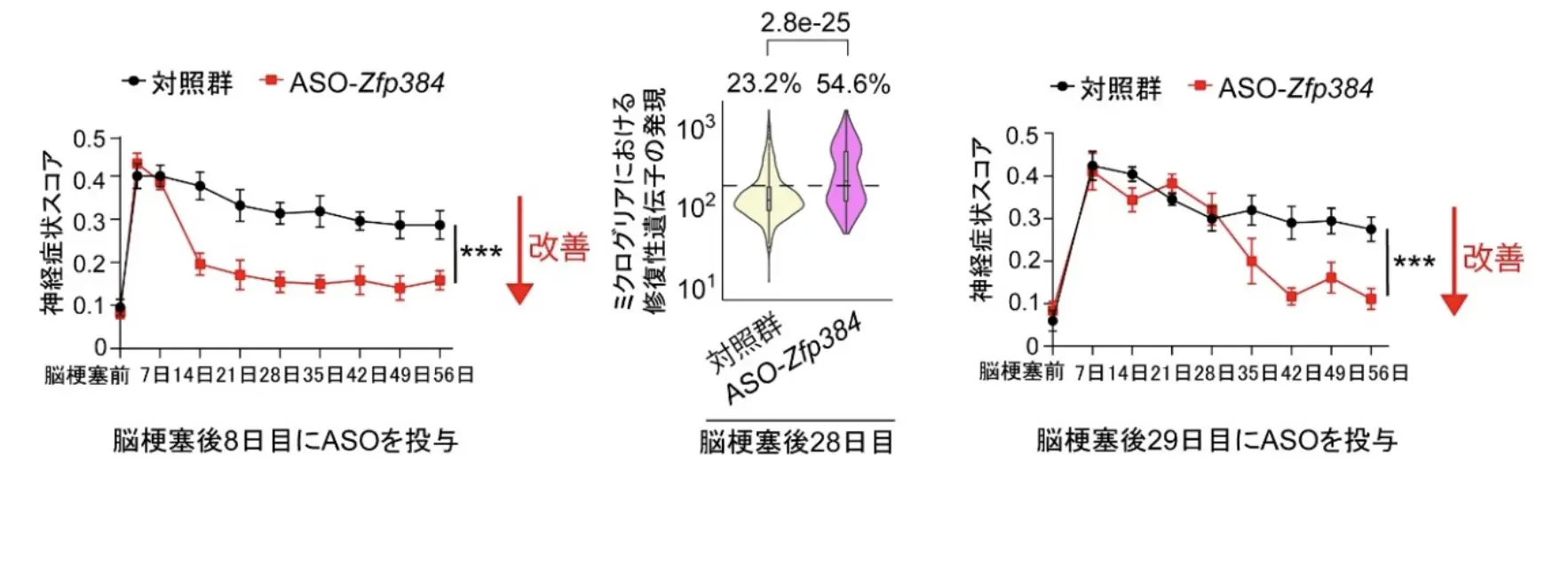
(中央図)ASO-Zfp384によって神経栄養因子など、修復性遺伝子の発現を持続促進できる。
5. 脳梗塞患者における検証
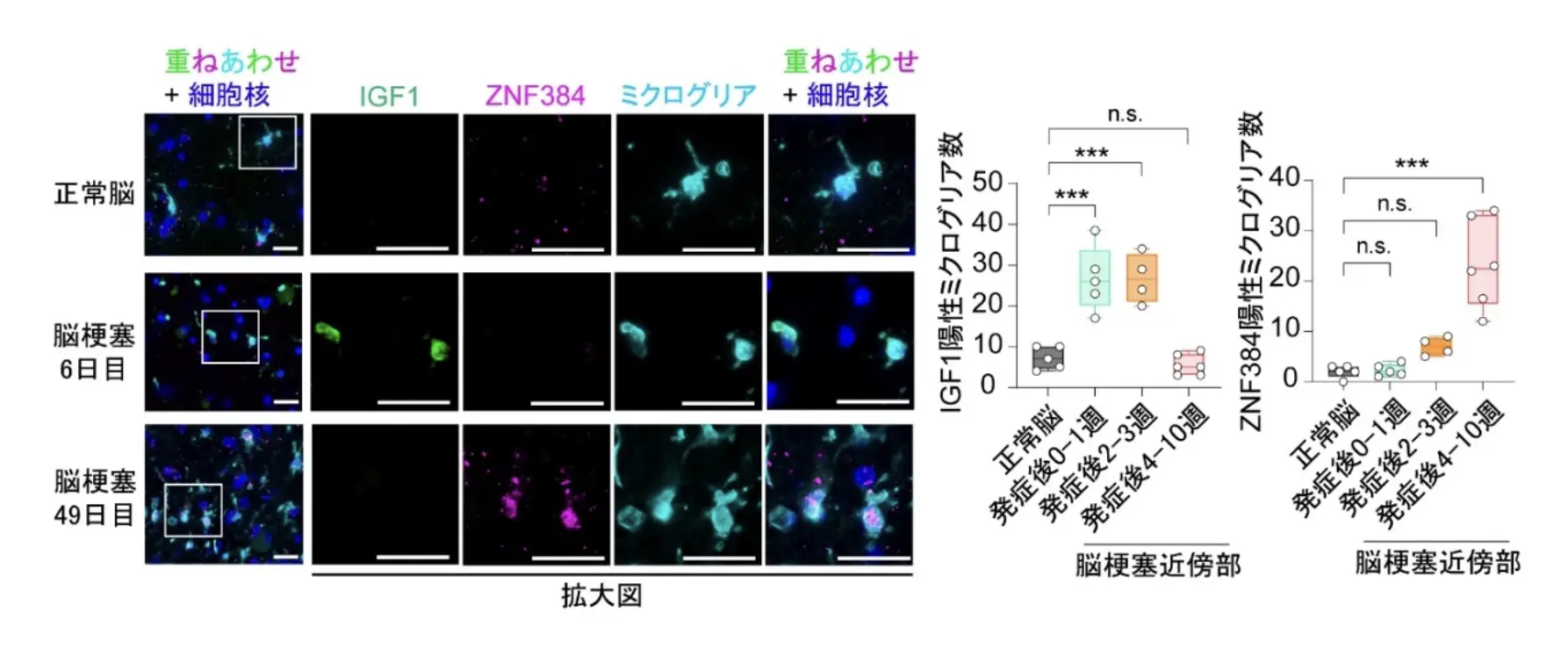
脳梗塞後に死亡した患者さんの剖検脳を解析したところ、発症1週間後の脳内にはIGF1を作るミクログリアを多く認めましたが、発症1~2ヵ月後にかけて時間の経過とともに減少し、患者さんにおいてもミクログリアが回復力を失っていくことが分かりました。また、代わりにミクログリアはZFP384(ヒトではZNF384と呼ぶ)を発現していることが分かりました。脳梗塞患者さんでは、IGF1とZFP384が時間と共に逆相関して発現していることを示しており、マウスと同様の変化が観察されたと考えられます(図4)。
社会的インパクト
脳卒中を発症すると、まだ回復が十分ではないのに、脳が回復力を失ってしまい、後遺症が残ってしまいます。脳に自然に備わった回復力を促進させる治療法の開発が期待されていますが、どうして失った脳機能を取り戻すことができるのかはまだ詳しく分かっていませんでした。本研究はミクログリアが回復力を獲得して失うまでの一連のメカニズムを解明したもので、ミクログリアの回復力を失わせずに持続させられる薬剤を創り出せた点で革新的です。アンチセンス核酸は神経難病の患者さんにも投与されている薬剤で、本研究が開発したASO-Zfp384は、脳梗塞発症後1週間~1ヵ月が経過してから投与した場合でも治療効果を示しました。脳卒中を発症して1週間~1ヵ月後は、患者さんが入院して集中治療を受けた後、病状が落ち着いてリハビリテーションを専門とする病院に転院する時期に当たります。この時期に投与して、脳に備わった自然な回復力を持続促進する薬剤の開発に成功したことから、後遺症を減らす・なくすための画期的な医薬品を創り出すコンセプトを確立することができました。
脳は治らない臓器だと考えられがちですが、強い回復力を持っていることが本研究で証明されました。臓器に備わった自然な回復力を失わせずに持続させ、機能を回復させる医薬品開発のコンセプトが世界に普及してほしいと考えています。
今後の展開
ASO-Zfp384は、脳卒中後の後遺症を減らす薬になることが期待されます。薬の開発には、副作用を減らす、薬効を高める等、時間をかけて改良を重ねる必要があります。また、脳卒中以外の脳の病気にも治療効果が期待できるのかどうかも興味深く、今後も研究を進めていきたいと考えています。
付記
本研究は、日本医療研究開発機構(AMED)の革新的先端研究開発支援事業AMED-CREST「生体組織の適応・修復機構の時空間的解析による生命現象の理解と医療技術シーズの創出」、文部科学省科学研究費助成事業 学術変革領域研究(A)「リカバロミクス」(JP26H00476)、「グリアデコード」(JP23H04181)、基盤研究(A)(JP24H00626)、基盤研究(C)(JP21K06386、23K05626)、東レ科学技術研究助成、武田科学振興財団、上原記念生命科学財団、光科学技術研究振興財団、MSD生命科学財団、千里ライフサイエンス振興財団、小野薬品がん・免疫・神経研究財団、公益信託美原脳血管障害研究振興基金、ならびに東京科学大学の高深度オミクス医学研究拠点整備事業、難治疾患共同研究拠点、学際領域展開ハブ形成プログラム「多階層ストレス疾患の克服」の支援を受けて実施されました。
用語解説
- [1] ZFP384:
- DNAに結合して遺伝子の発現を調節する転写因子としての機能を持つタンパク質。本研究で、ミクログリアの回復力を失わせる働きを持つことを発見した。ヒトではZNF384と呼ばれる。
- [2] アンチセンス核酸(ASO):
- 特定の遺伝子の働きを抑えるために設計された短い核酸の薬。標的の遺伝子から作られるメッセンジャーRNAに結合して分解を促すことで、そのタンパク質が作られないようにする。
- [3] ミクログリア:
- 脳に常在する免疫細胞。普段は脳の環境を見守り、脳がダメージを受けると活性化して炎症を起こすが、1週間ほどで炎症を収束させて修復を助ける細胞に変わる。IGF1などの神経栄養因子を作って脳機能を回復させる。
- [4] インスリン様成長因子1(IGF1):
- 神経の成長や修復を助ける物質。シナプス(神経のつなぎ目)の形成や、髄鞘(神経の絶縁体)の再生を促し、脳機能の回復に重要な役割を果たすことが本研究で明らかとなった。
- [5] 遺伝子改変マウス:
- 本研究では、遺伝子を操作して特定の細胞だけを光らせたり、除去したりできるように操作したマウスを用いた。
- [6] YY1:
- DNAの離れた部分をループ状につなげて、遺伝子の発現をコントロールする役割を持つタンパク質。本研究で、修復遺伝子の活性化に必要であることが示された。
- [7] 転写因子:
- 細胞の中で、どの遺伝子を働かせるかを指示するタンパク質。DNAに直接結合して、必要な遺伝子の発現を促したり、止めたりする。本研究では、YY1が脳機能回復に必要な遺伝子を働かせ、ZFP384がその働きを止める役割を持つ。
- [8] 脳室内投与:
- 脳の中には「脳室」と呼ばれる液体(脳脊髄液)で満たされた空間があり、ここに薬を注入する方法。脳室に投与された薬は脳脊髄液を通じて脳全体に届く。脳脊髄液は脳室から脊髄まで一続きにつながっているため、ヒトでは腰から針を刺して脳脊髄液に薬を届ける方法(髄腔内投与)も広く用いられている。実際に、アンチセンス核酸を髄腔内投与する治療法は神経難病の患者さんにすでに実用化されている。
