HOME > Oct 2019 No.035

Oct. 2019 No.035
特集
Topics
開催報告
受賞報告
編集後記
Topics
ウイルス感染を抑制する新たな肝細胞の自然免疫の仕組みを発見
感染制御プロジェクトの山根大典首席研究員らは「ウイルス感染を抑制する新たな肝細胞の自然免疫シグナルの仕組み」について英国科学雑誌「Nature Microbiology」に発表しました。
感染制御プロジェクト 主席研究員山根 大典
肝炎ウイルスやデングウイルス等の病原体は、ヒトの肝細胞に感染し増殖することで急性・慢性肝炎を引き起こし、肝機能障害や肝癌の原因となることが公衆衛生上重要な問題となっています。肝臓組織を構成する肝細胞は本来、ウイルス複製を抑制する自然免疫機構を持ちますが、その詳細な仕組みについては不明な点が多く残されています。
私たちは、肝細胞においてウイルスの増殖を抑制する宿主因子を解明するため、抗ウイルスシグナル経路を構成する一連の遺伝子の機能を詳細に調べました。その結果、基底レベルで発現しているインターフェロン制御因子※(IRF1)が多くの抗ウイルス因子群の発現を恒常的に維持することでウイルス感染を強力に抑制していることを発見しました。
これまでの報告では、RIG-I様受容体やToll様受容体と呼ばれる病原体特有のパターン構造を認識する受容体が侵入したウイルスを感知することで抗ウイルス応答を活性化し、抗ウイルス遺伝子の発現を誘導することでウイルス増殖が抑制されると考えられてきました。ところが意外なことに、これらのウイルス感染に応答して活性化するシグナル経路は、肝細胞においてはウイルス増殖の抑制にほとんど寄与していないことがわかりました。
さらにIRF1 は肝炎ウイルスのみならず、デングウイルスやジカウイルスを含む重要なヒト病原体についても幅広く抑制する機能を持つことを明らかにしました。IRF1 は転写因子として様々な遺伝子の発現誘導を制御しますが、私たちはこれまでに抗ウイルス活性を持つことが知られていない脂質代謝酵素、免疫プロテアソーム構成分子やペプチダーゼ遺伝子を含む51のIRF1 制御遺伝子群を同定し、多くの遺伝子がIRF1 の抗ウイルス機能を介在していることがわかりました。これらのIRF1制御遺伝子の中でも、異なるウイルスに対して普遍的に抑制作用を持つ遺伝子だけでなく、特定のウイルスにのみ作用する遺伝子が存在することを明らかにし、IRF1 が広範なウイルスに対して強力な抑制効果を持つ機序を見出しました。
この研究により、これまで重要と考えられていたウイルス感染応答性のシグナルではなく、IRF1 による「基底レベル」で維持されている抗ウイルスシグナルが強力にウイルス増殖を制御するという、新たなウイルス制御モデルを提唱しました(図1)。今後の展開として、IRF1 制御遺伝子の作用機序を詳細に解明することにより、IRF1 の機能を模倣する新たな抗ウイルス剤の開発を目指して研究を進めています。また、様々な培養細胞において強力なウイルス抑制作用を持つIRF1 の機能をノックアウトすることにより、これまで培養が困難であった病原体の細胞培養法や、それを用いたウイルス治療薬の薬剤スクリーニング系の開発へと繋がることが期待されます。
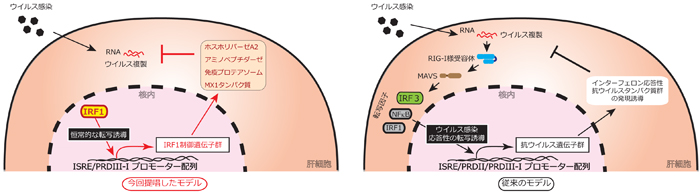
図1
用語解説
- ※インターフェロン制御因子:
- 抗ウイルス遺伝子の転写制御を司る転写因子。ヒト細胞においてはIRF1からIRF9という9つのファミリーが存在し、ISREやPRD-I、PRD-IIIと呼ばれる特定の宿主DNA配列に結合することで標的遺伝子の発現を誘導します。

