
2017年3月1日
米国科学誌「Cellular and Molecular Gastroenterology and Hepatology」に感染制御プロジェクト 真田 崇弘 研究員が 「B型肝炎ウイルスの新規感染経路の発見」 について発表しました。
B型肝炎ウイルスの感染に細胞外小胞を利用した経路が存在することを発見
B型肝炎ウイルス(HBV)は、ヒトに持続感染することで、慢性的な肝炎を引き起こし、やがては肝硬変・肝細胞癌を引き起こします。現在、HBV感染に対する有効なワクチンはありますが、ワクチン接種者であってもHBVに感染する事例が報告されています。そのため、ワクチン免疫を回避するメカニズムの存在があるものと考えられ、そのメカニズムの解明および対策が求められていました。今回の研究では、細胞間の情報伝達に関与している細胞外小胞に着目し、HBVが細胞外小胞に包まれることで、宿主からの免疫機構から回避しているのではないかと考え、ヒトの初代培養肝細胞を用いて、解析を行いました。その結果、細胞外小胞にはウイルスの遺伝子およびHBcタンパク質が内包されていることが明らかとなり、またウイルスとしての感染性をもつことがわかりました。さらに、HBVを内包した細胞外小胞の感染は、HBVに対する中和抗体では阻害できませんでした。以上の結果から、これまで知られていたウイルス粒子の産生・感染経路とは別の細胞外小胞を介したHBVの産生・感染経路が見出されました。本研究から、HBVのHBsタンパク質を標的とした現在のワクチン戦略では、HBV感染に対して不充分であると考えられ、細胞外小胞を介した感染経路を阻害することで、より予防効果の高いワクチン開発に繋がるものと考えられます。
- <発表雑誌>
- Cellular and Molecular Gastroenterology and Hepatology
- <論文タイトル>
- Transmission of HBV DNA Mediated by Ceramide-Triggered Extracellular Vesicles
PDF
本研究成果は、2017年3月1日、米国科学雑誌 「Cellular and Molecular Gastroenterology and Hepatology」 に掲載されました。
1.研究の背景
B型肝炎ウイルス(HBV)は、ヒトに持続感染することで、慢性的な肝炎を引き起こし、やがては肝硬変・肝細胞癌を引き起こします。全世界においておよそ3億5千万人もの慢性HBV感染者がいると考えられていますが、いまだB型肝炎を根治する治療法は存在しておらず、公衆衛生学上、重要な問題となっています。
現在、HBV感染に対する有効なワクチンはありますが、ワクチン接種者であってもHBVに感染する事例が報告されています。そのため、ワクチン免疫を回避するメカニズムの存在があるものと考えられ、そのメカニズムの解明および対策が求められていました。
2.研究の概要
我々は、細胞間の情報伝達に関与している *細胞外小胞に着目し、HBVが細胞外小胞に包まれることで、宿主からの免疫機構から回避しているのではないかと考え、ヒトの初代培養肝細胞を用いて、解析を行いました。
その結果、以下の点が明らかとなりました。
- 細胞外小胞にはウイルスの遺伝子およびHBcタンパク質が内包されているが、外殻タンパク質であるHBsタンパク質は内包されていなかった。
- HBVを内包した細胞外小胞は、ヒトの初代培養肝細胞に感染し、ウイルスの複製がみられた。
- HBVを内包した細胞外小胞の感染は、HBVに対する中和抗体では阻害できなかった。
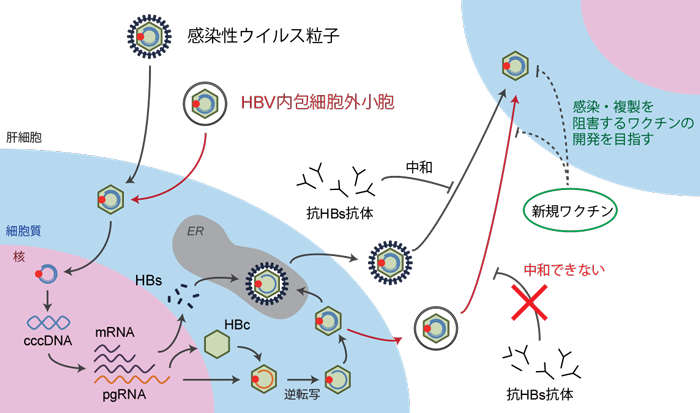
以上の結果から、細胞外小胞の中にはHBVのウイルス粒子そのものではなく、コア粒子として内包されているものと考えられます。これまで知られていたウイルス粒子の産生・感染経路とは別の細胞外小胞を介したHBVの産生・感染経路が見出されました。
3.今後の展望
本研究により、HBVのHBsタンパク質を標的とした現在のワクチン戦略では、HBV感染に対して不充分であると考えられました。細胞外小胞を介した感染経路を阻害することで、より予防効果の高いワクチン開発に繋がることが期待されます。
用語解説
- *細胞外小胞:
- 細胞より分泌される小胞で、miRNAなどの核酸や蛋白質を内包しており、これらを別の細胞へと輸送することで、細胞間のコミュニケーションに重要な役割を担っています。


