
2017年5月19日
米国科学誌 「Molecular Cell」 に蛋白質代謝研究室の土屋光研究員らが 「ユビキチン化基質がプロテアソームに運ばれる仕組み」 について発表しました。
ユビキチン化基質がプロテアソームに運ばれる仕組み ~疾患の発症機構解明につながることを期待~
(公財)東京都医学総合研究所・蛋白質代謝研究室の土屋光研究員、大竹史明主席研究員、田中啓二所長、佐伯泰副参事研究員らは、定量プロテオミクス解析により細胞内におけるユビキチンシグナルの使い分けを明らかにすると共に、プロテアソームで分解される基質タンパク質の大部分がCdc48/p97とRad23により運ばれていることを明らかにしました。本研究成果は、ユビキチン・プロテアソーム系が関与する疾患の発症機構解明や治療に役立つことが期待されます。
本研究は、日本学術振興会科研費(新学術領域研究、特別推進研究)および(公財)武田科学振興財団、(公財)住友財団の研究助成により実施しました。本研究成果は2017年5月18日に米国科学誌 「Molecular Cell」 に掲載されました。
- <発表雑誌>
- 米国科学誌 「Molecular Cell」 (2017年5月18日 掲載)
- <論文タイトル>
- “In Vivo Ubiquitin Linkage-type Analysis Reveals that the Cdc48-Rad23/Dsk2 Axis Contributes to K48-linked Chain Specificity of the Proteasome.
(Cdc48-Rad23/Dsk2軸がプロテアソーム依存的タンパク質分解の主要経路である)
1.研究の背景
ユビキチンは酵母からヒトまで保存された小さなタンパク質です。ユビキチンの主な役割は、標的となるタンパク質に「目印」として付加され (ユビキチン化)、タンパク質の運命を決定することです。ユビキチンが目印として付加された不要なタンパク質や異常タンパク質はプロテアソーム (*1)により認識され速やかに分解・除去されます。一方で、ユビキチンは膜タンパク質の輸送、細胞内の情報伝達、DNA損傷の修復などの目印にもなることがわかっており、多彩な機能を発揮することが近年分かってきました。ユビキチンの機能が損なわれるとがんや免疫疾患、パーキンソン病やアルツハイマー病などの神経変性疾患の発症につながると考えられており、ユビキチン研究は基礎研究だけでなく臨床面からも注目を集めています。
ユビキチンが細胞内で様々な現象の目印となることができる理由として、ユビキチンが多様な構造をとることがあげられます。ユビキチンは多くの場合、ユビキチン同士が連結することで数珠状のユビキチン鎖を形成します。ユビキチンには連結できる場所が8か所あるため、それぞれが異なる構造のユビキチン鎖(K6 鎖、K11鎖、K27鎖、K29鎖、K33鎖、K48鎖、K63鎖およびM1 鎖)を形成し、独自の目印として機能します。これらの異なる構造のユビキチン鎖はそれぞれ特有のデコーダータンパク質に識別され、下流の分子に情報が伝えられると考えられていますが、細胞内に数多く存在するデコーダータンパク質がどのタイプのユビキチン鎖を認識しているのか、どのように使い分けられているのかということはあまりよくわかっていませんでした。
2.研究の概要
私たちはモデル生物である酵母の主要なユビキチン結合タンパク質について、細胞内でどの種類のユビキチン鎖を認識しているのか質量分析計を用いて網羅的に定量解析しました(図1)。その結果、それぞれのデコーダータンパク質に結合するユビキチン鎖の種類は機能と相関した選択性をもつことがわかりました。すなわちプロテアソーム分解に関与するユビキチン結合タンパク質はK48鎖、タンパク質輸送に関与するものはK63鎖に対して選択性をもつことがわかりました。一方で、オートファジーとMVB経路(*2)に関与するものはK48鎖とK63鎖の両方を認識できることがわかりました。プロテアソームの機能を低下させると、全てのユビキチン依存的経路が変動したことから、プロテアソームの活性はユビキチンネットワーク全体に影響を与えていることが明らかとなりました。
次に、プロテアソームによるタンパク質分解経路に着目しました。その結果、これまでプロテアソームはユビキチン化されたタンパク質を直接認識していると考えられていましたが、細胞内ではユビキチン依存的シャペロンのCdc48/p97(*3)とシャトリングタンパク質Rad23/Dsk2を介した間接的な経路が主要であることが初めて分かりました(図2)。
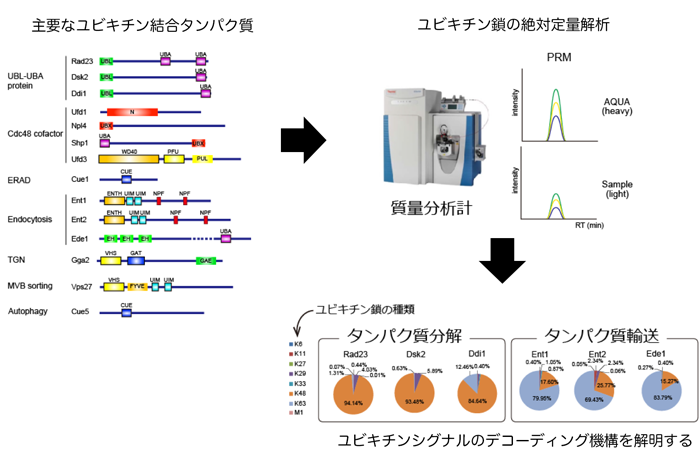
図1. デコーダー分⼦が認識するユビキチン鎖の網羅的解析
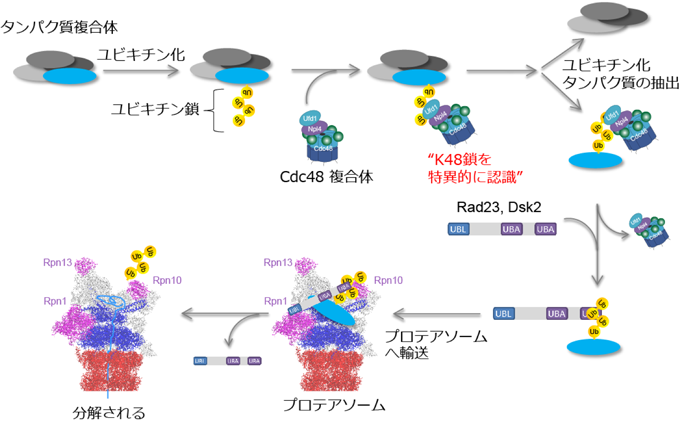
図2. プロテアソームによるタンパク質分解経路の全体像
3.今後の展望
ユビキチン・プロテアソーム系の破たんはガンや神経変性疾患と密接に関わっており、プロテアソームを標的とした阻害剤はすでに血液がん治療薬として用いられています。ユビキチン結合タンパク質はヒトでは150種類以上と多様であり、ユビキチン結合タンパク質が繋ぐユビキチンネットワークの解明は、将来的に疾患の発症機構解明や薬剤開発の基盤となることが期待されます。
用語解説
- *1 プロテアソーム:
- 細胞内の不要なタンパク質を分解する巨大な酵素複合体。ユビキチンが付加されたタンパク質を選択的に分解することにより様々な生命現象を制御している。
- *2 MVB経路:
- 小胞輸送により他のオルガネラなどからタンパク質がMVBs (multivesicular bodies) に送りこまれ、リソソームに輸送されるタンパク質の輸送経路。
- *3 Cdc48/p97
- Cdc48/p97はAAA+タイプのユビキチン選択的シャペロン分子である。小胞体関連タンパク質分解経路などのタンパク質品質管理に関与することがしられている。


