HOME > 広報活動 > 刊行物 > January 2014 No.012

January 2014 No.012
特集
研究紹介
トピックス
開催報告
編集後記
研究紹介
血小板膜上の微小領域における血栓形成の仕組みを解明
米国科学雑誌「Blood」に細胞膜研究室の笠原浩二研究員らの研究成果が発表されました。
細胞膜研究室 副研究室長笠原 浩二
血栓性疾患(心筋梗塞、脳梗塞など)は東京都民の最大の死亡原因の一つであることから、血栓形成の基礎研究は新たな治療戦略に道筋をつけるうえで重要です。血管内で血液凝固反応が開始されると血小板は凝集し、フィブリン網とともに血栓を形成します。血小板は血栓の主要な細胞成分であり、その表面が血液凝固因子の活性化の場となることから、血栓形成開始時において先導的な役割を果たしています。最近、細胞膜は均等に分布しているのではなく、偏った脂質成分が集合した微小領域が存在し、様々な生命活動を調節していることが分かってきました。
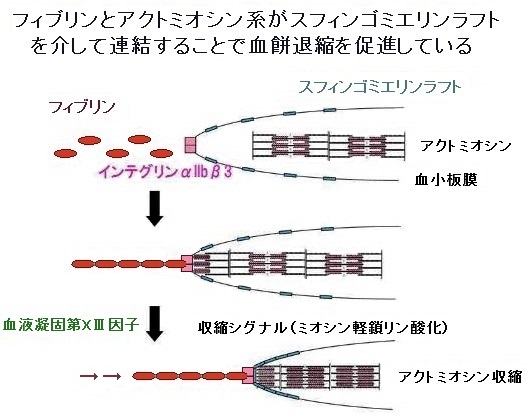
止血血栓形成の際に、フィブリンと血小板からなる血栓が収縮する血餅退縮という現象が知られています。血小板の働きにより収縮し血管の切断端を引き寄せ、強固な血栓を形成します。フィブリン線維が血小板表面上の受容体(インテグリンαIIbβ3)に結合し、その内側に細胞骨格(アクトミオシン)が連結し、筋肉と似た仕組みで収縮することによっておこると考えられています。私達は、フィブリン線維と細胞骨格の連結が血小板膜上で一様におこるのではなく、血小板膜脂質であるスフィンゴミエリンとコレステロールが集合した「脂質ラフト」と呼ばれる微小領域で起こることにより収縮に必要な細胞内シグナル伝達(ミオシン軽鎖リン酸化)を可能にし、効率よく血餅退縮をおこしていることを明らかにしました。さらに、フィブリンが脂質ラフトに結合し血餅退縮をおこすためには、血液凝固第XⅢ因子が必要であることがわかり、本研究は血液凝固第XⅢ因子の新しい機能を示しました。
本研究から、血小板膜上の微小領域である脂質ラフトによる血餅退縮促進の仕組みが明らかになりました。したがって、ラフトを構成する脂質や血液凝固第XⅢ因子を標的とした、血栓性疾患における新たな検査法や治療法の開発につながることが期待されます。
Kasahara K, Kaneda M, Miki T, Iida K, Sekino-Suzuki N, Kawashima I,Suzuki H , Shimonaka M, Arai M, Ohno-Iwashita Y, Kojima S, Abe M, Kobayashi T, Okazaki T, Souri M, Ichinose A, and Yamamoto N(2013)
Clot retraction is mediated by factor XⅢ-dependent fibrin-αⅡbβ3-myosin axis in platelet sphingomyelin-rich membrane rafts.
Blood.122:3340-3348
doi:10.1182/blood-2013-04-491290