Apr. 2020 No.037
特集
Topics
開催報告
受賞報告
編集後記
Topics
ユビキチンは、ミトコンドリア - ペルオキシソーム間の輸送シグナルとして機能する
ユビキチンプロジェクトの小谷野史香 主任研究員及び松田憲之 副参事研究員らは「ユビキチンがミトコンドリア - ペルオキシソーム間輸送シグナルとして機能する」について「EMBO Reports」に発表しました。
ユビキチンプロジェクト 主任研究員小谷野 史香
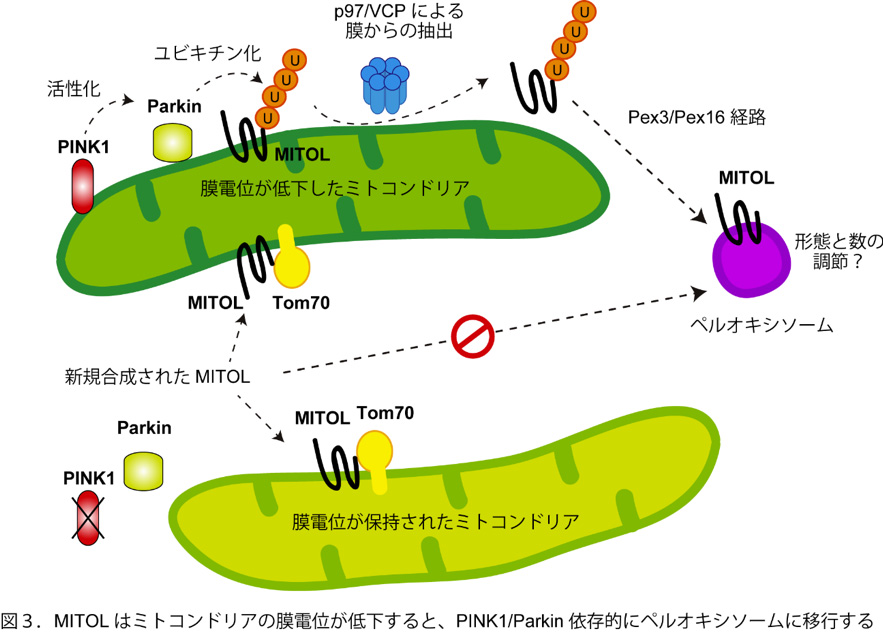
私たちのグループでは、遺伝性パーキンソン病の原因遺伝子産物であるPINK1 (Ser/Thr kinase) とParkin(Ubiquitin ligase: E3) が、低品質なミトコンドリアをユビキチン化して除去することで、ミトコンドリアの品質管理を行うことを示してきました (Matsuda et al, JCB, 2010)。さらに、この過程において、PINK1 がユビキチンをリン酸化することや、リン酸化ユビキチンがParkinを活性化することを明らかにしました (Koyano et al,Nature, 2014)。これらの研究を進める過程で私たちは、ミトコンドリアの膜電位が低下した状態が継続すると、E3 であるMITOL/March5 の局在がミトコンドリア外膜からペルオキシソームに変化する現象を見出しました(図)。この現象はミトコンドリアの膜電位低下に加えて、PINK1 とParkin の活性に依存することが判明しました。複数の解析結果から、Parkin によってMITOL/March5 がユビキチン化されると、これがシグナルとなり、MITOL/March5 がミトコンドリアからp97/VCP によって引き抜かれて、Pex3, Pex16 依存的にペルオキシソームに輸送されることを初めて明らかにしました (Koyano et al, EMBO Rep., 2019)。このように、膜蛋白質が不良なミトコンドリアからペルオキシソームへと輸送され、さらにその過程でユビキチン化という翻訳後修飾がシグナルとして機能するという新たな仕組みを見出しました。
AAA ATPase であるp97/VCP は、複数のcofactorと協調して標的蛋白質上のユビキチン鎖を認識し、膜から蛋白質を抽出することが知られています。今後は、本研究で得られた知見をもとに、「ミトコンドリア膜からMITOL/March5 が選択的に引き抜かれる現象」が、p97/VCP cofactor のどの分子に依存するのか調べたいと考えています。また、ペルオキシソームに輸送されたあとに、MITOL/March5 が果たす役割を調べることで、遺伝性パーキンソン病の発症を抑制する過程で起きる現象の新たな一面が見えてくるかもしれません。