
2014年7月3日
米国科学誌「Annals of Clinical and Translational Neurology」にパーキンソン病プロジェクトの 橋本款副参事研究員、関山一成研究員らの研究成果が発表されました。
パーキンソン病モデルにおけるアディポネクチンの治療効果について
Disease modifying effect of adiponectin in model of α-synucleinopathies
近年、糖尿病や動脈硬化などの中年期以降における慢性疾患が弧発性のアルツハイマー病やパーキンソン病などの神経変性疾患の増悪に関係しているという見解が支持されていますが、そのメカニズムは必ずしも明らかではありません。
橋本款副参事研究員、関山一成研究員らの論文は、抗糖尿病因子として知られているアディポネクチンがシヌクレイノパチーなどの神経変性疾患の新しい治療薬になる可能性を細胞及びマウスモデルを使って示した前臨床的実験結果であり、神経変性疾患の治療の分野に貢献することができるのではないかと考えています。
1.研究の背景
パーキンソン病 (PD)※1は臨床的に、安静時振戦、筋強剛、寡動および姿勢反射障害などパーキンソニズムとよばれる運動機能障害を呈し、病理学的には、中脳黒質のドパミン神経におけるα-シヌクレイン(αS)※2の蓄積・凝集、それに伴うドパミン神経の変性・脱落やレビー小体とよばれる細胞内封入体の形成を特徴とする神経変性疾患です。
パーキンソン病 (PD)は、その大部分が高齢者に発症し、アルツハイマー病(AD)に次いで頻度の高い神経変性疾患であり、高齢化が進む現代社会において患者数は増加し、その莫大な医療費や介護に伴う支出は大きな問題となっています。 それにもかかわらず、現状では有効な予防法や根治療法は無く、その開発は医学研究の急務の一つと言っても決して過言ではありません。
近年、多くの研究により、II型糖尿病や動脈硬化などの生活習慣病がパーキンソン病 (PD)を含む神経変性疾患に対して危険因子となること、また、蛋白分解系やミトコンドリアの異常などの様々な病態が神経変性疾患とII型糖尿病との間に共通することがわかってきました。 これらのことから、我々は、パーキンソン病 (PD)やアルツハイマー病(AD)などの神経変性疾患とII型糖尿病や動脈硬化との間に共通の治療ターゲットが存在するのではないかと考え、抗糖尿病・抗動脈硬因子として知られているアディポネクチン(APN)※3に着目しました。
2.研究成果の要点
パーキンソン病 (PD)および、その近縁疾患(シヌクレイノパチー)※4であるレビー小体型認知症(DLB)の患者様の死後脳をアディポネクチン(APN)に対する抗体を用いて免疫染色した結果、レビー小体にアディポネクチン(APN)の陽性像を確認し(図1)、アディポネクチン(APN)がシヌクレイノパチーの病態に関与している可能性が示唆されました。
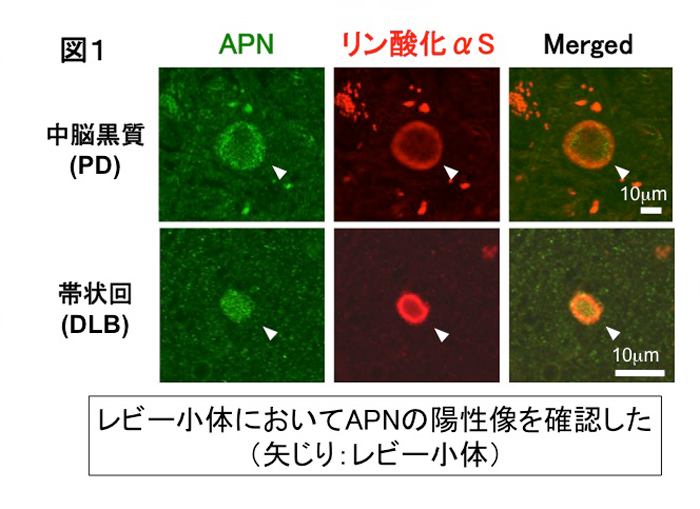
そこで、シヌクレイノパチーに対するアディポネクチン(APN)の効果をシヌクレイノパチーモデル(培養細胞・トランスジェニックマウス)を用いて検討した結果、 i) α-シヌクレイン(αS)を恒常的に発現したB103神経芽細胞においてアディポネクチン(APN)はその受容体(AdipoR1)を介してAMPキナーゼを活性化させることで α-シヌクレイン(αS)の凝集を抑制しました。また、様々な神経毒性に対しアディポネクチン(APN)が神経保護的に作用することがわかりました。 ii)さらに、α-シヌクレイン(αS)を発現したトランスジェニックマウスに対して、アディポネクチン(APN)のC末端部分の球状ドメインを若い時から長期間鼻粘膜投与することにより、α-シヌクレイン(αS)を発現したマウスの神経病理や運動機能試験の成績が有意に改善する事を観察しました(図2)。
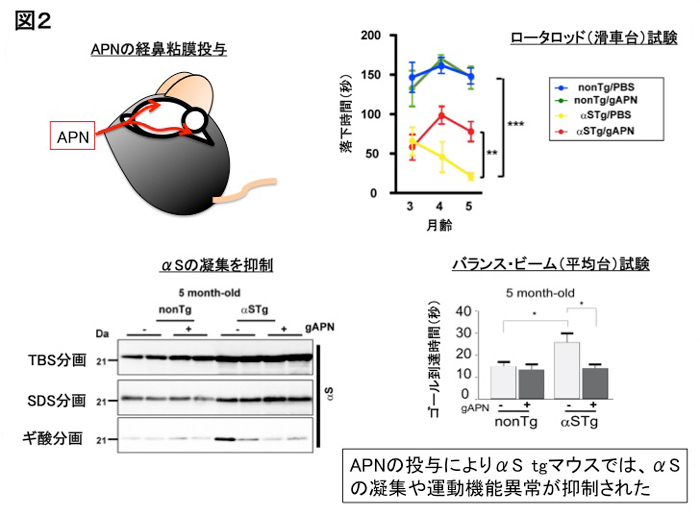
3.発見の意義
本研究により、マウスモデルに対するアディポネクチン(APN)の投与によって、α-シヌクレイン(αS)の凝集や運動機能障害が抑制されるなど、アディポネクチン(APN)がシヌクレイノパチー病態を改善することが示されました。今後、アディポネクチン(APN)の抗神経変性作用の詳細なメカニズムを解明し、近い将来、パーキンソン病(PD)やレビー小体型認知症(DLB)などの予防、あるいは根治療法の開発に繋がることが期待されます。また、これらの知見は、アルツハイマー病(AD)や筋委縮性硬化症(ALS)など他の神経変性疾患にも適応できる可能性があるのではないかと考えています。
【用語説明および補足】
- ※1 パーキンソン病(PD):
- パーキンソン病(PD)は、特定の遺伝子の変異が原因となる家族性(若年性)パーキンソン病と様々な遺伝的および環境的要因で発症する弧発性パーキンソン病に別けられますが、大部分(90~95%)は高齢期に発症する弧発性パーキンソン病です(Sekiyama et al, Biochem Biophys Res Commun. Review 2014)。パーキンソン病(PD)はアルツハイマー病(AD)に次いで頻度の高い神経変性疾患であり、日本では人口10万人あたり100~150名の患者がいます。現時点で有効な根治療法はなく、神経細胞の脱落により不足したドパミンをレボドパ(L-dopa)など薬剤によりドパミンの作用を補充する対症療法が主となっています。レボドパの服用により運動機能は劇的に回復しますが、長期間の投与によりレボドパの効く時間が短くなってしまいます。また、レボドパの量を増やすとジスキネジアと呼ばれる不随意運動があらわれる副作用が生じることが知られています。そのため、パーキンソン病(PD)の効果的な予防法や根治療法の確立が待ち望まれています。
- ※2 α-シヌクレイン(αS):
- 神経の前シナプスに豊富に存在する凝集しやすいタンパク質で、その生理的な機能は未だ不明ですが、シナプスの可塑性や神経伝達物質放出の制御に関与する可能性が報告されています。1995年に家族性パーキンソン病の原因がα-シヌクレイン(αS)遺伝子の変異であることが発見され(PARK1)、α-シヌクレイン(αS)に関する多くの研究がおこなわれるようになりました。α-シヌクレイン(αS)はレビー小体の主成分であることからも、その神経細胞毒性が弧発性パーキンソン病の病態に中心的な役割を担っているのではないかと注目されています。
- ※3 アディポネクチン(APN):
- 脂肪組織より分泌される善玉のアディポサイトカインの一つであり、骨格筋や肝臓において受容体(AdipoR1およびAdipoR2などが知られている)を介しAMPキナーゼを活性化することで、脂肪燃焼や糖取り込みを促進し、インスリン抵抗性を改善する(Kadowaki et al, J Clin Invest. 2006)。AMPキナーゼを介したシグナル伝達は糖尿病や癌などを含む老齢性疾患との関連で大きな注目を浴びています。一方、神経変性疾患におけるアディポネクチン(APN)の役割はまだあまり明らかにされていません。
- ※4 シヌクレイノパチー:
- パーキンソン病(PD)は、レビー小体型認知症(DLB) や多系統萎縮症(MSA)とともに、α-シヌクレイン(αS)の蓄積・凝集やその凝集体であるレビー小体の形成(MSAではアストロサイトなどグリア系の細胞に封入体形成がおきることが知られています)を病理学的な特徴とすることから、シヌクレイノパチーと総称されます。同様に、タウ蛋白の蓄積を特徴とするアルツハイマー病(AD)をはじめ,進行性核上麻痺,大脳皮質基底核変性症,ピック病など一連の神経変性疾患を総称してタウオパチー、TDP-43が凝集、蓄積するALSや前頭側頭葉変性症を単一のスペクトラムとしてとらえて、TDP-43プロテイノパチーと分類することが知られています。


