
2014年11月5日
米国科学雑誌「Neuropsychopharmacology(ニューロサイコパーマコロジー)(米国神経精神薬理学会機関誌)」に 依存性薬物プロジェクトの池田和隆参事研究員らの研究成果が発表されました。
ドーパミンが無くても歩けることを発見
~パーキンソン病や統合失調症の新規治療に繋がる可能性~
ポイント
- 細胞外ドーパミン量と活動量は相関すると考えられていたが、今回の研究結果では、細胞外ドーパミン量が極端に減少するとむしろ活動量が上がることを発見した。
- 活動量の上昇(異常な多動)はクロザミンで抑制できること明らかにした。
- これらの発見は、脳の制御機構の解明に貢献するとともに、パーキンソン病や統合失調症の治療法の開発に大きなインパクトを与えるものと期待される。
公益財団法人東京都医学総合研究所の池田和隆参事研究員らは、遺伝子操作によりドーパミンを欠乏させたマウスにおいて、その行動や薬への反応性を調べ、ドーパミン欠乏マウスがほぼ正常に歩行でき、むしろ多動を示すことを発見しました。 さらに、この多動はクロザピンという抗精神病薬によって抑えられますが、ハロペリドールという抗精神病薬では抑えられないことがわかりました。 さらに詳しくメカニズムを調べた結果、アセチルコリンシステムがこのクロザピンの抑制効果と関わっていることを明らかにしました。 ドーパミンは、人格、運動、動機など、極めて重要な脳機能を担っていることが広く知られていますが、今回の研究により、ドーパミンと活動量の関係に関する従来の常識が覆されることになりました。 ドーパミン神経細胞が脱落して運動失調を示すパーキンソン病患者でも場合によって動けることや、クロザピンによってのみ改善効果が認められる統合失調症症状が知られていますが、ドーパミン欠乏マウスの行動は、このような従来説明のつかなかった現象と類似しています。
今回の研究成果は、ドーパミン機能の本質に関わる発見であり、パーキンソン病や統合失調症の新たな治療法に繋がる可能性が期待できます。 この研究成果は、米国科学雑誌「Neuropsychopharmacology(ニューロサイコパーマコロジー)(米国神経精神薬理学会機関誌)」の11月4日午前10時(米国東部時間)付オンライン版で発表されました。
1.研究の背景と経緯
ドーパミンは神経伝達物質の一つで、人格、運動、動機など、極めて重要な脳機能を担っています。カールソン博士はドーパミンに関する一連の研究により2000年のノーベル生理学・医学賞を受賞しました。パーキンソン病ではドーパミン神経細胞が脱落して運動失調を示し、ドーパミン前駆体のL-ドーパを摂取して脳内のドーパミンを補充することで治療されています。一方、統合失調症では多くの場合ドーパミン量が上昇することで幻覚や妄想が現れ、ドーパミン神経伝達を抑制するハロペリドールなどの抗精神病薬によって症状が消失します。つまり、ドーパミン量が少なければ活動量が少なくパーキンソン病となり、ドーパミン量が多過ぎると過活動となり統合失調症の症状が現れると考えられてきました(図1A)。ところが、普段ほとんど動くことができないパーキンソン病患者が火事など特殊な状況下では動けるという奇異性歩行(kinesia paradoxia)や、ハロペリドールなどの抗精神病薬では治らないけれどクロザピンという抗精神病薬では治る統合失調症症状があることも、一方で知られていて、そのメカニズムはわかっていませんでした。
このようなドーパミンが関係する脳機能を調べる上で、遺伝子操作によって作成されたドーパミン欠乏マウスは極めて有用だと考えられます。ドーパミン欠乏マウスは、ドーパミンやアドレナリンなどのカテコラミンの合成酵素の一つであるチロシン水酸化酵素の遺伝子を欠損させ、さらにアドレナリン神経細胞やノルアドレナリン神経細胞でチロシン水酸化酵素を発現するように遺伝子を組み換えたマウスで、アドレナリンやノルアドレナリンは有るけれどドーパミンが無いマウスです。このマウスは通常は生後2週齢ほどで死んでしまいますが、L-ドーパというドーパミンの前駆体を投与しておくと生体内でL-ドーパがドーパミンになり、生き続けることができます。
2.研究の概要
公益財団法人東京都医学総合研究所の依存性薬物プロジェクトおよびパーキンソン病プロジェクトの研究メンバーは、福島県立医大の小林和人教授、東京大学の柳原大准教授、ノースウェスタン大学のメルツアー教授らとともに、ドーパミン欠乏マウスの解析を行い、ドーパミンが無くても歩けることを発見しました。L-ドーパを投与して成獣に育てたマウスを用い、L-ドーパの投与を中止してから24時間後に脳での細胞外ドーパミン量をマイクロダイアリシス法※1によって計測したところ、ドーパミンが検出されることがわかりました。そこでL-ドーパ投与中止72時間後に測定したところ、ドーパミン量が検出限界以下となりました。また、L-ドーパ投与中止72時間後にマウスの活動量を調べたところ、ドーパミン欠乏マウスは最初はあまり動きませんが、徐々に動くようになり、数時間後には普通のマウスよりもよく動くことがわかりました。この時の歩行を詳しく分析したところ、パーキンソン病の症状に似た歩行パターンが若干現れていましたが、ほぼ正常な歩行でした。
ドーパミン欠乏マウスが示す多動に対して、ハロペリドールとクロザピンという抗精神病薬を投与したところ、ハロペリドールは全く効果が無く、クロザピンは多動を抑えました。ハロペリドールはドーパミン受容体を阻害する作用が主ですが、クロザピンには他にも様々な分子標的があることが知られています。そこで、選択的な薬剤を用いることでクロザピンがもつ複数の作用を1つ1つ個別に調べたところ、クロザピンが持つムスカリニックアセチルコリン受容体※2を作動させる作用が、ドーパミン欠乏マウスの多動を抑えることがわかりました。
ドーパミン欠乏マウスにおけるアセチルコリンシステムについて調べたところ、細胞外アセチルコリン量が低下していることとアセチルコリンの合成酵素の量が減少していることを見出しました。ドーパミンが欠乏するとアセチルコリンの量が低下して、異常な多動が現れた可能性が考えられます。
従来、細胞外ドーパミン量と活動量は相関すると考えられていましたが(図1A)、今回の結果から、細胞外ドーパミン量が極端に減少すると、むしろ活動量が上昇することがわかりました。さらに、この異常な多動は、クロザピンによって抑制できることが明らかとなりました(図1B)
参照図
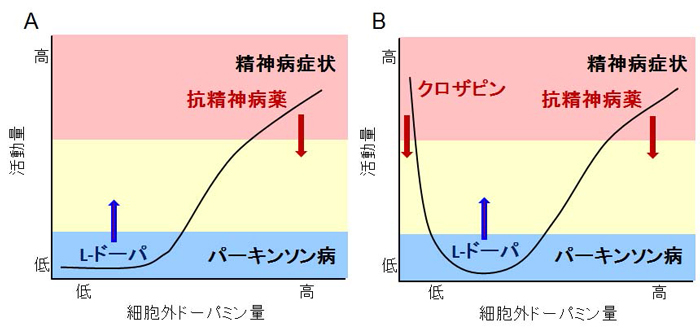
図1:細胞外ドーパミン量と活動量の関係に関する新旧モデル
(A)従来のモデル。細胞外ドーパミン量が増えると活動量が上がり、上がり過ぎると精神病症状が現れ、抗精神病薬によって細胞外ドーパミン量を下げれば症状が抑えられ、逆に、細胞外ドーパミン量が減ると活動量が下がり、下がり過ぎるとパーキンソン病となり、ドーパミン前駆体のL-ドーパを投与すると細胞外ドーパミン量が増えて症状が抑えられると考えられていました。(B)今回の研究結果から、細胞外ドーパミン量が極端に減少するとむしろ活動量が上昇し、この異常行動は抗精神病薬の一つであるクロザピンによって抑制されることが明らかになりました。
3.今後の展望
ドーパミンは一般の方々もよく耳にする広く知られた神経伝達物質であり、人格、運動、動機など人々の関心の高い脳機能と密接に関わっています。ドーパミン欠乏マウスを用いることで、ドーパミンの機能に関する従来の常識を覆す研究結果が得られたことは、脳の制御機構の解明に貢献するものだと考えられます。
パーキンソン病患者では、L-ドーパやドーパミン受容体作動薬など、ドーパミン神経伝達を亢進させる治療が行われていますが、今回、ドーパミンが無くてもほぼ正常に歩くことができることが明らかになったので、ドーパミン神経伝達を逆に抑えることで治療効果が出る可能性も考えられます。
統合失調症は罹患率が1%程度と高く、社会的損失が大きく社会的関心も高い疾患ですが、その病態メカニズムは十分にはわかっていません。統合失調症患者の中には、通常の抗精神病薬では効果が限定的でクロザピンによって劇的に症状が改善する例が知られています。また、ムスカリニックアセチルコリン神経伝達が統合失調症の症状と関連する可能性も近年指摘されてきています。今回、クロザピンおよびムスカリニックアセチルコリン作動薬で抑制されるドーパミン欠乏マウスの行動異常は、このような未解明の統合失調症の病態メカニズムの解明に繋がる可能性が期待できます。
【用語説明】
- ※1 マイクロダイアリシス法:
- 局所の微量物質の濃度変化を測定する方法。局所に半透膜のプローブを留置して、その中にかん流液を流し、かん流液中にしみ出した局所の微量物質の濃度を液体クロマトグラフィーにより分析する。
- ※2 ムスカリニックアセチルコリン受容体:
- 神経伝達物質の一つであるアセチルコリンの生体内の作用点の一つ。アセチルコリン受容体にはニコチンが作用するニコチニックアセチルコリン受容体と、ムスカリンという物質が作用するムスカリニックアセチルコリン受容体の2つのグループがある。ムスカリニックアセチルコリン受容体には、m1, m2, m3, m4, m5の5つのサブタイプが存在する。


