
2014年10月4日
米国科学雑誌「PLoS ONE(プロスワン)」に運動失調プロジェクトの筧慎治副参事研究員、石川享宏研究員らの研究成果が発表されました。
小脳から大脳への出力形成メカニズムを解明
~巧みな運動制御における小脳の役割の解明に向けて前進~
小脳※1は後頭部の奥深くにあり、大きさでは大脳に次いで2番目ですが、中に詰め込まれた神経細胞の数では大脳を大きく上回り、極めて高度な情報処理が行われていると考えられています。 機能的には大脳と連携して、身体を思い通りに動かすために必須の役割を果たしています。 小脳の障害に伴いさまざまな運動失調※2が現れることは100年以上前から知られていましたが、複雑な小脳の神経回路がその機能を実現する仕組みは未解明のままでした。 特に小脳での情報処理の結果を、大脳に送り返すための出力形成メカニズムが大きな謎であり、数十年来の論争が続いていました。
公益財団法人 東京都医学総合研究所・運動失調プロジェクト・プロジェクトリーダーの筧慎治副参事研究員と石川享宏研究員らは、同研究所の角田吉昭研究員、李鍾昊研究員、国立精神・神経医療研究センターの戸松彩花研究員、米国・ピッツバーグ大学(Pittsburgh University)のDonna Hoffman博士との共同研究により、運動遂行時の小脳皮質から小脳核※3への情報の流れを追跡し、小脳の出力形成メカニズムを明らかにしました。 本研究成果により、人間の巧妙な運動制御や、小脳疾患において運動障害が生じる仕組みの理解が更に深まることが期待されます。
この研究成果は、米国科学学会誌「PLOS ONE」10月3日午前0時(米国東部時間)付オンライン版に掲載されました。
1.研究の背景
我々人間の小脳の大部分は、大脳皮質と連関して(図1.大脳小脳連関)運動制御や高次脳機能の円滑な遂行に重要な役割を果たしています。 例えば目の前のコップを掴もうとする時、腕を動かすために必要な運動指令が最初に大脳運動野※4で作られ、脊髄に送られると同時に、運動指令のコピーが小脳へと送られます。 現在最も有力な小脳機能の仮説によれば、小脳はその運動指令に基づいて次の瞬間の身体の状態を実際に身体が動くよりも前に予想し、小脳核を通してその予想結果を大脳へと送り返します。 大脳はその予測情報を元に、更に次の瞬間の運動指令を生成します。 手がコップを掴むまで、大脳と小脳がこの様な情報のやり取りを繰り返すことにより、スムーズな運動が実現できるというわけです。 この大脳と小脳の役割分担は、餅つきの時の杵を持った「つき手」と、お餅をひっくり返す「返し手」の関係と似ています。 しかし、この様な機能を実現している小脳の神経活動とその原理について、具体的なことは全く分かっていませんでした。
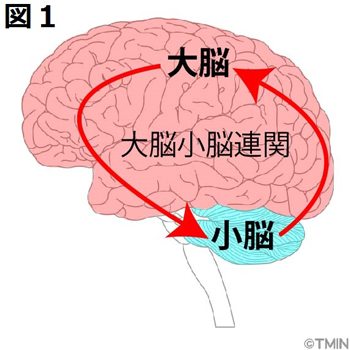
小脳と大脳は、赤の矢印のように双方向性に情報をやり取りしながら、連携して機能を果たしている。これを大脳小脳連関とよぶ。
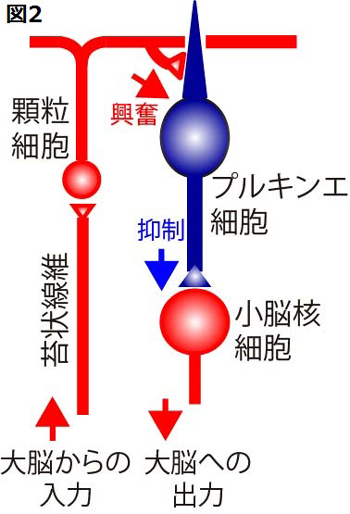
図2に示すように、大脳からの入力は苔状線維によって、最初に小脳皮質の顆粒細胞に入力されます。 次いで顆粒細胞から、プルキンエ細胞※5へと信号が伝わり、最後に小脳核の神経細胞で信号が統合されて大脳へ送り返されます。ここで注目すべきは、プルキンエ細胞が抑制性※6の細胞で、小脳核細胞の興奮性を抑えるところです。このシナリオでは、運動を行うときに大脳からの入力が増加すると、プルキンエ細胞が興奮し、小脳核への抑制が強まります。従ってプルキンエ細胞の標的である小脳核細胞にはブレーキがかかり、活動が減るはずです。ところが予想に反して、小脳核細胞は運動時に活動を大幅に増加させることが分かっていました。 小脳核細胞はプルキンエ細胞からの抑制で興奮していることになります。ブレーキで加速する車?これは謎です。
そこで筧慎治プロジェクトリーダーと石川享宏研究員らのグループは、小脳核の興奮の謎の解明を目指して、運動をしているニホンザルでプルキンエ細胞と小脳核細胞の活動の関係を調べました。
2.研究成果の要点
運動中のプルキンエ細胞と小脳核細胞の活動を調べるため、図3に示すようなテレビゲーム形式の行動課題を行うようにニホンザルを訓練しました。 サルは手首の角度を測る装置をマウス代わりに操作して、手首の動きと連動するモニター上のカーソルを目標の円内に動かします。 このような行動課題の最中にプルキンエ細胞と小脳核細胞の活動を記録すると、図4左に示すようにプルキンエ細胞は手首運動の直前に活動が減少し、逆に小脳核細胞の活動が増加しました。
図3.
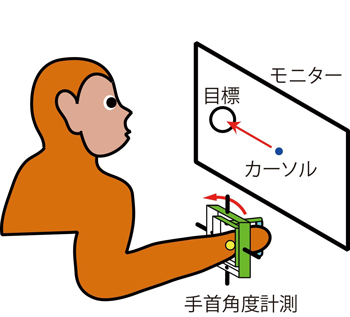
緑色の器械がサルの手首の角度を計測し、コンピューターマウスと同じ機能を果たす。その結果、手首の動きに連動してモニター上のカーソルが動く。
この結果は、プルキンエ細胞から小脳核細胞への抑制(ブレーキ)が減少した結果、「脱抑制」と呼ばれる仕組み(図4右)により小脳核細胞が興奮したことを示しています。プルキンエ細胞②は常に高い活動レベルを示し、小脳核細胞③に持続的に強いブレーキを掛けています。ここでプルキンエ細胞②の活動が減少すると、ブレーキが弱まり、抑制から解放された反動で小脳核細胞③が興奮すると解釈できます。
ではプルキンエ細胞を抑制している陰の主役は何でしょう?実は、小脳皮質には非常に多くの抑制性介在細胞(図4右①)が存在することが昔から知られていましたが、それらが何の役に立つのか誰にも説明出来ませんでした。そのため図2では介在細胞が省略されていました。今回の研究で、従来の小脳理論では脇役であった抑制性介在細胞が情報処理の主役として小脳研究の表舞台に初めて姿を現しました。
図4.
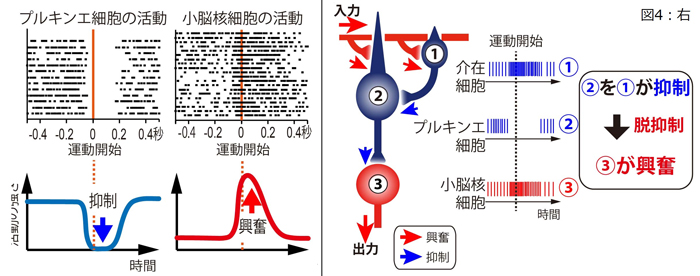
左:プルキンエ細胞、小脳核細胞ともに、横軸は時間軸を表す。
図の上半の水平な黒点の並びは、運動の1試行毎の細胞の活動である活動電位(黒点)のタイミングを示す。黒点の密度が高いところは細胞が興奮していることを、密度が低いところは細胞が抑制されていることを示す。図の下半は上のデータに基づく活動電位の発火頻度の増減を模式的に示すグラフ。グラフの上向きの振れは興奮を、下向きの振れは抑制を示す。運動開始の前後では、プルキンエ細胞の活動は急激に減少し、対照的に小脳核細胞の活動は急激に増加している。
右:本研究で明らかになったプルキンエ細胞と小脳核細胞の活動の関係を模式化したもの。
プルキンエ細胞を抑制する介在細胞は図2では省略されていた。介在細胞の活動は、プルキンエ細胞の活動から推定した。プルキンエ細胞への直接の興奮作用の効果は、介在細胞の抑制によりマスクされているため観察されない。
3.発見の意義
<基礎研究としての意義>
従来の小脳理論は、小脳から大脳への出力形成に関して、プルキンエ細胞の興奮をプラスの情報、抑制をマイナスの情報と仮定して、全ての実験データを解釈してきました。また、あくまでも興奮が主であり抑制は脇役でした。本研究は、その符号と主客を逆転させ、そのような前提が誤りであることを示しました。今後、この新しい前提に基づく小脳理論の再構築が必要になりました。
<応用研究としての意義>
小脳から大脳への出力形成メカニズムの謎が解かれた結果、小脳の神経細胞や、その活動の基盤となる各種の遺伝子やタンパク質の機能的な役割を、正しく位置づけられるようになりました。今回の成果を起点として小脳の働きの詳細な理解が進むことにより、将来的に脊髄小脳変性症等の難病に対して根治的な治療を行う際の標的部位の選択にも貢献できると期待されます。
【用語説明および補足】
- ※1 小脳:
- その名前はラテン語で「小さな脳」を意味するcerebellumに由来し、大脳の後下方に位置しています。重量では脳全体の10%にすぎませんが、数では1000億の神経細胞から成り(大脳は約140億!)、神経系全体の過半数を占めています。18世紀に小脳の損傷が運動障害の原因となることが発見され、以来多くの研究によって小脳は全身のさまざまな運動をスムーズかつ正確に行うために必須の脳領域であることが明らかになってきました。小脳の主要な役割は運動の調節ですが、近年では認知や感情などの高次脳機能にも重要な貢献をしていることが示されています。
- ※2 運動失調:
- 小脳疾患に伴って現れる特徴的な運動障害を特に小脳性運動失調と呼ぶ。筋力の低下や感覚異常は認められず、筋の協調的な収縮パターンの乱れが原因と考えられています。指鼻試験、膝踵試験などにおける運動の分解や測定異常、反復拮抗運動不能、筋緊張の低下、時間測定異常などが見られます。
- ※3 小脳核:
- 小脳内部で処理された情報を他の脳領域に出力する部位であり、左右の脳に歯状核、中位核、室頂核と呼ばれる3対の神経核があります。大脳に情報を送り出すのは主に歯状核であり、ヒトの場合は歯状核のみが極端に発達しています。このことは、大脳がその機能を果たす上で小脳の助けを借りることが必須であり、ヒトの大脳と小脳の発達が並行してきたことを示唆しています。
- ※4 大脳運動野:
- 大脳は部位によって異なる役割を持っており(機能局在)、運動の制御に特化した脳領域を大脳運動野と呼びます。その中でも一次運動野と呼ばれる領域には、頭から足先まで全身のあらゆる部位の運動に対応する神経細胞が地図のように並んでおり、これをホムンクルス(ラテン語で“脳の中の小人”の意)と呼んでいます。ヒトではこのホムンクルスの顔、口、手に対応する部位が極端に大きな面積を占めていることから、これらの部位の細かな運動制御が、ヒトにとって極めて重要な意味を持っていることが想像できます。
- ※5 プルキンエ細胞:
- 小脳皮質にある抑制性の神経細胞。発見者であるチェコの解剖学者ヤン・エヴァンゲリスタ・プルキニェにちなんで名づけられました。ヒトの脳で最も大きな神経細胞の一つであり、非常に大きな樹状突起を持っています。一つの細胞あたり約20万もの平行線維入力を受け、それらの信号を統合した結果を小脳核の細胞に伝達します。
- ※6 抑制性:
- 神経細胞の性質で、他の神経細胞の興奮性を低下させる性質を指しています。神経細胞が抑制性の伝達物質を放出し、その物質が相手の神経細胞に薬理学的な作用を及ぼすことにより、興奮性を低下させます。


