
Jul. 2022 No.046
特集
Topics
開催報告
編集後記
Topics
筋萎縮性側索硬化症及び前頭側頭型認知症患者の脳内で凝集したTDP-43タンパク質の研究における構造上のブレークスルー
認知症プロジェクトリーダー長谷川 成人
筋萎縮性側索硬化症(ALS)は、成人になってから発症する運動ニューロン疾患の中で最も多い疾患であり、前頭側頭型認知症(FTD)は、アルツハイマー病に次いで多い老年性認知症です。ALS と多くのFTD は、中枢神経系におけるTDP-43 の蓄積病変が特徴であり、神経変性の原因と考えられています。現在、これらの疾患の早期診断は不可能であり、疾患を改善する治療法もありません。これは、病的なTDP-43 凝集体の構造が不明であることが一因です。今回、我々は愛知医科大学とMRC 分子生物学研究所との共同研究により、ALS 及びFTD 患者脳におけるTDP-43 線維の異常構造を明らかすることに成功しました。
TDP-43 は本来、核に局在するヘテロ核リボヌクレオタンパク質の一種で、正常では遺伝子の転写やその後のpremRNAの転写後修飾に関与するタンパク質です。ところが、ALS やFTD の患者では線維化して細胞質や突起内に蓄積し、正常な機能を果たせなくなると同時に細胞に障害を及ぼします。今回、愛知医科大学に保管されていた2 例のALS 及びFTD 剖検脳の前頭葉、並びに運動皮質から、界面活性剤に溶けないという性質を利用して凝集したTDP-43 を含む試料を調製しました。MRC 分子生物学研究所に送り、低温電子顕微鏡解析(クライオ電顕)を行いましたところ、ヘリカル再構成法を用いて2.6 オングストロームの分解能でその構造が明らかとなりました。線維化したTDP-43 は分子が積み重なってできたアミロイド様の捻れた線維構造をとっていました。興味深いことに、その線維中心はらせん軸に垂直な方向に、これまで知られていなかったダブルスパイラル状の折り畳み構造をとっていました。調べた全ての脳領域及び個人で同じ構造でしたが、実験モデルでこれまでに形成されたTDP-43 線維とは類似性を示しませんでした。TDP-43 の線維中心は、複雑なアミノ酸組成を持たない領域によって形成されており、神経変性疾患に関わるタウやαシヌクレインなどのタンパク質線維と比較して、構造的にも化学的にもユニークな線維表面をもつことがわかりました。これらの結果は、TDP-43 凝集を伴うALS やFTD の分子病態メカニズムの解明だけでなく、診断プローブ、治療法の開発の役立つことが期待されます。
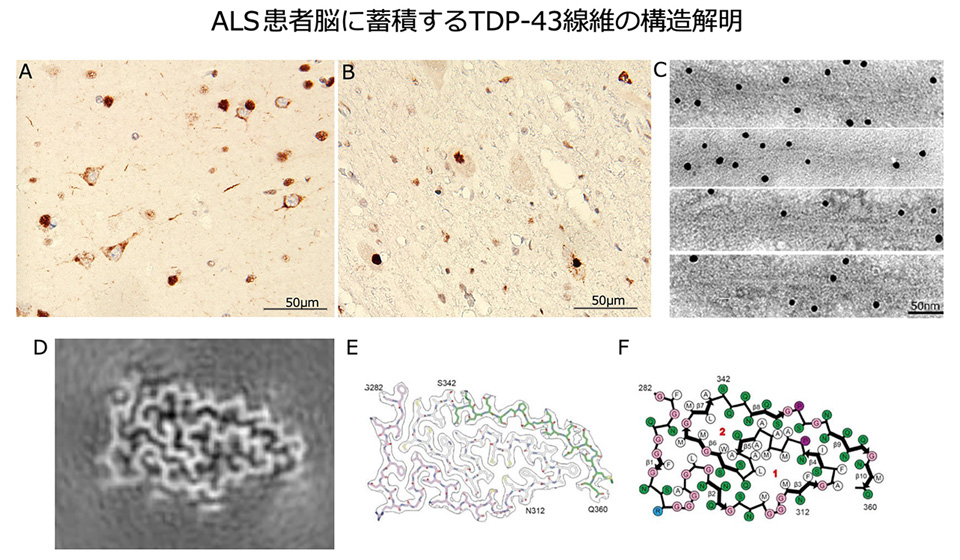
B. ALS患者脳に蓄積するリン酸化TDP-43の免疫組織染色(脊髄),
C. 患者剖検脳から単離したTDP-43線維の電顕像(10nm金コロイド結合TDP抗体でラベル),
D. クライオ電顕解析によるTDP-43線維の立体再構成像,
E. クライオ電顕デンシティマップ,
F. TDP-43線維の折り畳み構造の原子モデル

