
2015年7月13日
米国科学アカデミー紀要「Proceedings of the National Academy of Sciences of the United State of America」に神経病理解析室の新井信隆副所長、増井憲太研究員(現・東京女子医科大学第一病理、協力研究員)、シナプス可塑性プロジェクトの山形要人副参事研究員らの研究成果が発表されました。
癌は栄養素を利用して治療に抵抗する
~ 悪性脳腫瘍の新しい病態機構を解明、新たな治療戦略開発に期待 ~
私たちは、悪性の脳腫瘍である膠芽腫(グリオブラストーマ)※1という難病が薬剤治療に抵抗する新規の病態メカニズムを解明しました。この腫瘍では、細胞の代謝活動に必要な栄養素が細胞増殖に影響を与えており、腫瘍は栄養素の代謝産物を利用して治療に抵抗性を発揮することが明らかとなりました。このメカニズムは、従来行われている手術、化学療法や放射線療法とは異なる標的となる可能性があり、現在治療選択肢が少ない悪性脳腫瘍に対する新しい予防・治療戦略に繋がることが期待されます。
1.研究の背景
癌細胞は正常の細胞と異なり、物質の代謝経路を自身に都合の良いように活性化して、過酷な環境下でも生き延びることが知られています(癌代謝)※2。癌の研究者達は、腫瘍が特徴的な代謝を持っていることを以前より認識しており、この異常に亢進した代謝活動をPETスキャンなどの診断ツールとして利用しています。近年、科学者たちはこの異常な代謝活動が癌の病態に与える影響を解析し始めています。つまり、これまで多くの癌において代謝が活性化されることは知られていたのですが、それが癌の成長に対してどのように有利に働いているのかは不明な点が多い状況でした。私たちは以前、細胞の代謝を調節する中心的な存在であるmTOR複合体2(mTORC2)※3が癌代謝を活性化することを報告しました。 そこで今回、mTORによる代謝の亢進が悪性脳腫瘍(グリオブラストーマ)の生存に対してどのように有利に働いているのかを解析することにしました(図1)。
図1:癌代謝が悪性脳腫瘍の病態に与える影響
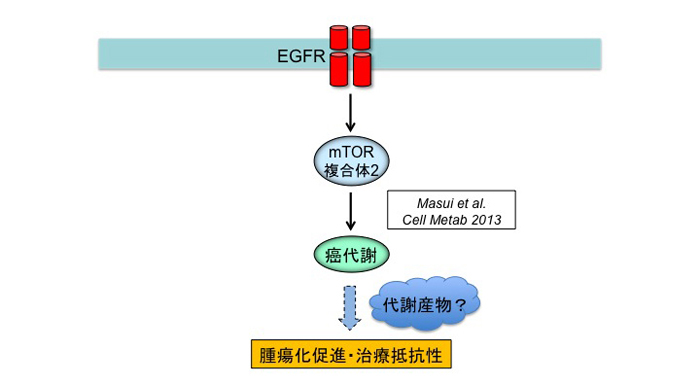
以前私たちはmTOR複合体2(mTORC2)が癌代謝を活性化することを報告した(Cell Metab 2013)。この癌代謝活性化が悪性脳腫瘍にとってどのように有利に働くのかを今回検討した。
2.研究の概要
最初の結果は膠芽腫細胞を培養して調べる実験系から生まれました。私たちは、細胞の代謝活動に必須である代謝基質(グルコースまたは酢酸)を細胞に加えると、これらの栄養素が細胞増殖に必要なmTORC2を活性化することを見出しました。さらにmTORC2の活性化に重要な要素は、グルコースおよび酢酸から代謝活動により産生されるアセチルCoAであることを掘り下げました。つまり、癌細胞において代謝が活性化する結果、産生された代謝産物がmTORC2を活性化し、細胞増殖に有利に働くことを示す結果です。これは相互的な関係であり、mTORC2は癌代謝を活性化しますが、活性化した癌代謝は逆にmTORC2を活性化するわけです(図2)。
多くの腫瘍はEGFR(上皮成長因子受容体)※4という分子により増殖を駆動されており、EGFRに対する阻害剤が重要な治療選択肢の一つとなっています。しかしながら、膠芽腫においてはEGFR阻害剤の効果が低いことが以前より問題でした。興味深いことに、グルコース及び酢酸の非存在下では、EGFR阻害剤はmTORC2のシグナル伝達をオフに切り替えることができますが、グルコースと酢酸を添加した場合には、EGFR阻害剤は作動しませんでした。つまり、グルコースまたは酢酸はアセチルCoAの産生を通じてmTORC2を活性化し、腫瘍がEGFR阻害剤などの分子標的治療※5に抵抗することを可能としたわけです(図2)。同様のメカニズムは、膠芽腫患者さんから直接採取された細胞およびマウスに移植したヒト膠芽腫動物モデルでも観察されました。
図2:癌代謝の活性化が治療抵抗性へつながる
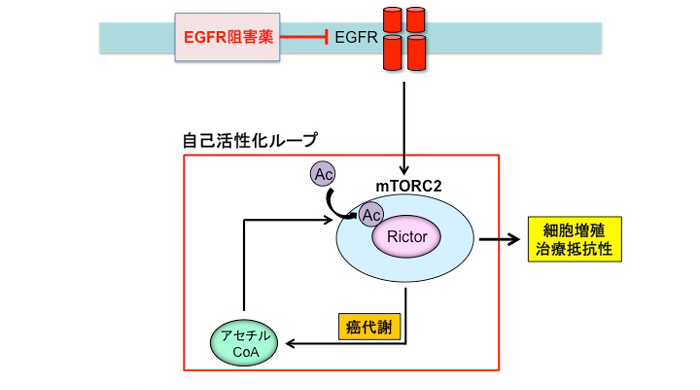
mTORC2は癌代謝を活性化するが、活性化した癌代謝は逆にアセチルCoAによるRictorのアセチル化を介してmTORC2を活性化する。これによりmTORC2の自己活性化ループが形成され、EGFR阻害剤への抵抗性が発揮される。
今後の展望
栄養素や代謝活動が癌に有利に働く事を示すこの研究結果は、癌に関与する遺伝子・細胞内シグナルと環境要因との間に複数の相互作用が存在する可能性があることを示しています。将来の検討により、食生活を含むライフスタイルが癌におよぼす影響の解明や、癌患者さんのためのより効果的な予防および治療戦略の開発が可能となるかもしれません。また、mTORC2や癌代謝を標的とする治療法を開発することが、膠芽腫の新たな治療戦略となりうる可能性を示唆しています。
用語解説
- ※ 1 膠芽腫(グリオブラストーマ):
- 脳腫瘍の一種で、ヒトの腫瘍の中でも最も悪性度が高い腫瘍の一つ。診断後の平均生存期間は1年前後の難病で、新たな病態解明および治療開発が望まれている。
- ※ 2 癌代謝:
- 癌細胞は正常の細胞と異なり、物質の代謝経路を自身に都合の良いように再構成する。急速に増殖するために必要な材料およびエネルギーが癌細胞に供給され、癌細胞の生存に有利に働くと考えられている。
- ※ 3 mTOR複合体:
- mTOR複合体は細胞の代謝を調節する中心的な存在であり、mTOR複合体1(mTORC1)とmTOR複合体2(mTORC2)に分類される。
- ※ 4 EGFR(上皮成長因子受容体):
- 上皮細胞の成長に必要な受容体であり、膠芽腫を含む多くの癌で活性化していることが知られている。したがって、その阻害が癌治療の選択肢の一つとして注目されている。
- ※ 5 分子標的治療:
- 癌細胞にのみ発現する分子を標的とする分子標的治療薬を使用する癌の治療。従来の抗癌剤よりも副作用が少なく効果が高いとされる。

