
2015年11月7日
国際科学雑誌「Acta Neuropathologica」オンライン版に長谷川成人参事研究員らの論文が発表されました。
タウの異常構造の違いによる認知症の生化学分類
研究の背景
認知症をひき起こす原因タンパク質として微小管結合タンパク質の一種の「タウ※1」があり、タウの異常病変を伴う疾患群はタウオパチーと総称されます。最も患者数が多いアルツハイマー病をはじめ、働き盛りを襲う若年性認知症認知症のピック病※2、手が思うように使えない等の運動障害があらわれる皮質基底核変性症※3や進行性核上性麻痺※4など、様々な認知症疾患が含まれます。重要なことにタウの異常病変の分布や広がりが臨床症状と密接な関係があり、異常になったタウが直接、間接的に神経細胞の変性、脱落を誘導することが示唆されています。タウは神経細胞内で他のタンパク質と一緒に存在し、主に軸索などに局在していますが、認知症の患者さんの脳ではタウが自己重合して異常な線維構造を形成し、リン酸化やユビキチン化を受けて神経細胞内やグリア細胞内に蓄積してきます。不思議なことに、アルツハイマー病では脳に発現する6種類すべてのタウが蓄積しますが、ピック病では3リピートタウが、皮質基底核変性症や進行性核状性麻痺では4リピートタウが蓄積します。このようにタウの病変は、疾患、病型ごとに特徴的な形態、病理を呈しますが、なぜ様々なタウの病変が出現するのか、その違いは何に起因するのかなどは明らかではありませんでした。そこで様々な疾患の患者剖検脳に蓄積する異常型タウの詳細な解析を行いました。
この成果は、国際科学雑誌「Acta Neuropathologica」オンライン版に11月7日掲載されました(http://link.springer.com/article/10.1007/s00401-015-1503-3より free download可)。
研究の概要
アルツハイマー病(AD)、ピック病(PiD)、皮質基底核変性症(PSP)、進行性核上性麻痺(CBD)、タウ遺伝子(イントロン10)の異常による前頭側頭葉変性症(MAPT)※5の患者剖検脳からサルコシルという界面活性剤に不溶性を示すタウ(異常型タウ)を分離し、様々なタウの部位に対する抗体を用いた生化学解析、及び免疫電顕による超微細形態の観察により調べました。また、異常型タウにプロテアーゼの一種であるトリプシンを作用させ、トリプシンでも分解を受けないトリプシン耐性領域について、質量分析やアミノ酸配列解析などのタンパク化学解析による詳細な解析を行いました。
その結果、ADでは6種類すべてのタウが(3リピートタウト4リピートタウが1:1の比率で)蓄積していること、PiDでは3リピートタウが、CBD、PSP、MAPTでは4リピートタウが蓄積していること、さらには、タウのC末端断片やトリプシン耐性領域のバンドパターンが疾患によって異なることが明らかとなりました。また、トリプシン耐性領域をさらに詳細に調べると、疾患ごとに自己重合に関わっている微小管結合領域が少しづつ異なること、その違いは重合したタウ線維の特徴的な形態と強く関係していることが示されました。この結果は、多様な病態を形成するタウオパチーが、異常型タウの構造の違いによって生化学的に分類可能であることを示します。
本研究結果は、タウオパチーの多様性と規則性が、最初に形成される異常型タウの種類、構造の違いや、どの細胞に出現するかによって、多様でかつ規則正しいタウ病理が形成されること、そしてその異常構造が別の細胞に伝播することによって、同じ異常構造を有するタウ病変が他の細胞にも広がって病気が進行する可能性があることを示します。疾患ごとに異なるタウの異常構造が形成される模式図を参考図3に示します。
参考図
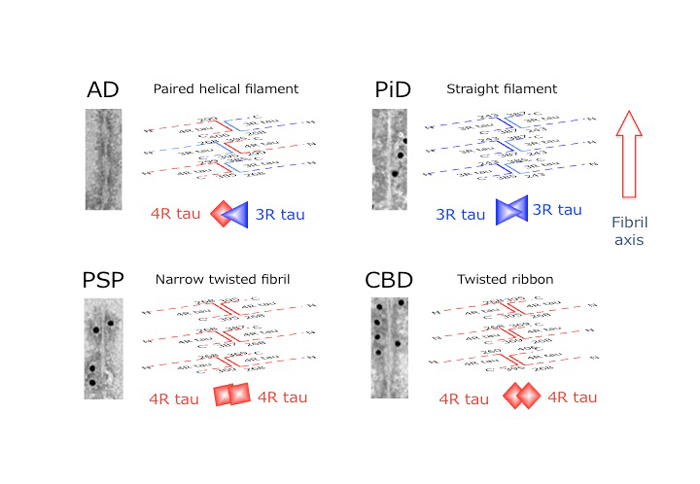
タウオパチー(AD, PiD, PSP, CBD)におけるタウ線維とその異常型タウ(重合体)の模式図
青色が3リピートタウ、赤色が4リピートタウを示す。タウ同士が逆平行(アンチパラレル)に重合し、積み重なって線維化する様子を模式的に示した。それぞれの疾患脳に認められるタウ線維の電子顕微鏡写真を左側に、その模式図を右側に示す。赤色四角と青色三角で示した模式図は、それぞれの疾患で最初に形成されると考えられる異常型タウ(二量体)のシード(種)を示す。
今後の展望
今回、トリプシン耐性バンドパターンの違いにより、AD, PiD, CBD, PSP, MAPTの生化学分類が可能となりましたが、他の病型(嗜銀顆粒性認知症、顆粒性グリア細胞タウオパチーなど)のタウオパチーの分類にも応用できると考えられます。また、疾患ごとに異常型タウの重合領域の詳細な構造が示されましたので、それらを区別する化合物や抗体のデザイン、診断薬や疾患特異的なPETプローブの開発、さらには治療薬や治療法の開発に役立つ可能性が考えられます。
【用語説明】
- ※1 タウ:
- タウは神経細胞に多く発現し、細胞の形態や物質輸送に重要な微小管の重合や安定化にはたらくタンパク質で、ヒトの大人の脳では6種類の分子種(アイソフォーム)が発現する。微小管との結合に関わる繰り返し配列が3つの3リピートタウと4つの4リピートタウに大別され、その比率はほぼ1:1。
- ※2 ピック病:
- 若年性認知症の中核的な疾患で、主に前頭葉の神経細胞が変性することにより、性格変化や自己抑制がきかなくなるような症状を特徴とする認知症。変性する神経細胞にピック球とよばれる特徴的なタウの異常構造物が出現する。
- ※3 皮質基底核変性症:
- 手が思うように使えないなどの大脳基底核の異常に伴う症状や、筋肉の硬さ、動作緩慢、歩行障害などのパーキンソニズムが同時にみられる病気。典型的な症状がないために、診断が難しい。神経病理学的には、死後脳病理解析でastrocytic plaqueというタウ陽性の特徴病変がある場合にこの病気と診断される。
- ※4 進行性核上性麻痺:
- 後ろ向きに転倒し易い、上を見ることができないなどの症状やパーキンソニズム、認知症を伴う病気。神経病理学的には、死後脳病理解析でtuft-shaped astrocytes と呼ばれるタウ陽性異常構造が見られる場合にこの病気と診断される。
- ※5 タウ遺伝子の異常による前頭側頭葉変性症:
- タウ遺伝子(MAPT)の異常により、異常タウが神経細胞やグリア細胞内に蓄積し、変性する疾患の総称。これまでに30カ所以上の変異が報告されており、変異の部位や種類によって様々な臨床病理学的表現形が報告されている。今回解析した症例はイントロン10変異で、変異により4リピートタウの割合が増加すること、患者脳では4リピートタウが神経細胞、グリア細胞に蓄積していることが知られている。


