
Apr. 2021 No.041
特集
Topics
開催報告
編集後記
Topics
構造の異なるαシヌクレイン線維はプロテアソーム阻害の違いにより異なる病理を誘導する
認知症プロジェクトの鈴木元治郎主席研究員、長谷川成人参事研究員らは「構造の異なるαシヌクレイン線維はプロテアソーム阻害の違いにより異なる病理を誘導する」について米国科学雑誌eLifeに発表しました。
認知症プロジェクト 主席研究員鈴木 元治郎
アルツハイマー病をはじめとする神経変性疾患では多くの場合その病気に特徴的なタンパク質の凝集体の蓄積が患者脳で観察されます。パーキンソン病、レビー小体型認知症などではαシヌクレイン(α Syn)というタンパク質の凝集体の蓄積が観察され、これらの疾患はαシヌクレイノパチーと総称されます。凝集体が蓄積する部位と神経変性が起きる部位が相関することから、α Syn凝集体自身がαシヌクレイノパチーの病因であると考えられます。しかし、α Syn凝集体にどのような毒性があるのか?α Syn凝集体により異なる疾患が引き起こされるのはなぜか?などはわかっていませんでした。
まず、大腸菌を用いて精製した可溶性のα Synタンパク質を生理的条件の塩(KCl:塩化カリウム)の存在下(KCl+)と非存在下(KCl-)で凝集体を形成し、得られた凝集体は異なる構造を持つことを確認しました。これらの凝集体を野生型マウスの脳内に注入したところ、KCl-で形成したα Syn凝集体を注入したマウスではα Syn 凝集体が蓄積しましたが、KCl+で形成したα Syn凝集体を注入したマウスではα Syn凝集体はほとんど蓄積しませんでした(図右)。これらの凝集体をマウス初代培養神経細胞に導入した場合も同様で、KCl-で形成したα Syn凝集体を導入した神経細胞でのみα Syn凝集体の蓄積が顕著に認められました。どのような機序でKCl-で形成したα Syn凝集体のみがα Syn凝集体の蓄積を誘導したかを調べたところ、KCl-で形成したα Syn凝集体は、C末端領域が露出した構造をもっており、プロテアソームと呼ばれるタンパク質複合体と相互作用し、その活性を阻害することが明らかになりました(図左)。
今回の結果から、α Syn凝集体の毒性はその構造により異なり、プロテアソームと結合し活性を阻害するという毒性を有するものが存在することが明らかになりました。また、α Synの構造の違いにより引き起こされる病理が異なることの原因が明らかとなり、今後αシヌクレイノパチーの発症メカニズムの解明につながることが期待されます。
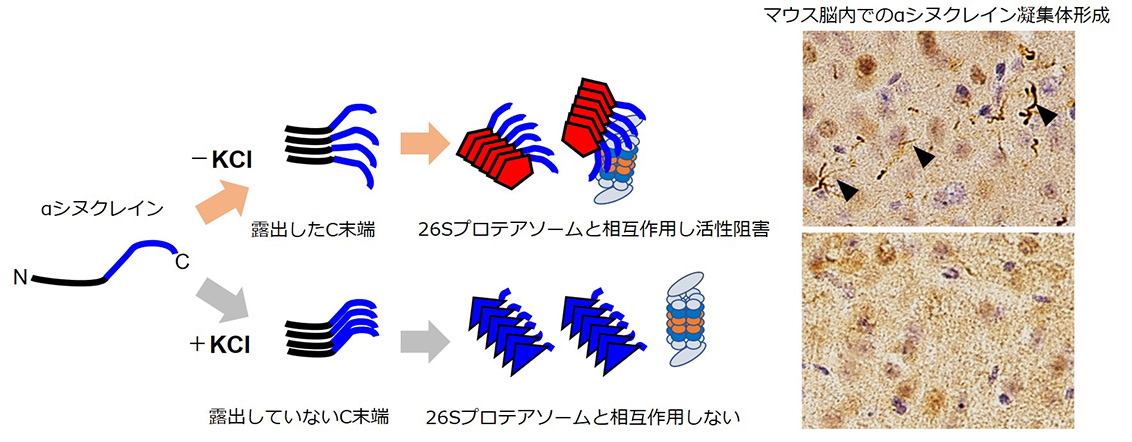
図
αシヌクレインはC末端領域に負に荷電した領域(青)がある。塩(KCl)の非存在下で凝集体を形成するとC末端領域の静電的反発により、C末端領域が露出した構造の凝集体が形成される。この凝集体の露出したC末端領域がプロテアソームと相互作用し、その活性を阻害すると考えられる(左上)。このような構造の凝集体をマウスや細胞に導入するとリン酸化αシヌクレインの蓄積が誘導される(右上)。一方、塩の存在下で凝集体を形成すると、静電的反発が抑えられ、C末端領域が埋没した構造の凝集体が形成される。この凝集体はプロテアソームと相互作用をせず、その活性も阻害しないと考えられ(左下)、αシヌクレインの蓄積をほとんど誘導しない(右下)。

