
2016年6月27日
「Nature Communications」に田中所長らが「肝細胞がんを抑制する新規化合物を同定」について発表
肝細臓がんを抑制する新規化合物を同定
新潟大学大学院医歯学総合研究科分子遺伝学の小松雅明教授、東京都医学総合研究所の田中啓二所長らは、肝細胞がんが増殖する仕組みを解明し、その仕組みを打ち消す新規化合物を突き止め肝細胞がんの悪性化を抑制することに成功しました。研究成果は、新潟大学大学院医歯学総合研究科消化器外科学の若井俊文教授、東京大学創薬機構の岡部隆義教授、慶應義塾大学先端生命科学研究所の曽我朋義教授らとの共同研究で得られたもので、2016年6月27日(英国時間)に英国科学誌『Nature Communications(ネーチャーコミュニケーションズ)』(IMPACT FACTOR 11.470)にオンライン掲載されました。
http://www.nature.com/ncomms/2016/160627/ncomms12030/full/ncomms12030.html
- <論文タイトル>
-
p62/Sqstm1 promotes malignancy of HCV-positive hepatocellular carcinoma through Nrf2-dependent metabolic reprogramming.
p62/Sqstm1はNrf2依存的代謝再編成により肝細胞がんの悪性化をもたらす。
1.研究の背景と経緯
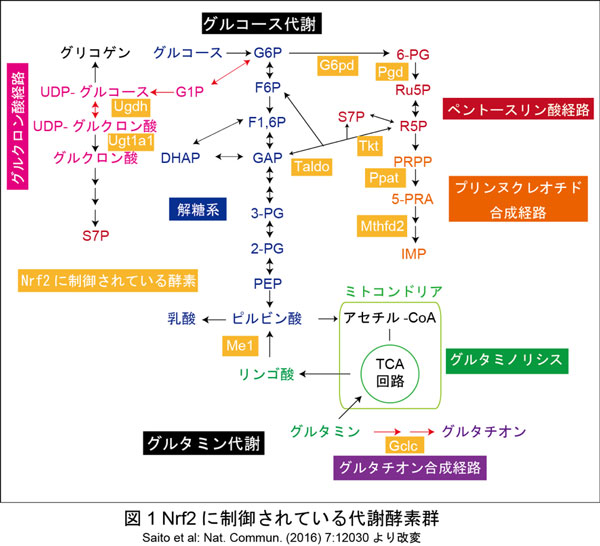
肝細胞がん患者のがん細胞において、マロリー小体と呼ばれる構造体が大量に存在することが知られています。我々はこれまでにこの構造体の主成分であるp62/SQSTM1による酸化ストレス応答機構Keap1−Nrf2経路の制御機構を明らかにしてきました。この経路では、p62の349番目のセリン残基がリン酸化されると転写因子Nrf2の抑制タンパク質であるKeap1が不活化し、Nrf2の標的遺伝子である抗酸化タンパク質、解毒酵素群の遺伝子発現が誘導されます。このp62−Keap1−Nrf2経路は、正常細胞では選択的オートファジー起動時に一過的に活性化するのに対し、肝細胞がんでは恒常的に活性化しており、それが腫瘍の増殖に寄与します。しかし、如何にして腫瘍増殖に寄与するのかは不明のままでした。2012年に、PI3K-Akt経路が活性化されている肺がん細胞において、恒常的なNrf2の活性化がグルコースおよびグルタミン代謝に関わる律速酵素の遺伝子発現を正に制御し、プリンヌクレオチドやグルタチオンの合成経路、そしてグルタミノリシスを亢進させることが明らかになりました(図1)。そこで我々はp62−Keap1−Nrf2活性化時にも上記のような代謝リプログラミングが起こっており、それが腫瘍増殖に寄与している可能性を考え、その仮定を検討しました。
図1
2.研究の成果
今回、ヒト肝細胞がん株、リン酸化p62を蓄積し肝腫瘍を形成する肝臓特異的Atg7欠損マウス、そして肝細胞がん患者検体を用いた解析により以下のことを明らかにしました。
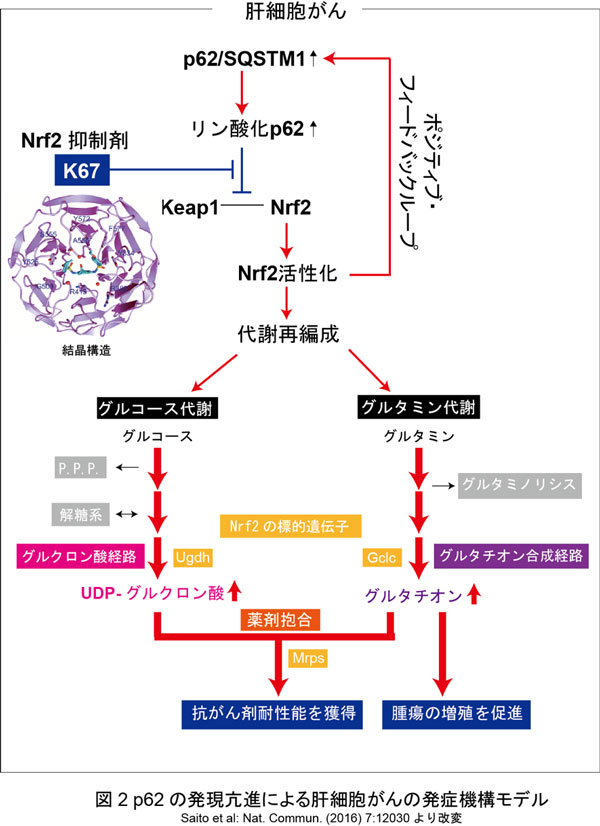
1. 肝細胞がん細胞におけるリン酸化p62を介したNrf2の活性化は、グルコースからUDP-グルクロン酸の合成、およびグルタミンからグルタチオン合成を促進させた(図2)。
2. 薬剤抱合に関与するUDP-グルクロン酸およびグルタチオンの産生亢進により、リン酸化p62を持つ肝細胞がん細胞は抗がん剤耐性能を獲得した。グルタチオンの産生亢進は、腫瘍の増殖を促進させた(図2)。
3. 肝臓特異的Atg7欠損マウス肝臓において、腫瘍形成以前にプリンヌクレオチド合成やグルタチオン合成促進などの代謝変化が確認され、それはNrf2の同時欠損により完全に戻った。
4. C型肝炎ウイルス陽性のHCC患者において、顕著なリン酸化p62の蓄積が認められた。
5. リン酸化p62によるNrf2活性化を防ぐ新規化合物K67を同定し、K67が肝細胞がん細胞の増殖を半分以下に抑制するとともに、既存の抗がん剤の薬効を高めることを確認した(図2)。
図2
3.今後の展望
現在、臨床応用を目指しK67の薬効を高めるK67誘導体の開発、NRF2自体を標的にした薬剤開発を進めています。これらの薬剤は肝細胞がん治療薬として期待されます。
用語説明
- 1. p62/SQSTM1:
- 細胞生存、細胞増殖、そして細胞死に関与する多機能タンパク質であり、オートファジーによりその量的制御を受けている。
- 2. Nrf2(NFE2L2):
- Nuclear factor (erythroid-derived2)-like 2の略。転写因子として,さまざまな生体防御に関わる遺伝子群を活性化する。
- 3. グルタミノリシス:
- グルタミンから乳酸が産生される経路。さまざまな同化経路に利用されるTCA回路の中間体を、グルタミンから補充する代謝経路である。
- 4. UDP-グルクロン酸:
- 生体内でUDP-グルコースから合成され、生体内に入った毒物・薬剤を抱合(グルクロン酸抱合)して細胞外に排出する中間体として使用される。
- 5. グルタチオン:
- 3つのアミノ酸(グリシン、システイン、グルタミン酸)からなるトリペプチドである。抗酸化物質の1つであり活性酸素種などから細胞を保護する補助的役割を有する。また、生体内の有機物質(抗がん剤なども含む)と結合し、抱合体となり細胞外に排出される。
- 6. HCC:
- 肝細胞がん(Hepatocellular carcinoma)の略。肝臓組織から発生する日本人のがん死因3位の悪性腫瘍である。長期の飲酒、B型やC型肝炎ウイルスの持続感染が肝臓に炎症と再生を繰り返し、肝細胞がんを発症すると考えられている。


