2023年6月16日
糖尿病性神経障害プロジェクトの鈴木マリ元研究員らの共同研究グループは、「糖尿病性神経障害モデルショウジョウバエにおけるグリア細胞プロテアソーム機能の関与」についてiScienceに発表しました。
糖尿病性神経障害モデルショウジョウバエにおけるグリア細胞プロテアソーム機能の関与
当研究所 糖尿病性神経障害プロジェクトの鈴木マリ元研究員、三五一憲プロジェクトリーダーらは、学習記憶プロジェクトの黒見坦客員研究員、齊藤 実プロジェクトリーダーらとの共同研究により、糖尿病性神経障害の新規発症・増悪機序を明らかにしました。高糖質食で飼育したショウジョウバエでは高血糖、インスリン抵抗性など2型糖尿病の病態を示し、通常食飼育のハエに比べて熱逃避行動の低下や脚の感覚神経細胞の萎縮がみられました。熱逃避行動障害を指標とした遺伝子スクリーニングの結果、プロテアソーム関連遺伝子PSMD9のハエホモログを修飾因子として同定しました。さらにグリア細胞におけるプロテアソーム機能を抑制することにより熱逃避行動障害の抑制がみられました。以上のことから、グリア細胞におけるタンパク質恒常性(プロテオスタシス)が糖尿病性神経障害の発症に関与することが示唆されました。
本研究は鈴木謙三記念医科学応用財団、武田科学振興財団、医療法人社団健朗会研究奨励寄付金、文部科学省研究費補助金の支援を受けて実施されました。
この研究成果は、2023年6月16日に国際学術誌「iScience」に掲載されました。
- <論文名>
- “A Drosophila model of diabetic neuropathy reveals a role of proteasome activity in the glia”
(糖尿病性神経障害モデルショウジョウバエにおけるグリア細胞プロテアソーム機能の関与) - <発表雑誌>
- iScience
DOI:10.1016/j.isci.2023.106997
URL:https://www.cell.com/iscience/fulltext/S2589-0042(23)01074-X
研究の背景
ショウジョウバエは遺伝学的解析に優れた小型モデル動物の一つであり、哺乳動物モデルに比べてハイスループットな個体解析が可能です。ヒト疾患遺伝子の77%がショウジョウバエにも保存されていることが知られ、ヒトの疾患研究において有用なツールとして広く利用されてきました。またショウジョウバエの神経内分泌系・シグナル伝達機構が哺乳類と全体的な構成が類似していることは以前から知られており、高糖質食や高脂肪食を与えることで、高血糖や高インスリン血症、インスリン抵抗性などの2型糖尿病1)と同様の症状が引き起こされることも明らかとなっています。糖尿病の慢性合併症の一つである糖尿病性神経障害2)の発症・増悪には、様々な組織・細胞間の相互作用の異常が深く関与すると考えられますが、遺伝子や薬剤スクリーニングに適した小型動物の研究モデルは開発されていませんでした。そこで我々は、遺伝学的スクリーニングによる新たな疾患関連遺伝子の同定と発症メカニズムの解明を目的として、ショウジョウバエを用いた糖尿病性神経障害モデルの確立を試みました。
研究の概要
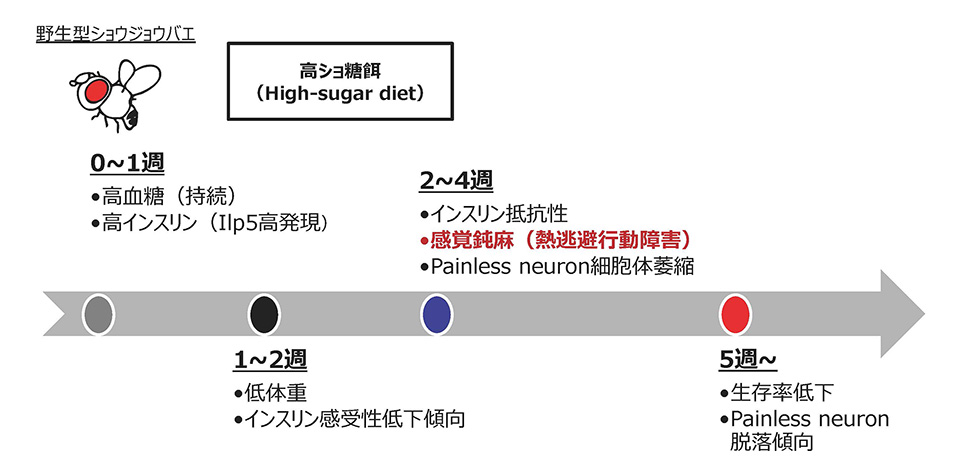
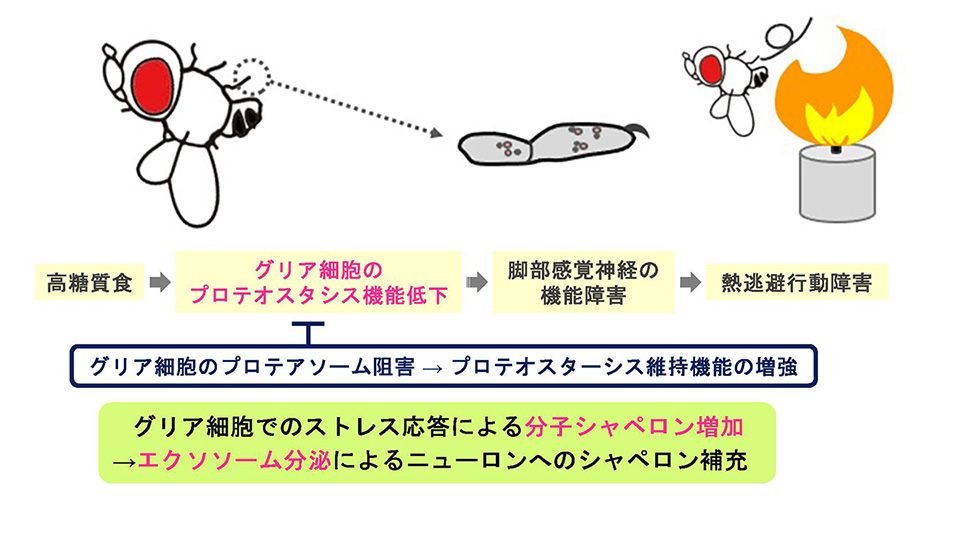
30%ショ糖を含む高糖質餌で飼育した野生型ハエでは通常食飼育のハエに比べ、1〜2週間で高血糖・インスリン抵抗性など糖尿病様の変化が認められました。さらに2週間以後では脚部感覚神経細胞 (painless neuron) の萎縮を伴う侵害性熱逃避行動の低下が見られ、末梢神経障害の進行が示唆されました(図1)。この熱逃避行動を指標として遺伝学的スクリーニングを進め、proteasome 26S subunit, non-ATPase 9 (PSMD9) など複数のプロテオスタシス(タンパク質恒常性)関連分子を同定しました。さらに、グリア細胞3)のPSMD9ノックダウンやプロテアソーム4)阻害薬により、熱逃避行動障害が抑制されることを明らかにしました。グリア細胞株を用いたプロテオーム解析では、プロテアソーム阻害薬によるHeat shock protein 40 (Hsp40) などの分子シャペロン5)群の増加が認められ、ショウジョウバエのグリア細胞特異的にHsp40を発現抑制するとプロテアソーム阻害薬の効果が見られなくなりました。以上のことから、グリア細胞のプロテオスタシス機能低下が糖尿病性神経障害モデルショウジョウバエの熱逃避行動障害発症に関与すると考えられました。糖尿病によりグリア細胞のプロテオスタシス機能が低下し、ニューロンに影響することで感覚障害が引き起こされます。しかし事前にプロテアソーム阻害でグリア細胞のストレス応答を誘導し、Hsp40の増加などプロテオスタシス維持機能が増強されると、感覚障害が抑制されるのではないかと推察されました(図2)。
社会的意義と今後の展望
糖尿病性神経障害に対する有効な治療法は開発されておらず、血糖コントロールや対症療法に依存せざるを得ない状況が続いています。本研究成果を踏まえ、今後さらに糖尿病マウスモデルを用いて分子シャペロン誘導剤の効果を検証するなどして、グリア細胞プロテオスタシスが糖尿病性神経障害の新たな治療標的となる可能性を示したいと考えています。
<用語解説>
- 1) 2型糖尿病:
- 我が国の糖尿病患者の約95%を占め、遺伝的素因に肥満や運動不足等の生活習慣が加わって、多くは中年期以降に発症する。成因として、膵ランゲルハンス島β細胞からのインスリン分泌不全や、筋肉や脂肪組織における糖利用の異常(インスリン抵抗性)等が知られている。
- 2) 糖尿病性神経障害:
- 糖尿病の慢性合併症の中で最も早期に出現し、末梢の感覚、運動、自律神経が障害されることにより多彩な臨床症状を呈する。感覚神経障害による両側四肢末端の痛みやしびれ等が特徴的な症状だが、病期が進行すれば逆に感覚が低下し足のケガや火傷に気付かず、潰瘍や壊疽(えそ)を招いて足切断の原因ともなる。また自律神経障害が進行すると、重症不整脈や無痛性心筋梗塞等の深刻な事態を招く。
- 3) グリア細胞:
- 神経細胞(ニューロン)の生存や機能維持に不可欠な細胞で、哺乳類の中枢神経ではアストロサイト、オリゴデンドロサイト、ミクログリアなどがある。末梢神経ではシュワン細胞が唯一のグリア細胞で、ニューロンの代謝維持、神経栄養因子の産生、髄鞘形成などを担っている。
- 4) プロテアソーム:
- 生体内でタンパク質の分解を担う巨大な酵素複合体。 不要になったり劣化したりしたタンパク質にユビキチンが付加し、このユビキチン化されたタンパク質を標的として、分解および再利用が進められる。細胞内のプロテオスタシス(タンパク質恒常性)維持に中心的な役割を果たし、細胞周期制御や免疫応答、シグナル伝達などに関与する。
- 5) 分子シャペロン:
- 細胞内でタンパク質が凝集することなく、そのアミノ酸の配列順序で決まる立体構造に「自ら折りたたむ (folding) 」ことを介助するタンパク質ファミリー。さまざまなタンパク質と相互作用することにより、タンパク質の正しい会合を介添えしたり、高温や高塩濃度などのストレス環境から細胞を保護したりするなどの重要な働きを担う。
