2023年11月9日
体内時計プロジェクト倉林伸博主席研究員(当時 富山大学学術研究部医学系)らは「ダウン症候群において脳機能異常が起こる仕組みの理解へ前進~新規ダウン症モデルマウスの脳発生異常を報告~」を iScience に発表しました。
ダウン症候群において脳機能異常が起こる仕組みの理解へ前進
~新規ダウン症モデルマウスの脳発生異常を報告~
- <論文名>
- “Neocortical neuronal production and maturation defects in the TcMAC21 mouse model of Down syndrome”
(ダウン症モデルマウスTcMAC21の大脳新皮質における神経細胞の産生や成熟の異常) - <著者>
- 倉林伸博、藤井一希、乙部優太、廣木進吾、平塚正治、吉種光、香月康宏、高雄啓三
- <発表雑誌>
- iScience
DOI:https://doi.org/10.1016/j.isci.2023.108379
URL:https://www.sciencedirect.com/science/article/pii/S2589004223024562?via%3Dihub
ポイント
- 21番染色体*1が3倍体になるダウン症候群(ダウン症)において、脳の発生が異常になる仕組みを発見した。
- これまででダウン症を最も良く再現していると考えられるTcMAC21モデルマウスにおける脳の発生異常を世界で初めて報告した。
- ダウン症において脳機能の異常が発症する仕組みの理解に寄与すると共に、将来の治療戦略の確立のための重要な指針の提供が期待できる。
概要
当研究所 体内時計プロジェクト倉林伸博主席研究員(当時 富山大学学術研究部医学系)と富山大学学術研究部医学系の高雄啓三教授は、体内時計プロジェクトの吉種光プロジェクトリーダー、鳥取大学医学部生命科学科/染色体工学研究センターの香月康宏教授と共に、ダウン症のモデルマウスにおける脳の発生異常の解析を行った。すなわち、これまででダウン症を最も良く再現していると考えられるTcMAC21マウスのモデルを用いた解析により、このマウスの脳の発生異常がヒトのダウン症で認められる脳の特徴と類似していることが明らかとなった。今後、このマウスを用いたダウン症研究が発展することにより、ダウン症において脳機能障害が引き起こされる仕組みの解明や、その症状改善のための治療法・治療薬の開発が加速することが期待される。
研究の背景
ダウン症は、通常は2本である21番目の染色体が3本(トリソミー)になることで引き起こされる先天性疾患で、発育の遅れや知的障害などのさまざまな症状があることが知られている。ダウン症において知的障害が引き起こされる仕組みの解明や治療薬開発を目指して、これまで、ダウン症様の症状を示す様々なモデルマウスが開発され、その脳発生の異常が解析されてきた。しかしながら、発現する異常がモデルマウス間で異なったり、ヒトのダウン症の症状が部分的に再現されていないなどの課題があった。この原因の一つとして、用いられてきたモデルマウスが部分トリソミー(21番染色体上にある遺伝子の一部しか3つになっていない)であることが考えられ、より適切なモデルマウスでの脳発生の解析が求められていた。
研究の内容・成果
富山大学学術研究部医学系の倉林伸博講師(現:当研究所 主席研究員)と高雄啓三教授は、鳥取大学医学部生命科学科/染色体工学研究センターの香月康宏教授との共同研究により、ヒト21番染色体上の遺伝子の93%以上がトリソミーであるTcMAC21マウスの脳発生を解析し、その結果を世界で初めて報告した。
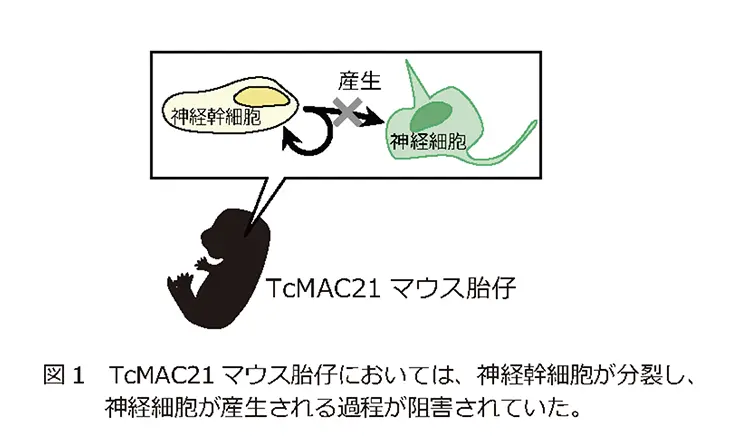
すなわち、脳を構成する神経細胞やグリア細胞*2 は、神経幹細胞(神経細胞を生み出す親細胞)が非対称に分裂することで生み出されるが、TcMAC21マウスの胎仔脳から切片を作製し、免疫組織染色*3によって神経幹細胞の数を調べたところ、その数は通常のマウスとほとんど変化がなかった。しかし、神経幹細胞の分裂の頻度を調べたところ、TcMAC21マウスにおいて分裂の頻度が低下していることが判った。さらに、神経幹細胞から神経細胞が産み出される過程を調べたところ、TcMAC21マウスにおいてこの過程が阻害されていることが明らかとなった(図1)。
次に、成体のTcMAC21マウスを用いた実験により、脳で産生された神経細胞の数を調べた。大脳新皮質を構成する神経細胞は、興奮性の錐体ニューロンと抑制性の介在ニューロンに大別される。先ず、3種類の錐体ニューロンを識別する方法で各個にニューロンの数を調べたところ、どの種類の錐体ニューロンも、TcMAC21マウスで数が減少していた。介在ニューロンに関しては、4種類を識別する方法で同様に数を調べたところ、2種類のニューロン(パルブアルブミンを発現する介在ニューロンとソマトスタチンを発現する介在ニューロン)の数が減少していることが判った。また、グリア細胞の数を調べたところ、アストロサイト*4やミクログリア*5の数には差が認められなかったが、成熟したオリゴデンドロサイト*6の割合がTcMAC21マウスにおいて低下していることが見出された(図2)。以上のように、TcMAC21マウスにおける脳発生の異常が明らかとなったが、重要なことに、以上の観察された特徴は、ヒトのダウン症脳で認められる現象と良く類似していた。

一方、脳発生の異常に伴って、TcMAC21マウスは記憶学習能力が低下することが知られている。そこで、脳機能の異常が引き起こされる仕組みに迫るため、当研究所の吉種光プロジェクトリーダーとの共同研究により、タンパク質を網羅的に解析できるプロテオーム解析を行った。その結果、タンパク質の機能制御に重要である「リン酸化*7」の程度が、TcMAC21マウスで変化していることが明らかとなった。特に、リン酸化の程度が減少しているタンパク質の中では、神経細胞やシナプス*8の成熟に関係しているタンパク質が多いことが判った。この結果から、TcMAC21マウスにおいては神経細胞が正常に働くためのリン酸化の制御に異常があり、これが学習記憶障害などの脳機能異常に関与している可能性が示された。
今後の展開
ダウン症はおよそ800人の新生児あたりに1人という頻度で発生しており、知的障害を引き起こす疾患の中では最も頻度が高い。すなわち、ダウン症の治療戦略の確立は社会的要請が極めて高いと言える。今後、TcMAC21マウスを用いたさらなる研究により、ダウン症において脳の正常な形成や発達を妨げる分子メカニズムの詳細が明らかになれば、ダウン症の発症の仕組みが解き明かされ、症状を緩和する治療法の確立に重要な手がかりが提供されると期待される。
用語解説
- *1 染色体
- 細胞の中にあり、複数の遺伝子が存在する構造体の名称。1本の染色体には数百~数千の遺伝子が含まれており、人間の細胞は通常、23対(計46本)の染色体をもつ。
- *2 グリア細胞
- 神経系を構成する細胞の中で、神経細胞ではない細胞の総称。アストロサイト・ミクログリア・オリゴデンドロサイトなどに分類される(*4、*5、*6参照)。
- *3 免疫組織染色
- 組織切片中のタンパク質などの位置を検出するために、抗体を用いてこれらを可視化・解析する実験手法。
- *4 アストロサイト
- 脳を構成するグリア細胞の一つ。構造面で神経細胞のネットワークを支える機能や、物質の輸送を介してアストロサイト周辺の様々な環境を調節する機能を持つ。
- *5 ミクログリア
- グリア細胞の一つで、免疫のほか、異常代謝物などの回収を担う細胞。
- *6 オリゴデンドロサイト
- グリア細胞の一つで、神経細胞に巻き付き、巻きついた神経細胞の維持と栄養補給の機能を持つ。
- *7 リン酸化
- ここではタンパク質にリン酸基を付加させる化学反応のことを指す。これにより、タンパク質の構造や機能が変化する例が多く知られている。
- *8 シナプス
- 主に神経細胞間で形成される接合部位とその構造のことを指し、細胞間の情報伝達など、神経活動に関わる部位である。
