2023年12月18日
幹細胞プロジェクトの北島健二主席研究員らは「ヒトiPS細胞からマクロファージへの分化誘導方法を開発」について「International Immunology」に発表しました。
ヒトiPS細胞からマクロファージへの分化誘導方法を開発
当研究所幹細胞プロジェクトの北島健二主席研究員、原孝彦参事研究員、真貝美奈子研修生(現タカラバイオ)、安藤輝研修生らは、ヒトiPS細胞からマクロファージへの分化を効率よく誘導できる培養方法を開発し、日本免疫学会の国際学術雑誌に発表しました。
- <論文名>
- “FLT3 signaling augments macrophage production from human pluripotent stem cells.”
- <著者>
- Kitajima K, Shingai M, Ando H, Hara T.
- <発表雑誌>
- International Immunology 2023 Dec 18:dxad047.
DOI:10.1093/intimm/dxad047.
研究の背景
ヒトiPS細胞から作られた赤血球・白血球・血小板などの血液細胞は、がん免疫療法や再生医療、医薬品開発などの研究材料として有用です。そこで、私たちはヒトiPS細胞から効率よく血液細胞を得るための培養方法の研究を行っています。以前、私たちはWNTシグナルの制御に関与しているGSK3βの阻害剤CHIR99021がヒトiPS細胞から血液細胞への分化を顕著に促進することを発見しました(Kitajima et al. 2016)。さらに、この知見を活用し、CHIR99021処理したヒトiPS細胞を3次元培養(オルガノイド培養)することにより、血液細胞の源である造血幹前駆細胞の特徴を示す細胞(CD45陽性・CD34陽性・LIN陰性・CD38陰性・CD90陽性;以降、ヒトiPS由来造血幹前駆細胞と略す)を得ることに成功しました(Kitajima et al. 2022)。
しかし、このヒトiPS由来造血幹前駆細胞は、本来の造血幹前駆細胞の特徴である「長期骨髄再建能*1」をほとんど示さないことが明らかとなり、ヒトiPS細胞由来造血幹前駆細胞は、何らかの因子が欠損している可能性が惹起されました。そこで、ヒトiPS由来造血幹前駆細胞とヒト臍帯血から採取した造血幹前駆細胞の遺伝子発現を比較したところ、ヒト臍帯血の造血幹前駆細胞では高い発現を示すFLT3という受容体型チロシンキナーゼがヒトiPS由来造血幹前駆細胞では発現していないことを発見しました(Kitajima et al. 2022)。FLT3は細胞膜表面に発現し、サイトカインFLT3Lにより活性化されます。そこで、FLT3遺伝子を安定発現するヒトiPS細胞株(ヒトFLT3-iPS細胞)を作成し、FLT3Lを培養液中に添加してオルガノイド培養を行いました。残念ながら、長期骨髄再建能の獲得には至りませんでしたが、マクロファージや好中球などの免疫細胞の直接の前駆細胞である骨髄系造血前駆細胞が大量に得られることが判明しました(Kitajima et al. 2022)。
研究内容
マクロファージは、体内に侵入した病原性微生物の貪食による殺菌や死細胞の排除による組織の恒常性維持を司っている自然免疫の細胞です。また、Tリンパ球などの獲得免疫を活性化する役割も担っています。マクロファージ研究は、主にマウス由来のものが用いられています。しかし、マウスで得られた知見がヒトにおいても同様であるかどうかは疑問です。もし、ヒトiPS細胞から得られたマクロファージが研究に利用できるのであれば、ヒトのマクロファージ研究に多大な貢献をもたらします。
上述したように、FLT3はヒトiPS細胞から骨髄系造血前駆細胞の誘導を大幅に促進します。そこで、FLT3を上手に利用すれば、ヒトiPS細胞からマクロファージを大量に得るための新培養システムが構築できるのではないかと考えられます。そこで、ヒトiPS細胞からマクロファージへの分化誘導を行ったところ、FLT3の活性化により大量にマクロファージが得られることを見出しました(図1A)。次に、FLT3を利用して得られたヒトiPS由来マクロファージが、マクロファージ本来の機能を有しているのかどうかを調べたところ、通常のマクロファージの特徴や機能を有していることがわかりました(図1BC)。
マクロファージに、ガン細胞に特異的に結合する人工的な受容体を発現させると、ガン細胞を認識して接着し、貪食により退治します。この受容体は、キメラ抗原受容体(Chimeric Antigen Receptor;CAR)と呼ばれており、すでにTリンパ球では白血病などの治療に用いられています(CAR-T療法)。将来、CAR-T療法では効果の低いガン治療へのマクロファージの利用が見込まれており、ヒトiPS細胞由来のマクロファージは、この新しいガン治療法の開発のための研究材料として期待されます。
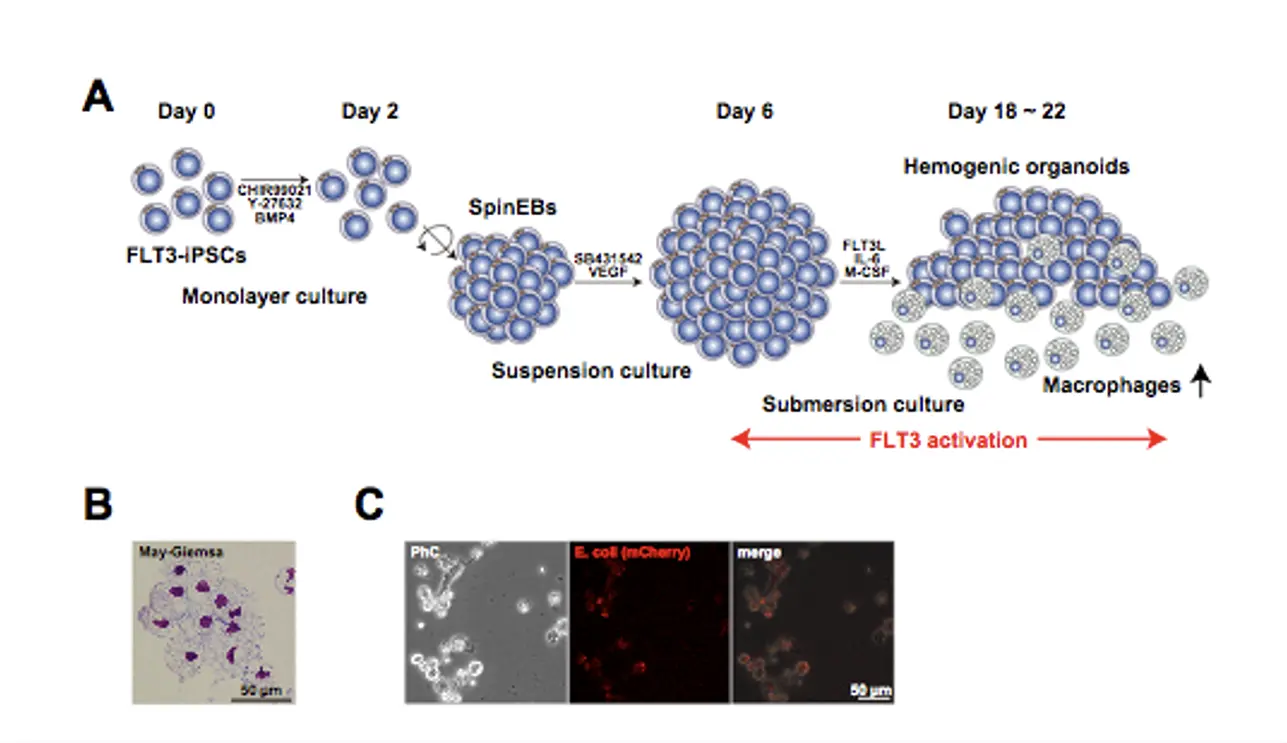
図1
(A)ヒトiPS細胞からマクロファージへの分化誘導。ヒトiPS細胞をCHIR99021などの化合物存在下で、2日間(Day 0 - 2)培養後、胚様体(SpinEBs)を作成する。この胚様体をVEGFなどのサイトカイン存在下で4日間(Day 2 - 6)培養後、M-CSFなどのサイトカイン存在下で浸漬培養する。FLT3を発現するヒトiPS細胞を用い、Day 6からFLT3Lを加えて培養すると、大量のマクロファージが得られることが判明した。(B,C)ヒトiPS細胞からFLT3/FLT3Lの活性化により得られたマクロファージの塗抹標本像(B)と、大腸菌のファゴサイトーシス(C)。(B)May-Grünwald/Giemsa染色後の顕微鏡写真を示す。特徴的なマクロファージの形態を示す細胞が多数認められる。(C)マクロファージに赤色蛍光タンパクmCherryを発現する大腸菌を加えたところ、貪食(ファゴサイトーシス)を示す細胞が多数認められた。<参考文献>
- Kitajima et al. (2016) GSK3β inhibition activates the CDX/HOX pathway and promotes hemogenic endothelial progenitor differentiation from human pluripotent stem cells. Exp Hematol. 44:68-74.
- Kitajima et al. (2022) An Interferon-γ/FLT3 Axis Positively Regulates Hematopoietic Progenitor Cell Expansion from Human Pluripotent Stem Cells. Stem Cells. 40(10):906-918.
