
2017年10月9日
英国科学誌 『Scientific Reports』 に松田憲之研究員(ユビキチンプロジェクト)と田中啓二所長らが 「遺伝性パーキンソン病の発症にアルデヒドが関与する~パーキンソン病の発症原因のさらなる理解につながる発見~」 について発表しました。
遺伝性パーキンソン病の発症にアルデヒドが関与する
~パーキンソン病の発症原因のさらなる理解につながる発見~
当研究所の松田憲之・ユビキチンプロジェクトリーダーと田中啓二所長らのグループは、兵庫県立大学 ピコバイオロジー研究所の水島恒裕教授、首都大学東京 理工学研究科の伊藤隆教授・三島正規准教授らとの共同研究によって、遺伝性のパーキンソン病(※1)に関係するDJ-1タンパク質が、アルデヒド(※2)の解毒を介してミトコンドリア(※3)の機能を助けることで、パーキンソン病の発症を抑えていることを世界で最初に明らかにしました。本発見は、アルデヒド解毒という純粋な基礎科学分野の成果として興味深いものであると同時に、パーキンソン病の新たな発症原因を提唱する成果です。
この研究成果は、2017年10月9日午前10時(英国時間)に英国科学誌『Scientific Reports』にオンライン掲載されました。
- <論文タイトル>
- Parkinson's disease-related DJ-1 functions in thiol quality control against aldehyde attack in vitro
- <発表雑誌>
- 英国科学誌 「Scientific Reports」、 2017年10月9日午前10時(英国時間)
https://www.nature.com/articles/s41598-017-13146-0
1.研究の背景
パーキンソン病は、神経伝達物質であるドーパミンを産生する神経細胞が失われることにより、安静時のふるえや歩行障害(すり足,小股、前屈姿勢など)、姿勢保持障害(例えば歩き出したり後方に引かれたりすると、止まれずに突進してしまう)、動作緩慢(動きが遅くなったり少なくなることで、細かい作業が困難になる)など様々な運動障害が起こる病気です。病状が進行すると自律神経障害、記憶力低下などの認知機能障害、幻視やうつなどの精神症状が表れることもあり、最終的に自立した生活が困難になり、車いすや寝たきりの生活になる危険性があります。
パーキンソン病は日本国内だけでも15万人を超える患者がいる難治性の神経変性疾患(※4)であり、高齢者ほど患者数が多く、65歳を超えると1%以上の人が罹患するといわれています。パーキンソン病の発症原因は完全に解明されているわけではありませんが、古くから(1990年代-)ミトコンドリアの機能低下が病気の発症に関係することが示唆されていました。社会の高齢化が進むにつれて患者数は増え続けており、パーキンソン病が発症する仕組みの解明と、早期診断法や根本的な治療法の確立が社会的に強く求められています。
パーキンソン病にはいくつかのタイプがあり、発症原因も単一ではないと考えられますが、PINK1, Parkin, DJ-1という遺伝子(及びその遺伝子によって作られるPINK1・Parkin・DJ-1タンパク質)に変異が起こると、パーキンソン病を若くして発症します。これらの疾患を遺伝性潜性(劣性)パーキンソン病といいます。変異によって遺伝子の機能が失われると病気が発症するので、PINK1・Parkin・DJ-1が普段は“パーキンソン病の発症を抑えるために働いている”ことが判ります。2010年から2015年にかけて、松田プロジェクトリーダーと田中所長らの研究グループは、“PINK1とParkinが低品質なミトコンドリアを分解してミトコンドリアの品質を保つことで遺伝性パーキンソン病の発症を抑えている”ことを明らかにしてきました。
一方でDJ-1の生体内の機能として、細胞内の酸化ストレス(※5)に対抗することや、ミトコンドリアの機能維持に重要であることが報告されています。しかしながらその機能については諸説あって、DJ-1が遺伝性潜性(劣性)パーキンソン病の原因遺伝子であることが報告されてから既に15年近くが経つにもかかわらずに、未だ結論に至っていません。DJ-1の分子機能はパーキンソン病の研究者が解明すべき重要な謎と考えられています。
2.研究成果の概要
松田プロジェクトリーダー・田中所長らの研究グループは、DJ-1の進化的保存性に着目して研究を開始しました。つまり、DJ-1はパーキンソン病の原因遺伝子であるにもかかわらず、神経を持たない植物や酵母、さらには細菌のような下等微生物にも相同な遺伝子が存在します。そして細菌のDJ-1相同遺伝子はメチルグリオキサール(※6)などの生体内アルデヒドの解毒に関与しています。
研究グループはこの点に着目して研究を進め、ミトコンドリアでエネルギーを産生する時に重要な役割を果たす低分子化合物である補酵素A(※7)とメチルグリオキサールが反応した物質(反応産物)をDJ-1が分解して、正常な補酵素Aと無害な乳酸に変えることを発見しました。さらにパーキンソン病の患者さんが持つ遺伝子変異によって、DJ-1のこの働きが阻害されることを発見しました。補酵素Aはミトコンドリアの機能に必須の役割を担っているので、一連の結果から「DJ-1がメチルグリオキサールというアルデヒドの解毒を介してミトコンドリアの機能を助けることで、パーキンソン病の発症を抑えている」ことが示唆されます(次ページ添付図参照)。
3.本研究の意義
3-1 基礎研究としての意義:ミトコンドリアの機能低下がパーキンソン病の発症に関与することは、既に膨大な数の論文から示唆されています。しかしながら、“ミトコンドリア機能に必須な低分子をアルデヒドから守る防御機構が破綻することで、パーキンソン病が発症する”という観点の研究は今まで行なわれておらず、本論文が発症機構に対する新たな展開の契機になると期待されます。また、本成果は遺伝性パーキンソン病に関するものですが、より一般的な孤発性パーキンソン病についても同様の仕組みが発症に関与している可能性は十分にあります。実際、アルデヒドと反応した低分子化合物が孤発性のパーキンソン病の患者で増加しているという論文も報告されています (Naoi et al., Ann Neurol 43, 212-216, 1998 など)。
3-2 応用研究としての意義:生体内の低分子化合物とアルデヒドが反応したテトラヒドロイソキノリン(TIQ)やサルソリノールという物質が神経毒性を持つことや、パーキンソン病の患者で量が増加していることが既に報告されています(Naoi et al., Neurotoxicol Teratol, 24, pp579-591, 2002 など)。そこで、本研究で示されたメチルグリオキサール-補酵素A 複合体のような“アルデヒドの付加した低分子化合物”が、パーキンソン病の細胞モデルや動物モデルを作製する際の道具となる可能性や、パーキンソン病の新しい診断マーカーになる可能性があります。しかしながら、これらに関しては現時点で実験系を確立していたり、データを得ているわけではなく、今後の課題として長期的な視野で取り組んでいきたいと考えています。つまり、本研究はすぐにパーキンソン病の治療法の開発に結びつく知見というよりは、病気を理解する上で重要な基礎研究と考えていただければ幸いです。
4.世界的な動向
再生医療や癌、パーキンソン病、アルツハイマー病といった分野では国際的に激しい競争が行なわれているので、類似した内容や関連した内容の論文がほぼ同時に報告されることはよくあります。今回もフランスのジャコブ・モノー研究所のRicharme博士らによって「グアニンとメチルグリオキサールが結合した反応産物をDJ-1が分解する」ことが報告されました(Richarme et al., Science 357, 208-211, July 14)。グアニンはミトコンドリアに関係するというよりも、DNA/RNAの材料としての重要性が知られている物質です。その意味で、この論文の内容と松田プロジェクトリーダー・田中所長らの論文の内容が完全に一致する訳ではありませんが、少なくとも「DJ-1タンパク質がメチルグリオキサール(アルデヒド)と反応した低分子化合物を分解・解毒する」というコンセプトは良く一致しており、今後はこのような観点での研究が世界中で展開されていくと思われます。
<模式図>
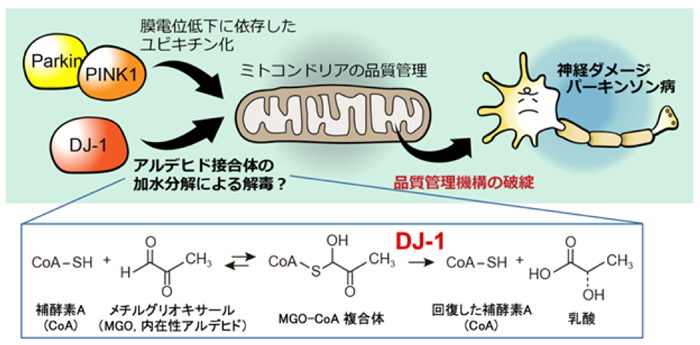
<図の説明>
通常時には、DJ-1が内在性のアルデヒドであるメチルグリオキサールと反応した補酵素Aを分解して、無害な乳酸と正常な補酵素Aに戻しています(下半分図)。しかしながら、DJ-1の遺伝子変異などでこの反応が破綻すると、メチルグリオキサールが蓄積したり正常な補酵素Aが減少したりして、ミトコンドリアの機能が低下して、パーキンソン病の発症に至ると予想されます(上半分図)。
用語解説
- *1: パーキンソン病
- ふるえや手足のこわばり、歩行障害、動作緩慢、転びやすさなどの症状がある神経変性疾患のひとつ。治療は症状を緩和する薬物治療が基本で、様々な運動療法によるリハビリテーションと組み合わされることが多いです。脳内で不足するドーパミンを補う対症療法が効果を上げていますが、根本的な治療法はまだ見つかっていません。
パーキンソン病は孤発性のものと、遺伝性のもの(厳密には、遺伝性パーキンソン症候群と呼ばれます)に大別されます。患者の大部分(8−9割)は孤発性のパーキンソン病に分類されますが、環境要因や生活習慣を含めて多面的な因子が発症に関与するので、病気の原因を絞り込むことが困難です。一方で、遺伝性のパーキンソン病が患者全体に占める比率は1−2割と考えられますが、病気の原因が単一遺伝子の変異であり、病気と発症原因の因果関係がはっきりしています。松田憲之プロジェクトリーダーと田中所長らのグループは、遺伝性パーキンソン病を引き起こす遺伝子の研究から病気の発症機構を明らかにするべく、10年以上に亘って研究を行ってきました。 - *2: アルデヒド
- 高い反応性を持ち、生物にとって有毒な有機化合物。一般化学式 R-CHO で表されます。よく知られているのはエタノールが体内で分解される過程で生じるアセトアルデヒドで、いわゆる二日酔いを引き起こします。生体内には、他にも毒性を発揮する内在性のアルデヒドとして、アルドース・ホルムアルデヒド・メチルグリオキサール(※6)などが存在します。いずれもタンパク質やDNAと反応することでその機能を阻害したり、架橋形成を介して凝固させたりする作用を持ちます。
- *3: ミトコンドリア
- 細胞の中に存在する小さな小部屋(細胞小器官/オルガネラ)の一つ。細長い二重の膜で包まれた袋状の構造体で、人間が生きていくために必要なエネルギー(アデノシン三リン酸:ATP)を産生する場所なので「細胞内のエネルギー産生工場」や「細胞内の発電所」とも言われます。ATPを産生できないミトコンドリアは「不良品」であり、このようなミトコンドリアをうまく処分できないことがパーキンソン病の発症につながることを示唆する論文が、多数報告されています。
- *4: 神経変性疾患
- 主に成人期以降に発症する脳の病気で、特定の神経細胞が異常になって死んでしまう(神経が変性して脱落する)ことが原因で発症します。パーキンソン病のほか、アルツハイマー病、筋萎縮性側索硬化症(ALS)、ハンチントン病などが知られています。
- *5: 酸化ストレス
- 生体内ではミトコンドリア呼吸や紫外線などによって恒常的に有害な活性酸素種が生じていますが、普段は還元されて無毒化されています。一方で、細胞内の酸化還元状態を維持する機構が破綻して活性酸素種が過剰に生じると、生体は酸化ストレスの状態に陥ります。近年では、ガンや神経変性疾患を含む様々な病気にこの酸化ストレスが関与していると言われています。
- *6: メチルグリオキサール
- 生体内で産生されるアルデヒドの一種。糖(グルコース)を分解してエネルギーを得る過程で必要な代謝系(解糖系)の副産物として生じます。化学式はCH3C(O)CHOです。
- *7: 補酵素A
- ミトコンドリアでエネルギーを産生する時に重要な役割を果たす低分子化合物で、CoAとも呼ばれます。糖(グルコース)からエネルギーを得る際には、解糖系ーTCA回路と言われる代謝経路を用いて糖を単純な低分子化合物に変換していきますが、補酵素Aはその代謝過程において炭素の受け渡しに必須の役割を担っています。

