2022年11月1日
佐伯泰プロジェクトリーダー(蛋白質代謝プロジェクト)らは、星薬科大学と東京大学と共同で「がんの治療標的タンパク質の分解を担う酵素を発見」についてNature Chemical Biology に発表しました。
がんの治療標的タンパク質の分解を担う酵素を発見
―がん治療の新たなコンセプト「分解創薬」を新たなステージへ―
星薬科大学の大竹史明特任准教授、秋月慶乃大学院生らの研究グループは当研究所と東京大学と共同で、がんの治療標的となるタンパク質「cIAP1」を薬剤によって細胞内で分解する際に働く酵素を発見し、2022 年11月1日(日本時間)に英国科学誌ネイチャー姉妹誌『Nature Chemical Biology』に発表しました。
研究成果のポイント
- がん細胞で高発現するタンパク質「cIAP1」はがんの治療標的として知られ、薬剤によって細胞内から分解消去する技術が研究されています。
- 本研究ではcIAP1 の分解を担う酵素として「UBE2N」を発見しました。UBE2N がcIAP1 の分解を促進することで、がん細胞を細胞死に導くことをつきとめました。
- この知見は今後、高効率・高精度ながん治療薬の開発や、分解薬の有効性を患者ごと事前に評価できるオーダーメイド医療につながることが期待されます。
- <論文名>
- “cIAP1-based degraders induce degradation via branched ubiquitin architectures”
(cIAP1 分解薬は分岐型ユビキチン鎖を介してタンパク質分解を誘導する) - <著者>
- Yoshino Akizuki, Mai Morita, Yuki Mori, Ai Kaiho-Soma, Shivani Dixit, Akinori Endo, Marie Shimogawa, Gosuke Hayashi, Mikihiko Naito, Akimitsu Okamoto, Keiji Tanaka, Yasushi Saeki, and Fumiaki Ohtake*
秋月慶乃(星薬科大学 大学院薬学研究科 修士課程:筆頭著者)
森田真衣(星薬科大学 薬学部 創薬科学科 4年)
森 友紀(星薬科大学 薬学部 創薬科学科 4年)
相馬 愛(星薬科大学 先端生命科学研究所 特任助教)
Shivani Dixit(東京大学 大学院工学系研究科 博士課程(研究当時))
遠藤彬則(東京都医学総合研究所 基礎医科学研究分野 蛋白質代謝プロジェクト 主任研究員)
下川茉莉絵(東京大学 工学部 4年)
林 剛介(東京大学 大学院工学系研究科 助教(研究当時))
内藤幹彦(東京大学 大学院薬学系研究科 特任教授)
岡本晃充(東京大学 大学院工学系研究科 教授)
田中啓二(東京都医学総合研究所 理事長)
佐伯 泰(東京都医学総合研究所 基礎医科学研究分野 蛋白質代謝プロジェクト プロジェクトリーダー)
大竹史明(星薬科大学 先端生命科学研究所 特任准教授:責任著者) - <発表雑誌>
- 英国科学誌 Nature Chemical Biology
DOI:10.1038/s41589-022-01178-1
概要
星薬科大学先端生命科学研究所の大竹史明特任准教授、秋月慶乃大学院生らの研究チームは、当研究所の田中啓二理事長および佐伯泰参事研究員、東京大学の内藤幹彦特任教授および岡本晃充教授らと共同で、がんの治療標的であるタンパク質「cIAP1」を薬剤によって細胞内で分解する際に働く酵素を初めて発見しました。
がん細胞で高発現するタンパク質「cIAP1」はがんの治療標的として知られ、細胞内での分解消去を引きおこす薬剤(分解薬)は現在臨床試験が進められています。しかし、作用メカニズムには不明な点がありました。
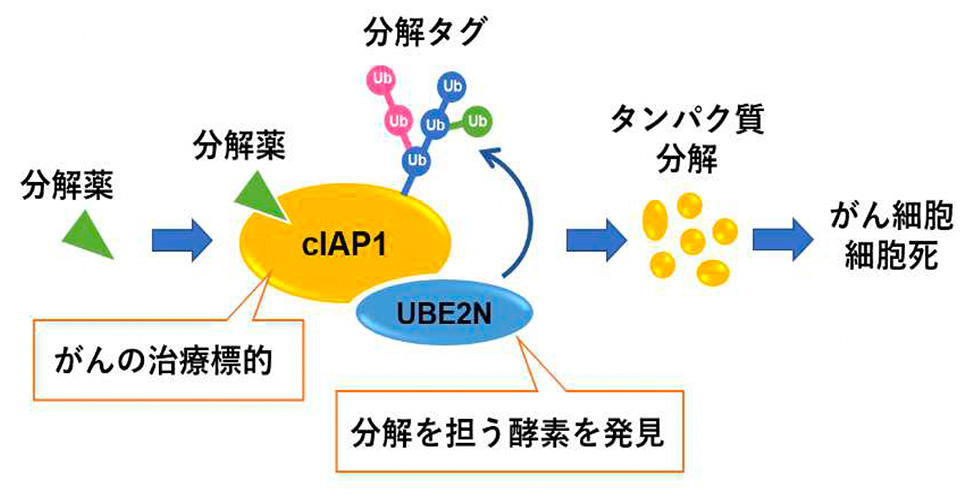
今回研究グループは、分解薬によってcIAP1 の分解が引き起こされる際に必要な酵素として「UBE2N」を発見しました(図)。UBE2N はcIAP1 に特殊な「目印」=分解タグ(ユビキチン(Ub)と呼ばれる)を付加することで、cIAP1 を分解に導くことをつきとめました。さらに、この分解促進効果によってがん細胞を細胞死に導くことがわかりました。
分解薬の効果に必要な酵素が明らかになったことで、今後、高効率ながん治療薬の開発や、分解薬の有効性を患者ごと事前に評価できるオーダーメイド医療につながることが期待されます。
研究成果は2022 年11月1日(日本時間)に英国科学誌ネイチャー姉妹誌『Nature Chemical Biology』オンライン版に掲載されました。
研究の背景
私たちの細胞内には、がん細胞の生存や増殖にとって有利に働くタンパク質が存在します。このようなタンパク質はがんの治療標的であり、薬剤によって阻害できればがん細胞の細胞死を引きおこすことができます。
このような治療標的タンパク質が数多く存在しますが、いわゆる阻害薬など既存の薬剤の標的となっているタンパク質はほんの一握り(約30%)で、それ以外の多くのタンパク質は薬剤によって阻害できませんでした。これに対して、標的タンパク質を細胞内で分解して除去する「標的タンパク質分解創薬」注1)が、創薬ターゲットの範囲を大幅に広げる革新的な創薬コンセプトとして脚光を浴びています。
標的タンパク質分解の原理は、細胞内にもともと備わっているユビキチン・プロテアソーム系注2)という機構を利用するものです。細胞内で不要になったタンパク質は、「ユビキチン」注2)と呼ばれる目印(タグ)を付加されます。タグ付け(ユビキチン化)されたタンパク質はタンパク質分解酵素「プロテアソーム」注2)によって分解されます。そこで、特殊な薬剤(分解薬)によって標的タンパク質のユビキチン化を誘導すれば、細胞内で狙ったタンパク質を分解することが可能になります。
本研究の成果
タンパク質「cIAP1」注3)はがん細胞の生存に有利に働くタンパク質であり、分解薬によってcIAP1 を細胞から除去すると、がん細胞の細胞死を引きおこすことができます。しかし、分解薬によってcIAP1 が分解されるメカニズムはよくわかってませんでした。
研究グループは、cIAP1 のユビキチン化に必要な酵素として「UBE2N」注4)を発見しました。UBE2Nは「ユビキチン結合酵素」と呼ばれる酵素群の一種です。今回、分解薬によって引き起こされるcIAP1 の分解にUBE2N が必要であることが明らかになりました。がん細胞のゲノムを操作してUBE2N の機能を減弱させたところ、分解薬によって誘導されるcIAP1 の分解や、がん細胞の細胞死が抑制されました。つまり、UBE2N は分解薬の効力発揮に必要であることがわかりました。分子レベルの解析の結果、UBE2N はcIAP1 に特殊な形状のユビキチンを付加することによって、cIAP1 の迅速な分解を引きおこすことをつきとめました。
今後の展望および波及効果
がんの治療標的となるタンパク質の分解消去を引きおこす薬剤(分解薬)は現在臨床試験が進められるなど、世界的な開発競争が進んでいます。しかし、作用メカニズムには不明な点がありました。本研究では治療標的タンパク質の一つであるcIAP1 の分解を担う酵素としてUBE2N を発見し、この酵素が特殊な形状の「分解タグ」(ユビキチン)を付加することをつきとめました。この知見から、UBE2Nが多く存在しているがんでは分解薬の効果が強いと考えられるため、薬剤の効き目をがんの種類や患者ごとに事前に予測するオーダーメイド医療につながっていく可能性が考えられます。また、将来的にUBE2N の存在量を増やしたり活性を増加させる方法が見つかれば、がんに対するより高効率な治療薬につながると考えられます。
<研究者のコメント>
- 星薬科大学・大竹史明特任准教授
標的タンパク質を分解するメカニズムがわかったことで、今後新たながん治療法の開発につながる可能性があります。 - 東京都医学総合研究所・田中啓二理事長
標的タンパク質分解誘導薬は次世代創薬のキーであり、多くの未知疾患の治療に資することが予想されています。 - 東京大学・内藤幹彦特任教授
cIAP1 の分解はからだの免疫細胞を活性化し、近年注目されているがんの免疫療法を増強することも期待されています。
<研究資金>
本研究は文部科学省科学研究費補助金(新学術領域研究「ケモテクノロジーが拓くユビキチンニューフロンティア」JP18H05498 JP18H05502)、日本医療研究開発機構(AMED-CREST 21458950)、日本学術振興会科学研究費補助金(基盤研究(B)JP21H02433)、日本学術振興会学術研究助成基金助成金(挑戦的研究(萌芽)JP20K21408)、(公財)武田科学振興財団、(公財)内藤記念科学振興財団などの支援を受けて行われました。
<用語解説>
- 注1)標的タンパク質分解創薬
- 特定の疾患原因タンパク質を分解することで細胞内から取り除く技術です。代表的な薬剤として、多発性骨髄腫の治療に使われているレナリドミドなどがあります。また、乳がん、前立腺がんに対する分解誘導剤が臨床試験に入っています。このような創薬コンセプトは「標的タンパク質分解誘導法」と呼ばれています。
- 注2)ユビキチン・プロテアソーム
- 細胞内で不要になったタンパク質は分解され、新しく合成されたタンパク質に置き換わっています。分解されるべきタンパク質を選別するための目印(タグ)の役割を果たすのが「ユビキチン」です。不要になったタンパク質は、ユビキチン付加酵素によって、ユビキチンを付加されます(ユビキチン化と呼ばれる)。ユビキチンを付加されたタンパク質は、タンパク質分解酵素である「プロテアソーム」へと運ばれて、分解されます。ユビキチンが鎖状に連なったものは「ユビキチン鎖」と呼ばれ、形状によって機能が異なると考えられています。一連の細胞内経路は「ユビキチン・プロテアソーム系」と呼ばれています。
- 注3)cIAP1
- 細胞の生存を促進、アポトーシスを抑制するタンパク質であり、炎症シグナル伝達に関わるユビキチンリガーゼです。cIAP1 が機能しなくなるとアポトーシスが誘導されます。そこで、cIAP1 タンパク質の分解を誘導する薬剤が開発されており、現在は様々な種類のがんに対して臨床試験が進められています。またcIAP1 は様々ながん細胞において、正常な細胞よりも、存在量が多いことがしられています。
- 注4)UBE2N
- ユビキチン結合酵素の一種。ユビキチン結合酵素は、ユビキチンリガーゼと相互作用して、標的となるタンパク質にユビキチンを結合させる働きをもっています。UBE2Nは乳がんや肺がんなど様々ながん細胞において、正常な細胞よりも存在量が多いことがしられています。
