2022年1月21日
認知症プロジェクトの鈴木元治郎 主席研究員、長谷川成人 参事研究員、粟汐里 研修生らは「神経細胞におけるシード依存的なαシヌクレインのリン酸化はシナプスから始まり軸索を経て細胞体へと広がる」について「Scientific Reports」に発表しました。
神経細胞におけるシード依存的なαシヌクレインのリン酸化は
シナプスから始まり軸索を経て細胞体へと広がる
- <論文名>
- "Phosphorylation of endogenous α-synuclein induced by extracellular seeds initiates at the pre-synaptic region and spreads to the cell body"
(神経細胞におけるシード依存的なαシヌクレインのリン酸化はシナプスから始まり軸索を経て細胞体へと広がる) - <発表雑誌>
- 「Scientific Reports」
DOI:10.1038/s41598-022-04780-4
URL:https://www.nature.com/articles/s41598-022-04780-4
研究の背景
神経変性疾患では多くの場合その病気に特徴的なタンパク質の線維状凝集体の蓄積が患者脳で観察されます。凝集体の蓄積と病変の広がりが相関していることから、これらの凝集体がプリオン様伝播をし、神経細胞の変性を引き起こしていると考えられます。これまでに、患者脳から抽出した凝集体や試験管内で形成したタンパク質凝集体をマウスなどの脳内に注入すると、数か月後には患者脳で見られる病理と類似した異常タンパク質の凝集体の蓄積がシード依存的に誘導されることが報告されてきました。しかし、このようなシード依存的な異常タンパク質の蓄積が、いつ?どこから?どのようにして?脳内に広がっていくかについてはほとんどわかっていませんでした。
研究の概要
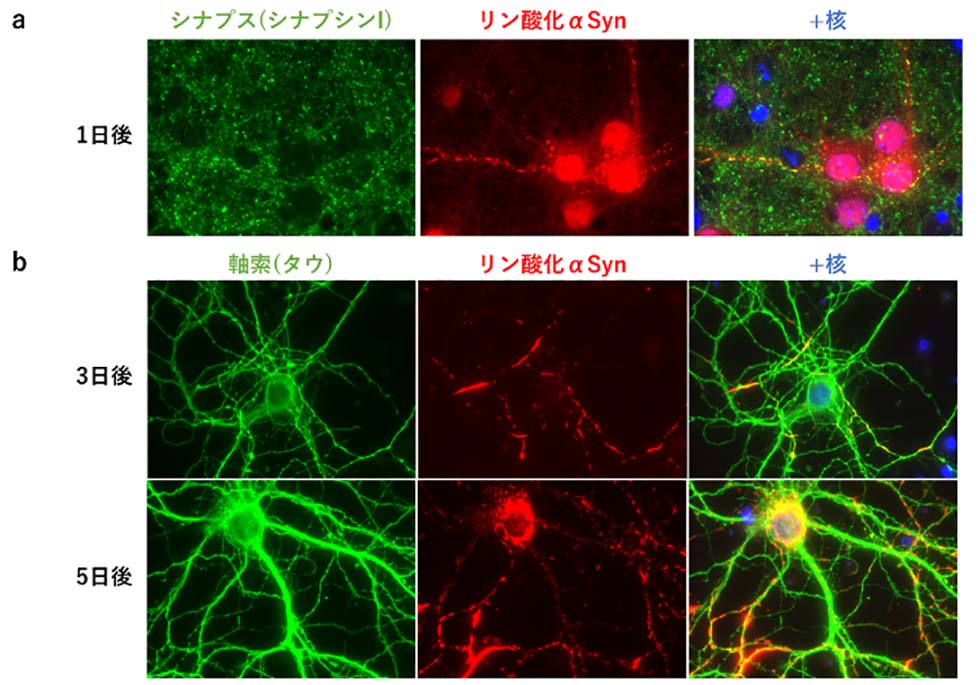
パーキンソン病、レビー小体型認知症、多系統委縮症などではαシヌクレインというタンパク質が異常リン酸化された凝集体の蓄積が観察され、これらの疾患はαシヌクレイノパチーと総称されます。これまでに試験管内で形成したαシヌクレイン凝集体を野生型マウスの脳内へ注入すると1か月後にはシード依存的なリン酸化αシヌクレイン凝集体が形成されることが報告されています。しかし、αシヌクレイン凝集体がマウス脳内に注入された後、いつ?どこから?リン酸化αシヌクレインの蓄積が誘導されるかはほとんどわかっていませんでした。そこで、試験管内で形成したαシヌクレイン凝集体を野生型マウスの海馬に注入し、3日、5日、14日後にリン酸化αシヌクレインの出現を検討したところ、注入後3日後にはすでにドット状のリン酸化αシヌクレインが出現し、5日後には線状の、14日後には神経細胞体内に凝集体状のリン酸化αシヌクレインが出現することがわかりました(図1a)。シナプス、軸索、神経細胞体のマーカータンパク質との共染色を行ったところ、注入後5日でのリン酸化αシヌクレインはシナプスや軸索に局在し、神経細胞体には局在しないことがわかりました(図1b)。また、接種部位である海馬と神経連絡をしている領域では、神経細胞体のリン酸化αシヌクレインの蓄積が認められましたが、シナプスでのリン酸化αシヌクレインの蓄積はほとんど観察されませんでした。これらのことから、リン酸化αシヌクレインは接種部位のシナプスでまず現れ、軸索を通り神経細胞体へと輸送されて凝集体を形成することが示唆されました。また、マウス胎児脳より調製した初代培養細胞にαシヌクレイン凝集体を添加すると、1日後にはシナプスでドット状のリン酸化αシヌクレインが現れ、3日後には軸索上にその局在を広げ、7日後には神経細胞体でも認められるようになりました(図2)。これらのことから、シード存在下では神経細胞のシナプスからリン酸化αシヌクレインの出現が始まり、軸索上への局在拡大を経て、神経細胞体でリン酸化αシヌクレイン凝集体が形成されることがわかりました。
本研究成果により、シード依存的なαシヌクレインのリン酸化はシナプス領域から始まることが明らかになりました。このことは、シードとなるαシヌクレイン凝集体は、シナプスから取り込まれる可能性を示唆しており、プリオン様伝播において重要な過程である神経細胞へのαシヌクレイン凝集体の取り込みを解明する端緒となることが期待されます。また、これまでのマウス脳内へのタンパク質凝集体注入実験では、注入後1か月以上経てからの病理形成をモニターしていましたが、本研究成果により3日後から病理の形成が確認でき、5日後程度では明らかな病理が形成されることがわかりました。このことは、これまで1か月以上かかっていたマウス脳内への注入による病理形成実験が一週間以内で終了できることを意味し、本実験系を利用した薬理評価などの期間が大幅に短縮されることが期待されます。
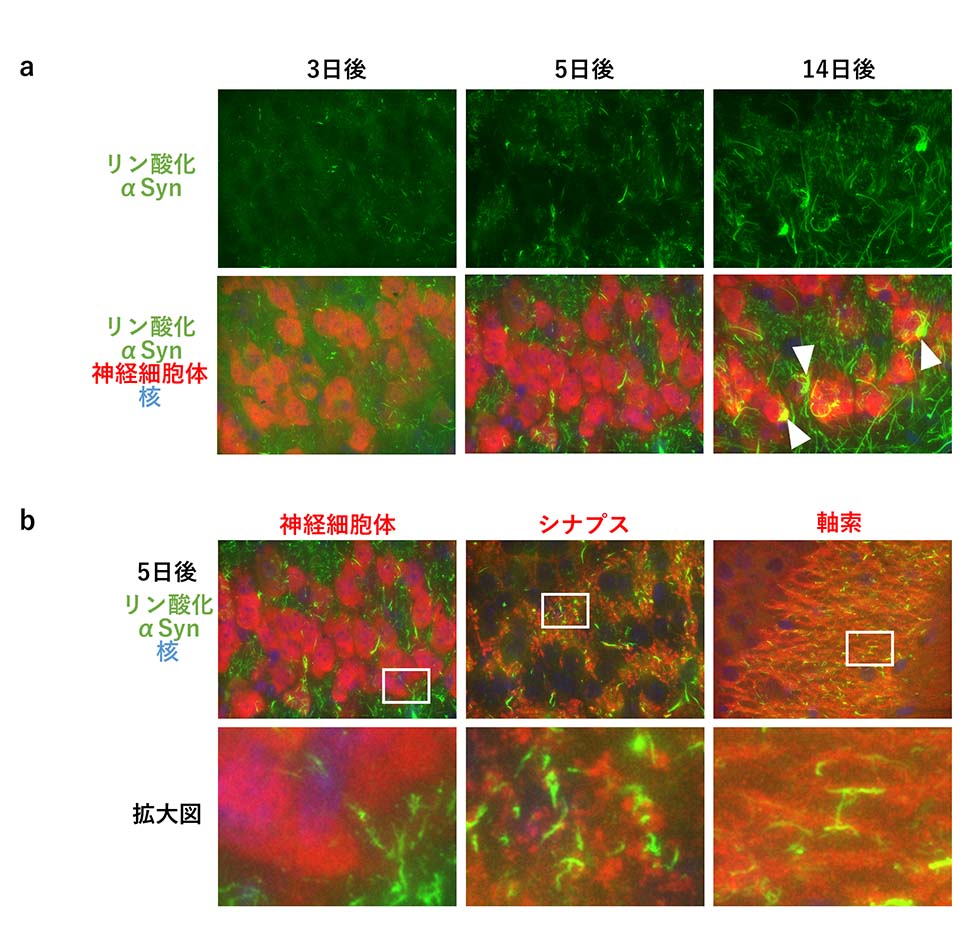
図1 野生型マウス脳内におけるシード依存的なリン酸化αシヌクレインの局在変化
- a.
- 試験管内で形成したαシヌクレイン凝集体を野生型マウスの海馬に注入後3,5,14日でのリン酸化αシヌクレイン(αSyn)の局在(上段)と神経細胞体マーカ―(NeuN)との共染色像(下段)。¬14日後になると神経細胞体に凝集体状のリン酸化αシヌクレインが蓄積していることがわかる(白矢頭)。
- b.
- 注入後5日でのリン酸化αシヌクレインと各種神経細胞マーカーとの共局在。リン酸化αシヌクレインは神経細胞体マーカー(NeuN;左)とは共局在しないが、シナプスマーカー(シナプシンI;中央)や軸索マーカー(タウ;右)とは共局在することがわかる。